В ячейках высокочастотного титрования электроды не соприкасаются с исследуемым раствором, что является одним из существенных достоинств метода.
2.2.2. Решение типовых задач по теме «Кондуктометрический анализ»
Задача 1. Сопротивление ячейки с 0,1 моль-экв/л раствора NaCl равно 46,8 Ом. Площадь каждого электрода 1,50 см3, а расстояние между ними 0,75 см. Определить удельную и эквивалентную электрическую проводимость.
Решение: Электрическая проводимость раствора вычисляется по формуле:
.![]() См.
См.
Рассчитываем удельную электрическую проводимость:
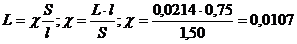 Ом-1 .см-1=0,0107 См . см-1=1,07 См . м-1
Ом-1 .см-1=0,0107 См . см-1=1,07 См . м-1
Рассчитываем эквивалентную электрическую проводимость:
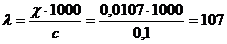 Ом-1 . см2 . экв-1=107 См . см2 . экв-1 =1,07 . 10-4 См . м2 . экв-1
Ом-1 . см2 . экв-1=107 См . см2 . экв-1 =1,07 . 10-4 См . м2 . экв-1
Ответ: c = 1,07 См. м-1; l = 1,07 . 10-4 См . м2 . экв-1 .
Задача 2. При кондуктометрическом титровании 50 мл раствора HCl 0,01 моль-экв/л NaOH были получены следующие данные
VNaOH,мл 0 2,0 4,0 6,0 8,0 10,0
c См. м-1 1,50 1,09 0,67 0,63 0,99 1,35
Рассчитать концентрацию HCl по данным кондуктометрического титрования.
Решение: Строим график кондуктометрического титрования в координатах: c - V (удельная электрическая проводимость – объем раствора титранта ) и определяем по графику точку эквивалентности, 5,0 мл раствора NaOH. Рассчитываем молярную концентрацию эквивалента раствора HCl из соотношения:
С HCl . V HCl = СNaOH . VNaOH
![]() моль-экв/л
моль-экв/л
Ответ: 0,001 моль-экв/л.
2.2.3. Контрольные вопросы по теме «Кондуктометрический анализ»
Измерение какого свойства лежит в основе кондуктометрического анализа? В каких единицах это свойство измеряется и с помощью каких устройств? Какие свойства в кондуктометрии принято обозначать символами c и l? Как практически определяют концентрацию методом прямой кондуктометрии? Почему в основном используется графический путь решения? Какой вид имеет градуировочный график? Какие определения невозможно выполнить методом прямой кондуктометрии: а) определение качества дистиллированной воды; б) содержания натрия и калия в морской воде; в) общего содержания примесей в технической серной кислоте; г) общего содержания солей в минеральных водах? Ответ поясните. Охарактеризуйте основные узлы прибора для кондуктометрического титрования. Изобразите и объясните ход кривой титрования смеси сильной и слабой кислот щелочью ( на любом конкретном примере). Как найти объемы, пошедшие на титрование каждого из компонентов? Как находят точку эквивалентности, если на кривой титрования нет четко выраженного излома? Какие из перечисленных достоинств следует отнести к методу кондуктометрического титрования: а) высокая точность; б) высокая чувствительность; в) возможность титрования мутных и окрашенных растворов; г) возможность анализа смесей двух веществ без предварительного разделения; д) возможность титрования в присутствии посторонних электролитов? В чем сущность высокочастотного титрования? Каковы особенности измерительной аппаратуры высокочастотного титрования? Какие виды кондуктометрии используются в анализе?
2.3. Кулонометрический метод анализа
2.3.1. Основные законы и формулы
В основе кулонометрических методов лежат законы электролиза Фарадея.
Законы Фарадея формулируются следующим образом
Количество электропревращенного (восстановленного или окисленного) в процессе электролиза вещества прямо пропорционально количеству прошедшего электричества. Массы различных веществ, выделенных или растворенных при прохождении одного и того же количества электричества, пропорциональны их электрохимическим эквивалентам.Электрохимический эквивалент – это масса вещества, выделившегося на электроде (или растворившегося с электрода) в процессе электролиза при протекании единицы количества электричества, т. е. 1 Кл.
Суть законов Фарадея заключается в том, что для выделения одного моля любого вещества в процессе электролиза необходимо затратить одно и то же количество электричества, называемое числом Фарадея (F). F =96500 Кл.
![]() ,
,
Где Q – количество электричества (Кл), необходимое для выделения на электроде m граммов вещества с молярной массой эквивалента, равной М / n (М – молярная масса определяемого вещества; n – число электронов, участвующих в электродной реакции).
Q= I . t ,
Где I – сила тока, А (ампер); t – время электролиза, с (секунда)
Ясно, что применение этой формулы требует, чтобы электролиз протекал со 100%-ной эффективностью тока (или со 100%-ным выходом по току), что возможно только в отсутствие конкурирующих реакций.
Различают два основных вида кулонометрических определений – прямую кулонометрию и кулонометрическое титрование. В методах прямой кулонометрии электрохимическому превращению непосредственно в кулонометрической ячейке подвергается анализируемое вещество. В методе кулонометрического титрования электролизу подвергается вспомогательное вещество, а еще продукт электролиза – титрант – реагирует с определяемым веществом. Кулонометрические определения могут проводиться при постоянном потенциале (потенциометрическая кулонометрия) и постоянной силе тока (амперостатическая кулонометрия). В прямой кулонометрии широко применяют потенциостатические методы. Массу определяемого вещества рассчитывают по приведенной выше формуле.
В методе кулонометрического титрования используются установки с постоянной силой тока. Содержание определяемого вещества рассчитывают по количеству электричества, израсходованного на генерацию необходимого для реакции с анализируемым веществом количества титранта. Кулонометрическое титрование в значительной степени сохраняет аналогию с другими титриметрическими методами. Основное различие относится к приготовлению титранта. В обычных титриметрических методах его готовят заранее готовят по точной навеске или стандартизируют по специальным установочным веществам, а в методах кулонометрического титрования титрант генерируется электрохимическим методом.
Как и любом другом титровании, в кулонометрическом тоже необходимо выбрать метод определения точки эквивалентности. Можно применять потенциометрический, амперометрический, спектрофотометрический и другие методы.
В кулонометрическом титровании используются химические реакции различных типов: кислотно-основные, окислительно-восстановительные, комплексообразования и др. Различные восстановители [Fe2+ , Sn2+ , Sb3+, As3+ и др.] могут быть оттитрованы, например, перманганатом, который легко генерируется из MnSO4 в ячейке с платиновым анодом. При анодном растворении хрома в серной кислоте получается дихромат-ион, который также может быть использован для этого титрования. В кулонометрическом титровании широко применяют также, например, свободный бром, генерируемый на платиновом аноде из хлорводородного бромида калия.
Установка для кулонометрического титрования при постоянной силе тока содержит следующие основные узлы: 1) источник постоянного тока; 2) устройство для определения количества электричества; 3) электрическую ячейку с генераторным электродом; 4) индикаторную систему для определения конца титрования; 5) хронометр для определения продолжительности электролиза.
Индикаторная система служит для индикации конечной точки титрования (к. т. т.). Наиболее часто для этой цели используют амперометрический и потенциометрический методы. В ячейку вводят индикаторные электроды: два платиновых электрода (при амперометрической индикации) или платиновый и каломельный электроды ( при потенциометрической индикации). Силу тока или разность потенциалов измеряют соответствующими приборами, входящими в комплект установки для титрования (блок индикации). Иногда для определения к. т.т. используют фотометрический метод, помещая ячейку в кюветное отделение фотоэлектроколориметра и измеряя светопоглощение в ходе титрования. В отдельных случаях конец титрования устанавливают визуально, например по появлению окраски раствора, вызванной избытком титранта. Приборостроительная промышленность серийно выпускает кулонометрические титраторы, в которых для индикации конечной точки титрования используется амперометрический или потенциометрический методы.
Решение типовых задач по теме «Кулонометрическое титрование»
Задача 1. На полное восстановление цинка в кулонометрии понадобилось 26 мин при силе тока 100 мА. Определить содержание (г) и концентрацию (моль/л) цинка в растворе, если на кулонометрический анализ было взято 10 мл раствора.
Решение: Рассчитываем содержание (г) цинка по формуле:
![]() ;
; ![]() г в 10 мл раствора, тогда в 1 л будет содержатся 5,285 г/л
г в 10 мл раствора, тогда в 1 л будет содержатся 5,285 г/л ![]() моль/л
моль/л
Ответ: mZn2+ =0,05285 г ; сZn2+ = 0,0808 моль/л.
Задача 2. На кулонометрическое титрование 10 мл раствора Na2S2O3 иодом, генерируемым в кулонометрической ячейке понадобилось 22 мин при силе тока 300 мА. Определить количество затраченного электричества и молярную концентрацию эквивалента раствора Na2S2O3.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 |




