3) Определение порядка реакции в случае, когда в ней принимает участие одно вещество.
Кинетическое уравнение
![]() (5)
(5)
где ![]() – концентрация вещества
– концентрация вещества ![]() ,
, ![]() – время,
– время, ![]() – константа скорости реакции,
– константа скорости реакции, ![]() – неизвестный порядок реакции.
– неизвестный порядок реакции.
Задача: Пусть дано уравнение (6) и начальное условие 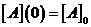 . Найти
. Найти ![]() .
.
Решение. Введем переменную ![]() :
: 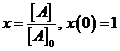 . Тогда (6) примет вид
. Тогда (6) примет вид
![]() или
или ![]() (7)
(7)
где 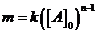 ,
, 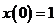 ,
, 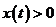 .
.
В результате интегрирования получим
![]() (8)
(8)
Выделим два момента времени ![]() и
и ![]() , найдем
, найдем ![]() и
и ![]() . Подставим в (8):
. Подставим в (8): 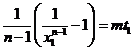 ;
; 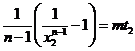 откуда следует, что
откуда следует, что 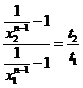 . Выберем
. Выберем ![]() и
и ![]() так, чтобы выполнялось
так, чтобы выполнялось ![]() . Тогда
. Тогда 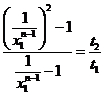 , откуда
, откуда 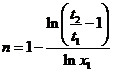 .
.
В дальнейшем будем рассматривать химические реакции, протекающие в замкнутой системе, для которых концентрации исходных веществ и продуктов реакции связаны соотношениями 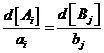 . Обозначим исходные концентрации через
. Обозначим исходные концентрации через ![]() и
и ![]() и проинтегрируем данное соотношение. Получим
и проинтегрируем данное соотношение. Получим 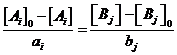 . Последнее соотношение можно обозначить через переменную
. Последнее соотношение можно обозначить через переменную ![]() :
:
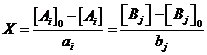 (9)
(9)
§ 2. Математические модели некоторых химических процессов.
Необратимые реакции первого порядка.
Задача 1. Некоторое вещество ![]() , концентрация которого в момент
, концентрация которого в момент ![]() равна
равна ![]() , подвергается превращению в процессе необратимой реакции первого порядка при постоянных условиях. Требуется получить уравнение кинетической линии и найти константу скорости реакции.
, подвергается превращению в процессе необратимой реакции первого порядка при постоянных условиях. Требуется получить уравнение кинетической линии и найти константу скорости реакции.
Решение. ![]() . Кинетическое уравнение:
. Кинетическое уравнение: 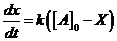 ,
, 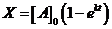 ,
, 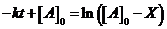 ,
, 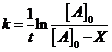 .
.
Для нахождения ![]() выбираем экспериментальные точки
выбираем экспериментальные точки ![]() , находят по формуле
, находят по формуле ![]() , в качестве
, в качестве ![]() берут среднее арифметическое значение.
берут среднее арифметическое значение.
Обратимые реакции первого порядка.
Рассмотрим одностадийную обратимую реакцию первого порядка:
![]() .
.
Выражение для скорости превращения вещества ![]() будет иметь вид
будет иметь вид ![]() . Вспомним (9):
. Вспомним (9): ![]() . Получим кинетическое уравнение
. Получим кинетическое уравнение ![]() или
или ![]() , где
, где ![]() .
.
Задача 2. Некоторое вещество ![]() , концентрация которого в момент
, концентрация которого в момент ![]() равна
равна ![]() , участвует в обратимой реакции, где оба процесса являются реакциями первого порядка. Требуется получить уравнение кинематической кривой и найти
, участвует в обратимой реакции, где оба процесса являются реакциями первого порядка. Требуется получить уравнение кинематической кривой и найти ![]() .
.
Решение. ![]() , где
, где ![]() .
. ![]() отсюда следует, что
отсюда следует, что ![]() . Начальное условие:
. Начальное условие: ![]() откуда следует, что
откуда следует, что ![]() ;
; ![]() ;
; 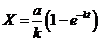 .
.
Найдем выражение для концентраций исходного вещества и продукта:
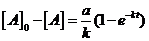 . Отсюда
. Отсюда 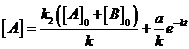 ;
; 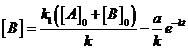 .
.
Устремим ![]() :
:
![]() ;
; ![]() .
.
Выразим ![]() :
:
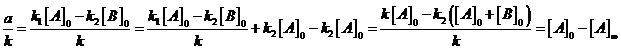
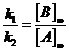 . Найдем
. Найдем ![]() : выражение для
: выражение для ![]() запишем в виде
запишем в виде ![]() . Отсюда
. Отсюда ![]() , отсюда
, отсюда 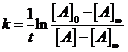 . Получим
. Получим ![]() ;
; ![]() , где
, где 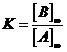 .
.
Обратимые реакции разных порядков.
Пример. ![]() . Будем исходить из допущения, что разложение
. Будем исходить из допущения, что разложение ![]() – реакция второго порядка, обратимая реакция – первого порядка.
– реакция второго порядка, обратимая реакция – первого порядка.
![]() ,
, ![]()
![]() . С другой стороны
. С другой стороны ![]() . Исключив
. Исключив ![]() , получим
, получим

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |




