при нагревании, так как необходимо разрушение Пи – связей в молекулярном строении
алкинов.
Химические реактивы и приборы:
СаС2 – карбид кальция, бромная вода, раствор КМп О4
1) Штатив с пробирками
2) Газоотводная трубка с изогнутым коленом ( для опытов №2,3)
3) Газоотводная трубка прямая с оттянутым концом ( для опыта № 4)
4) Спиртовки, спички.
Ход работы.
Опыт №1. Получение ацетилена из карбида кальция.
Подобрать небольшой кусочек карбида кальция, бросить его в пробирку и прилить чуть-–
чуть воды. Наблюдается образование и выделение газа. Какой это газ? Запишите свои
наблюдения, уравнение реакции и вывод.
Опыт №2. Бромирование ацетилена.
Подберите к пробирке газоотводную трубку с изогнут ым коленом, подготовьте другую
пробирку с бромной водой. Получите в 1–ой пробирке ацетилен (из 1–го опыта) и
пропустите его через бромную воду до полного обесцвечивания раствора. Записать свои
наблюдения, уравнения реакции и сделать вывод о скорости бромирования алкинов:
почему оно растянуто во времени?
Опыт №3. Окисление ацетилена раствором КМп О4.
Подготовьте пробирку с раствором КМп О4. Ацетилен получите в том же устройстве, что
опыте №2, добавив туда еще кусочек карбида кальция и воды, пропустите ацетилен
через раствор КМп О4 до изменения окраски от бурой до бледно–желтой.
Запишите наблюдения, уравнения реакции и сделайте вывод.
Опыт №4. Горение ацетилена.
К пробирке, где получали ацетилен, подберите прямую газоотводную трубку, добавьте в
пробирку кусочек карбида, немного воды, закройте пробкой с газоотводной трубкой и
зажгите выделяющийся ацетилен в конце газоотводной трубки.
Выньте пробку с трубкой из пробирки и, таким образом, прекратите горение ацетилена.
Запишите наблюдения, уравнения реакции и объясните, почему была копоть, чего не
хватало для полного сжигания ацетилена.
Контрольные вопросы:
1. Какие углеводороды называются алкинами?
2. Какая особенность строения алкинов?
3. Назовите гомологический ряд алкинов.
4. Приведите все изомеры гептина – 1.
5. Где используются алкины?
Практическая работа №1
«Предельные и непредельные углеводороды».
Решение экспериментальных задач.
Цель работы: Закрепить теоретические знания о предельных и непредельных
углеводородах с помощью решения экспериментальных задач.
Задание.
1. Объясните, как опытным путем можно отличить метан от водорода.
2. Напишите и дайте название трем углеводородам, соответствующим формуле
СnН2n+2, СnН2n, СnН2n-2.
3. Напишите структурные формулы для 1,2– диметилбутана и
1,2–диметилциклобутана.
4. Напишите все возможные изомеры для пентана, пентен–1 и пентин –1.
Укажите, в каком случае, у какого углеводорода изомеров больше.
5. Сколько вторичных углеводородов имеет октан?
6. Рассчитайте плотность этилена по водороду, по кислороду, по воздуху.
7. Выведите молекулярную формулу углеводорода, содержащего 88,9% углерода,
его плотность по воздуху 1,862.
Назовите это вещество и приведите два любых изомера.
8. Укажите, какие углеводороды вступают в реакцию гидрирования:
пропан, цикло– пропан, пропен, пропин.
Ответ подтвердите уравнениями реакций.
9. Рассчитайте, какой объем кислорода расходуется при сжигании 13 г ацетилена.
Напишите реакцию горения ацетилена.
10. Как из ацетилена получить 1,2– дихлорэтан.
Ответ подтвердите уравнениями реакций.
Лабораторная работа№4
«Свойства бензола».
Цель работы: 1. Закрепление теоретических знаний о свойствах бензола;
2. Приобретение практических навыков при выполнении лабораторных
экспериментов.
Приборы и реактивы: этиловый спирт – С2Н5ОН, сульфат меди– CuSO4, K2 Cr 2 O7 –бихромат калия, Н2SO4– серная кислота, метиловый оранжевый, фенолфталеин, синий лакмус, штатив с пробирками, спиртовки.
Теоретическое обоснование.
Первым представителем ароматических углеводородов является бензол – легкокипящая бесцветная жидкость с ароматным запахом, не растворимая в воде. При температуре ниже 5 градусов С бензол из жидкого состояния переходит в белую кристаллическую массу.
Ход работы.
Опыт №1. Реакция бромирования бензола.
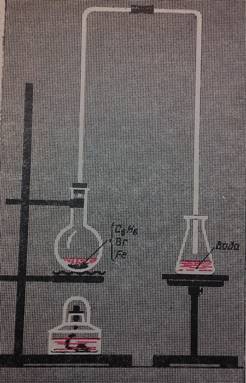
В колбу поместить небольшое количество жидкого бензола, добавить бром и железные
стружки в виде катализатора. Отверстие колбы закрыто пробкой с изогнутой стеклянной трубкой, которая выходит в емкость – приемник. Содержимое колбы нагревается от спиртовки и через некоторое время в изогнутой стеклянной трубке появляется дымок. В приемной колбе находится раствор нитрата серебра, куда капает из трубки тяжелая вязкая жидкость – бромбензол.
Запишите наблюдения, уравнения реакции и сделайте вывод.
Опыт №2. Реакция нитрования бензола.
Реакция протекает в колбе, прикрепленной на штативе, внутри находится бензол,
добавляется смесь концентрированных азотной и серной кислот. Все нагревается и через
некоторое по изогнутой трубке в колбу – приемник начинает стекать тяжелая желтоватая
жидкость с запахом миндаля. Это образовался нитробензол.
Написать уравнение реакции.
Опыт №3. Реакция гидрирования бензола.
Колбу с бензолом предварительно нагревают до выделения паров бензола.
Пропускают водород – идет реакция гидрирования. Через некоторое время образуется
новое вещество – циклогексан.
Написать свои наблюдения и уравнение реакции.
Контрольные вопросы:
1. Почему бензол является ароматическим углеводородом?
2. Назовите гомологи бензола.
3. Какой ученый вывел формулу бензола?
4. Назовите область применения бензола.
Лабораторная работа №5
«Фенол и его свойства»
Цель работы: 1. Практическое изучение свойств фенола;
2. Формирование навыков лабораторного эксперимента.
Химические реактивы и приборы: фенол, пирокатехин, резорцин, пирогаллол, гидрохинон, раствор NaОH, HNO3 (конц), раствор FeCl3, бромная вода.
Пробирки, стеклянные палочки, спиртовки.
Теоретическое обоснование.
Фенолами называются органические соединения, имеющие в своем строении одну гидроксильную группу –ОН, присоединенную к бензольному кольцу (одноосновный фенол),
имеющие в своем строении две и более групп –ОН, присоединенных к бензольному кольцу (многоосновные фенолы).
Ход работы.
Опыт №1. Растворение фенола в воде.
В пробирку помещают несколько капель фенола, прибавляют столько же H2O и взбалтывают. Образуется мутная жидкость – эмульсия фенола. Дать немного отстояться. Что происходит?
Указать образовавшийся цвет и запах, сделать вывод.
Опыт №2. Получение трибромфенола:
В пробирку наливаем 2мл бромной воды и столько же фенола. Вода обесцвечивается и мутнеет. При этом образуется белый осадок трибромфенола.
Написать уравнение реакции, дать название полученному веществу, указать образовавшийся цвет и запах, сделать вывод.
Опыт №3. Нитрование фенолов.
В пробирку помещают фенол и немного H2O, встряхивают до получения однородного раствора. В другую пробирку помещают 3 мл HNO3 (конц),
1 мл H2O, затем это приливают по каплям к жидкому фенолу, встряхивают и охлаждают под краном. Затем реакция идет очень энергично. Смесь выливают в пробирку с водой, зыкрывают пробкой с газоотводной трубкой и отгоняют нитрофенол в чистую сухую пробирку.
Написать уравнение реакции, дать название полученному веществу, указать образовавшийся цвет и запах, сделать вывод.
Опыт №4. Цветные реакции многоатомных фенолов.
В 1 пробирку налить 3к. 1% р-ра пирокатехина.
В 2 пр. - 3к. 1% р-ра резорцина.
В 3 пр. - 3к. 1% р-ра гидрохинона.
В 4 пр. – 3к. 1% р-ра пирогаллола.
В каждую пробирку прибавить по 1к. 0,1 N р-ра FeCl3
Написать уравнения реакций, дать название полученным веществам, указать образовавшийся цвет и запах, сделать вывод.
Опыт №5. Окисление многоатомных фенолов в присутствии NaOH.
В пробирки помещают по несколько капель эмульсий фенола, резорцина, гидрохинона, пирогаллола, пирокатехина и добавляют в каждую пробирку по несколько капель раствора NaOH.
Написать уравнение реакции, дать названия полученным веществам, указать образовавшийся цвет и запах, сделать вывод.
Контрольные вопросы:
1. Что называется фенолами?
2. Общая формула фенолов.
3. Является ли гидрохинон одноосновным фенолом?
4. Назовите область применения фенолов.
5. Назовите изомеры пирогаллола.
Практическая работа №2
«Ароматические углеводороды».
Решение экспериментальных задач.
Цель работы: Закрепить теоретические знания об ароматических углеводородах с
помощью решения экспериментальных задач.
Задание.
1.Какое противоречие существует между структурной формулой Кекуле и
свойствами бензола и как это противоречие объясняет электронная теория?
2. Распознайте на основании химических свойств три жидкости: бензол – С6Н6
гексан – С6Н14, гексен – С6Н12.
3. Напишите реакции, показывающие сходство бензола с предельными и
непредельными углеводородами, а также укажите различие их свойств.
4.Составьте уравнения реакций, отражающих получение бензола из метана.
Укажите условия их протекания.
5.Напишите структурную формулу ароматического углеводорода, если его
молекулярная формула – С7Н8.. Дайте название этому углеводороду.
6.Реакцией дегидрирования этилциклогексан можно превратить в ароматический
углеводород. Напишите уравнение реакции, подтверждающее данное
высказывание. Дайте название этому углеводороду.
7.Определите молекулярные массы для бензола, толуола, стирола.
8.Напишите реакции нитрования бензола, толуола.
В чем отличие протекания этих реакций?
9.Найдите плотность бензола, фенола и толуола по водороду.
Сделайте сравнение. Дайте вывод.
10.Напишите реакцию окисления толуола.
Лабораторная работа №6

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




