«Свойства спиртов».
Цель работы: 1. Закрепление теоретических знаний о свойствах спиртов.
2. Приобретение практических навыков.
Приборы и реактивы: этиловый спирт – С2Н5ОН, сульфат меди– CuSO4, K2 Cr 2 O7 –бихромат калия, Н2SO4– серная кислота, метиловый оранжевый, фенолфталеин, синий лакмус, штатив с пробирками, спиртовки.
Теоретическое обоснование.
Спиртами называются органические соединения, имеющие одну или несколько гидроксильных групп – ОН, присоединенных к углеводородному радикалу.
Спирты с одной гидроксильной группой называются одноатомными;
с двумя – двухатомными, более групп – ОН называются многоатомными.
Ход работы.
Опыт №1. Взаимодействие этилового спирта с сернокислой медью.
2С2Н5ОН + CuSO4 = (С2Н5О)2Cu + Н2SO4
В сухую пробирку приливают насыщенный раствор сульфата меди и добавляют по каплям немного этилового спирта.
Смесь нагревают и наблюдают протекание реакции.
Записать наблюдения, указать изменение цвета, сделать вывод.
Опыт №2. Взаимодействие этилового спирта с бихроматом калия.
В сухую пробирку приливают насыщенный раствор бихромата калия K2 Cr 2 O7 и добавляют по каплям немного этилового спирта С2Н5ОН.
Смесь нагревают и наблюдают протекание реакции.
Записать наблюдения, указать изменение цвета, сделать вывод.
Опыт №3. Взаимодействие этилового спирта с серной кислотой.
В сухую пробирку приливают 1 N– раствор серной кислоты Н2SO4, и добавляют по каплям немного этилового спирта С2Н5 ОН.
Смесь нагревают и наблюдают протекание реакции.
Записать наблюдения, указать изменение цвета, сделать вывод.
Опыт №4. Качественная реакция трехатомного спирта глицерина.
В сухую пробирку прилить немного глицерина. В другую пробирку добавляют по каплям свежеприготовленный раствор гидроксида меди в присутствии щелочи натрия.
Образуется раствор ярко– синего цвета – глицерат меди.
Напишите уравнение реакции, сделайте вывод.
Контрольные вопросы:
1. Назвать гомологический ряд спиртов.
2. Написать 2 изомера гексанола–1.
3. Назвать многоатомные спирты.
4. Каким по основности спиртом является этиленгликоль?
5. Где применяются спирты?
6. Какова растворимость глицерина в воде?
Лабораторная работа №7
«Получение новых веществ из этилового спирта».
Цель работы: 1. Закрепление теоретических знаний об электронном строении этилового
спирта.
2. Приобретение практических навыков.
Приборы и реактивы: этиловый спирт – С2Н5ОН, сульфат меди– CuSO4, K2 Cr 2 O7 –бихромат калия, Н2SO4– серная кислота, метиловый оранжевый, фенолфталеин, синий лакмус, штатив с пробирками, спиртовки.
Теоретическое обоснование.
Этиловый спирт СН3–СН2–ОН – бесцветная жидкость со своеобразным запахом, легче воды, хорошо растворяется в воде, температура кипения ниже, чем у воды и равна 78 градусам. Этиловый спирт или этанол является растворителем для многих неорганических и органических веществ.
Ход работы.
Опыт №1. Получение водорода из этилового спирта.

Поместим в пробирку со спиртом немного натрия. Тотчас начинается реакция с выделением газа – водорода. Если выполнить расчет, то можно сделать вывод:
Из каждой молекулы спирта при реакции с натрием выделяется только один атом водорода. Это водород гидроксильной группы, он более подвижен и слабо связан с атомом углерода
Опыт №2. Получение бромэтана из этилового спирта.
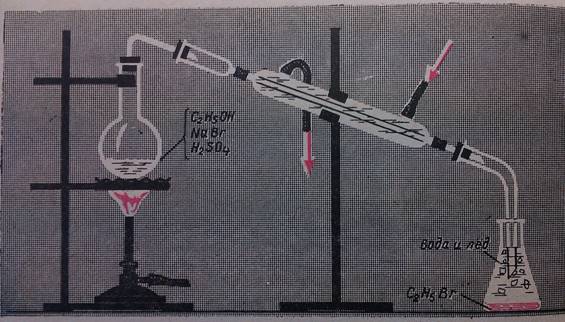
В колбу емкостью 100 мл поместить смесь этилового спирта с серной кислотой (10 мл), добавить постепенно 3 мл воды и 5 г бромида калия или бромида натрия. Закрыть колбу пробкой с холодильником, конец которого поместить в пробирку с холодной водой. Нагревать смесь осторожно на водяной бане или через сетку. В приемнике постепенно образуется тяжелая жидкость. Это– бромэтан. Его перелить в делительную воронку и аккуратно отделить от воды.
Контрольные вопросы:
1. Какой атом водорода принимает участие в реакциях присоединения?
2. Какие новые соединения можно получить из этилового спирта.?
3. Почему этиловый спирт хорошо растворим в воде?.
4. Дать название этилового спирта по международной номенклатуре.
5. В каких целях используется этиловый спирт?
Лабораторная работа №8
«Cвойства альдегидов»
Цель работы: 1. Закрепление теоретических знаний о свойствах альдегидов,
2. Формирование навыков лабораторного эксперимента.
Теоретическое обоснование.
Альдегидами называются органические соединения, имеющие в своем строении карбонильную группу – СОН, присоединенную к углеводородному радикалу.
Химические реактивы и приборы:
Формалин, аммиачный раствор оксида серебра, сульфат меди – CuSO4, гидроксид натрия NaOН, этиловый спирт – С2Н5ОН,, медная проволока, штатив с пробирками, спиртовка, спички.
Ход работы.
Опыт №1. Получение альдегида из этилового спирта.
Налить в пробирку немного этилового спирта, накалить медную спираль на пламени горелки, чтобы медь покрылась черным налетом оксида и быстро опустить в пробирку с этиловым спиртом. Повторить эту операцию несколько раз, пока не появится запах альдегида.
Написать уравнение реакции, сделать вывод.
Опыт №2. Получение водорода из этилового спирта.
Формальдегид вместе с водородом пропускают над никелевым катализатором.
Появляется запах спирта – это проиэошло превращение формальдегида в метиловый спирт. Написать уравнение реакции, сделать вывод.
Опыт №3. Реакция «Серебряного зеркала».
В чистую пробирку налить аммиачный раствор оксида серебра, 4–5 капель формалина и смесь нагреть. На стенках пробирки появляется осадок металлического серебра.
Написать уравнение реакции, сделать вывод.
Опыт №4. Качественная реакция формальдегида.
Приготовить свежий раствор гидроксида меди, соединив в одной пробирке немного сульфата меди и гидроксида натрия. К образовавшемуся осадку прилить 2 мл формалина и смесь нагреть до изменения цвета.
Написать уравнение реакции, сделать вывод.
Контрольные вопросы:
1. Какая группа атомов называется карбонильной?
2. Назовите гомологический ряд альдегидов, начиная с метаналя.
3. Напишите изомеры гептаналя.
4. Назовите область применения муравьиного альдегида, уксусного альдегида.
5. Где применяется реакция «серебряного зеркала»?
Практическая работа №3
«Свойства карбонильных соединений»
Решение экспериментальных задач.
Цель работы: Закрепить теоретические знания о карбонильных
соединениях с помощью решения экспериментальных задач.
Задание.
1. Сколько изомеров имеет пентаналь, напишите их структурные формулы и дайте
названия по систематической номенклатуре.
2. Напишите химическими реакциями получение этилового спирта из ацетилена.
Присутствует ли в промежуточной стадии альдегид? Если – да, то дайте ему название и подчеркните структурную формулу этого альдегида.
3. В реакции окисления бензилового спирта С6Н5–СН2ОН получается бензойный
альдегид С6Н5–СОН. Какой побочный продукт выделяется в ходе данного взаимодействия.
4. Выделите иэ ряда органических веществ карбонильные соединения и напишите их химические формулы:
Метанол, метаналь, ацетилен, ацетон, уксусная кислота, уксусный альдегид.
5. Напишите структурные формулы для 2,3–диметилпентаналя,
2,3,4– триметилгексаналя.
6. Укажите вторичный углерод в цепи ацетона.
7. Напишите, как из уксусного альдегида получить в две стадии бромэтан.
Составьте уравнения реакций.
8. Как реакцией гидрирования можно получить из формальдегида метиловый спирт?
Напишите уравнение реакции.
9. Определите молекулярные массы уксусного альдегида и пропионового альдегида. Сделайте сравнение, напишите вывод.
10. Определите плотность этанола по водороду.
Лабораторная работа №9
«Свойства карбоновых кислот».
Цель работы: 1. Практическое изучение свойств карбоновых кислот;
2. Формирование навыков лабораторного эксперимента.
Химические реактивы и материалы:
1. Уксусная кислота
2. Металлический цинк
3. Оксид меди
4. Раствор медного купороса – CuS04
5. Раствор едкого натрия – NaОH
6. Карбонат кальция (мел) –СаСО3
7. Кристаллический уксуснокислый натрий
8. Фенофталин
9. Пробирки, стеклянные палочки, спиртовки.
Теоретическое обоснование.
Карбоновыми называются органические кислоты, имеющие в своем строении карбоксильную группу –СООН, присоединенную к углеводородному радикалу. Кислоты с одной гидроксильной группой называются одноосновными, с двумя группами – двухосновными, с тремя и более – многоосновными карбоновыми кислотами.
Ход работы.
Опыт № 1. Получение уксусной кислоты.
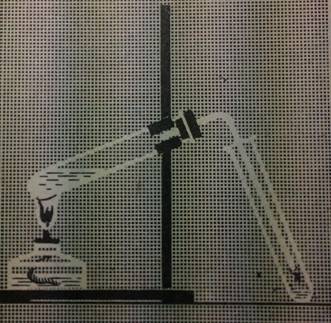
Поместить в пробирку 3 г ацетата натрия и прибавить 3 мл раствора серной кислоты. Пробирку закрыть пробкой с газоотводной трубкой, конец которой помещен в другую пробирку – приемник. Смесь нагреть, пока не соберется новая жидкость в приемнике. Появился запах уксусной кислоты.
Напишите свои наблюдения.
Опыт № 2. Взаимодействие карбоновых кислот с металлами
Поместить в пробирку 1-2 гранулы цинка и прилить 2 мл уксусной кислоты.
Что наблюдается? Подогрейте пробирку. Изменился ли ход действия?
Напишите уравнение реакции, укажите образовавшийся запах, дайте название полученному веществу, сделайте вывод.
Опыт №3. Взаимодействие карбоновых кислот с оксидами металлов
Поместите в пробирку немного оксида меди, прилейте 1,5-2 мл уксусной кислоты и подогрейте до изменения окраски.
Запишите наблюдения, уравнения реакции, назовите полученное вещество, сделайте вывод.
Опыт № 4. Взаимодействие карбоновых кислот с основаниями

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




