Сначала приготовим свежий гидрооксид меди. Для этого поместим в пробирку 1 мл р-ра CuS04 и 1 мл раствора NаOH. Затем к осадку гидрооксида меди прилейте 0,5-1 мл уксусной кислоты. Что наблюдается?
Запишите наблюдения, уравнения реакций, сделайте вывод.
Опыт № 5. Взаимодействие карбоновых кислот с солями
Поместите в пробирку немного карбоната кальция (мрамор, мел)
И прилейте 0,5 мл к уксусной кислоты. Что наблюдается?
Запишите наблюдения, укажите образовавшийся запах, напишите уравнения реакций, сделайте вывод.
Опыт № 6. Гидролиз солей карбоновых кислот
В пробирку поместите немного кристаллического ацетата натрия, растворите 3-5 мл дистиллированной воды и капните 2-3 капли раствора фенолфталеина.
Что наблюдается? Какова реакция раствора ацетата натрия и почему? Подогрейте содержимое пробирки. Что наблюдается?
Запишите наблюдения, уравнения реакции, сделайте вывод.
Контрольные вопросы:
1.Какие кислоты называются карбоновыми?
2.Написать общую формулу карбоновых кислот.
3.Написать несколько гомологов метановой кислоты.
4.Какую основность имеет щавелевая кислота.
5.Назовите область применения уксусной кислоты.
Лабораторная работа №10
«Получение и свойства эфиров».
Цель работы: 1. Практическое изучение свойств эфиров и способов их получения;
2.Формирование навыков лабораторного эксперимента.
Теоретическое обоснование.
Сложными эфирами называются органические соединения, полученные реакцией этерификации – взаимодействием карбоновых кислот со спиртами в присутствии сильных минеральных кислот, так как ионы водорода оказывают каталитическое действие.
Химические реактивы и материалы:
Эиловый спирт, уксусная кислота, серная кислота; колба, пробка с водяным или воздушным холодильником, нагревательный прибор.
Ход работы.
Опыт №1. Получение этилового эфира уксусной кислоты.
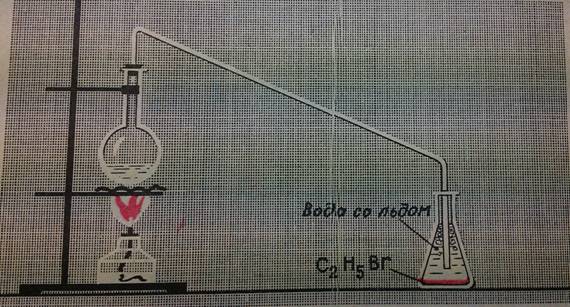
Налить в колбу 10 мл смеси этилового спирта, уксусной кислоты и серной кислоты.
Присоединить к колбе водяной или воздушный холодильник, конец которого опущен в колбу – приемник с холодной водой. Нагреть смесь в 1–й колбе на водяной бане или через металлическую сетку. Нагревание прекратить, когда в колбе – приемнике соберется достаточное количество эфира.
Напишите уравнение реакции, укажите образовавшийся запах, дайте название полученному веществу, сделайте вывод.
Опыт №2. Гидратация эфира.
Полученный в 1- м опыте эфир взболтать с водой и отобрать при помощи делительной воронки. Часть эфира поместить в отдельную колбу, добавить воды, равной по объему и все нагревать до изменения состава содержимого. Что получилось? Написать уравнение реакции, сделать вывод.
Контрольные вопросы:
1. Написать реакцию получения метилового эфира муравьиной кислоты.
2. Написать общую формулу эфиров.
3. Что получается при гидролизе эфиров?
4. Назовите области применения эфиров.
5. Что называется реакцией этерификации?
Лабораторная работа №11
«Свойства жиров».
Цель работы: 1) Практическое изучение свойств жиров;
2) Формирование навыков лабораторного эксперимента.
3) Подкрепление знаний о высокомолекулярных соединениях.
Приборы и реактивы: Штатив с пробирками, спиртовка, спирт, бензин бромная вода, раствор ![]() ,
,![]() ,
, ![]() (или KOH).
(или KOH).
Теоретическое обоснование:
Жирами называются сложные эфиры высших карбоновых кислот.
Ход работы.
Опыт №1. Испытание жиров на растворимость в воде.
В три пробирки налейте 1 мл воды, спирта и бензина и поместите в них примерно по равному кусочку твердого жира или по нескольку капель растительного масла. Наблюдайте, что происходит при встряхивании пробирок. В какой жидкости жиры лучше растворяются?
Опыт №2. Испытание жиров на растворимость в спирте.
Несколько капель раствора жира в спирте и бензине нанесите на фильтрованную бумагу. Что наблюдается после испарения растворителя?
Опыт №3. Испытание жиров на растворимость в бензине.
.В три пробирки налейте 1 мл воды, спирта и бензина и поместите в них примерно по равному кусочку твердого жира или по нескольку капель растительного масла. Наблюдайте, что происходит при встряхивании пробирок. В какой жидкости жиры лучше растворяются?
1.В три пробирки налейте 1 мл воды, спирта и бензина и поместите в них примерно по равному кусочку твердого жира или по нескольку капель растительного масла. Наблюдайте, что происходит при встряхивании пробирок. В какой жидкости жиры лучше растворяются?
Опыт №4. Испытание жиров на растворимость в серной кислоте.
В две пробирки налейте равное количество серной кислоты и поместите в них: немного твердого жира и в другую пробирку несколько капель растительного масла. Наблюдайте, что происходит при встряхивании пробирок. В какой пробирке жиры растворяются лучше?
Опыт №5. Испытание жиров на растворимость в шелочи.
В две пробирки налейте равное количество едкого натра и поместите в них немного твердого жира и в другую пробирку несколько капель растительного масла. Наблюдайте, что происходит при встряхивании пробирок. В какой пробирке жиры растворяются лучше?
Контрольные вопросы:
1. Что называется жирами?
2. Какие жиры вы знаете?
3. Что входит в состав жидких жиров, твердых жиров?
4. Назовите область применения жиров.
5. Назовите ученых, которые синтезировали жиры.
Лабораторная работа №12
«Сравнение свойств мыла и синтетических моюших средств».
Цель работы: 1. Закрепление теоретических знаний по свойствам мыла.
2. Приобретение практических навыков лабораторного эксперимента.
Приборы и реактивы: растворы мыла и синтетических моющих средств, CuSO4– сульфат меди, NaOН– гидроксид натрия, Н2SO4– серная кислота, метиловый оранжевый, фенолфталеин, штатив с пробирками, спиртовки.
Теоретическое обоснование.
Мыла –это соли высших карбоновых кислот.
Натриевые соли высших карбоновых кислот – это твердые вещества, плохо растворимые в воде. Калиевые соли – это жидкие вещества, хорошо растворимые в воде.
В настоящее время широко используются синтетические моющие средства – продукты переработки нефти. СМС – это натриевые соли кислых сложных эфиров высших спиртов
и серной кислоты.
Ход работы.
Опыт №1. Определение рН растворов мыла и синтетических моющих средств.
В одну пробирку прилить немного раствора мыла, в две другие – по несколько капель разных моющих средств в жидком состоянии по–отдельности. Испытать эти растворы на действие индикаторов. Моющее средство, предназначенное для стирки х/б тканей имеет щелочную среду, для стирки шерстяных и шелковых тканей – имеет нейтральную среду.
Напишите наблюдения, сделайте вывод.
Опыт №2. Влияние растворов мыла и синтетических моющих средств на ионы
кальция и магния.
В одну пробирку прилить немного раствора мыла, в две другие – по несколько капель разных моющих средств в жидком состоянии по–отдельности. В каждую пробирку добавить по несколько капель хлорида кальция. Этот опыт повторить с хлоридом магния.. Наблюдать выпадение белого осадка в одной из пробирок. Сделать вывод, почему так произошло.
Опыт №3. Влияние растворов мыла и синтетических моющих средств на твердые
и жидкие жиры.
В одну пробирку прилить немного раствора мыла, в две другие – по несколько капель разных моющих средств в жидком состоянии по–отдельности. В каждую пробирку прилить немного растительного масла и наблюдать, какие изменения и в какой пробирке могут быть. Этот опыт повторить с небольшим кусочком твердого жира.
Сравнить результаты, сделать вывод.
Опыт №4. Получение нерастворимого в воде медного мыла.
В одну пробирку прилить немного раствора мыла, в две другие – по несколько капель разных моющих средств в жидком состоянии по–отдельности. В каждую пробирку добавить немного раствора медного купороса.
Записать свои наблюдения, написать реакцию, сделать вывод.
Опыт №5. Получение нерастворимого в воде свинцового мыла.
В одну пробирку прилить немного раствора мыла, в две другие – по несколько капель разных моющих средств в жидком состоянии по–отдельности.
В каждую пробирку добавить немного уксуснокислого свинца.
Записать свои наблюдения, написать реакцию, сделать вывод.
Контрольные вопросы:
1. Что называется твердым мылом, жидким мылом?
2. Почему при стирке белья в жесткой воде расход мыла значительно возрастает
по сравнению с мягкой водой?
3. Почему синтетические моющие средства дают обильную пену в жесткой воде?
4. Что необходимо использовать для получения мыла?
Практическая работа №4
«Кислородсодержащие углеводороды».
Решение экспериментальных задач.
Цель работы: 1. Закрепить знания о кислородсодержащих углеводородах с помощью
решения экспериментальных задач.
Задание.
1. При пропускании хлороводорода через метиловый спирт образуется галогено–производное метана. Составьте уравнение реакции и назовите это вещество.
2. Получите хлорэтан из этилового спирта. Как еще можно получить хлорэтан?
Составьте уравнения реакций.
3. Назовите металл, с которым спирты будут реагировать энергичнее, чем с натрием.
Составьте уравнения реакций.
4. Какой максимальный объем водорода может быть вытеснен натрием из 230 г этилового спирта.?
5. Напишите уравнения реакций, при помощи которых можно получить метанол из метана и бутанол – 1 из бутана.
6. Объясните, как химическим способом можно отличить глицерин от этилового спирта.
Составьте уравнения реакций для получения фенола из бензола для химической
цепочки: С6Н6 --------С6Н5Cl -––––– С6Н5ОН
7. Напишите формулы 3–метилбутаналя и 4–метил, 3–этилпентаналя.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




