ЭКГ 15,10,2007 Умеренная синусовая брадикардия. Синусовый ритм с ЧСС 58-61, отклонение ЭОС влево. Единичная желудочковая экстрасистола. Изменения в миокарде заднедиафрагмальной, боковых отделах ЛЖ.
ЭхоКардиография 18,10,2007. Заключение: стенки аорты утолщены, створки АК и МК неравномерно утолщены, кальцинированы. Межпредсердная перегородка неравномерно утолщена с участками кальциноза (больше в верней части). Размеры полостей – правого желудочка верхняя граница нормы Гипертрофия миокарда ЛЖ. Дилатация ЛЖ, ЛП, восходящего отдела аорты. Регургитация на МК 1 с. Диастолическая функция нарушенна по 1 типу. Сократительная функция ЛЖ сохранена.
Данные МРТ и других параклинических исследований – без особенностей.
В результате этих дополнительных исследований диагноз «Транзиторная ишемическая атака в вертебрально-базиллярном бассейне артерий при артериальной гипертензии» был переписан как «Транзиторная ишемическая атака в вертебрально-базиллярном бассейне артерий по кардиогенному подтипу (СубТИА2) при артериальной гипертензии» [5]. Согласно которому и было назначено соответствующее лечение. Пациент в удовлетворительном состоянии был выписан домой под дальнейшее наблюдение невропатолога по месту жительства.
Следует заметить, что вопрос выбора наиболее информативного набора признаков-предикторов с максимальным дифференциально-диагностическим потенциалом был и пока остается еще далеким от окончательного решения. Чтобы нейросетевой классификатор эффективно работал, ему необходимо предоставить такой предварительно составленный набор наиболее информативных признаков-предикторов для осуществления дифференциально-диагностической прогнозной классификации.
В нашем представлении такую предподготовку лучше всего поручить генетическому алгоритму (ГА). Возможность и целесообразность применения ГА с этой целью также нами апробирована [19, 20]. Пример решения задачи отбора признаков-предикторов с максимально выраженным информационным дифференциально-диагностическим потенциалом с применением ГА приведен на рис. 1.
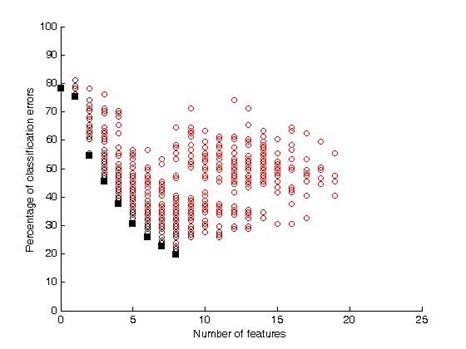
Рис. 1. Горизонтальная ось определяет количество принятых в рассмотрение признаков-предикторов, вертикальная – ошибку последующей классификации (распознавания) подтипов ТИА по АНК.
В ходе работы ГА (в данном случае это бикретериальная постановка задачи) происходит поиск решений оптимизационной задачи по двум противоречащим друг другу критериям: 1) точность распознавания и 2) выбор малозатратных по стоимости их получения признаков-предикторов, т. е. предполагается одновременная максимизация значения первого критерия и минимизация значения второго критерия. [19, 20].
В результате работы ГА из 41 признака в качестве наиболее эффективных (позволяющих сформировать классификатор с достаточно приемлемой точностью диагностики подтипов ТИА) признаков-предикторов определены восемь: зрительные расстройства (OPDISODS), снижение памяти (MEMORYLO), возраст начала курения (SMOKAGE), снижение трудоспособности (LABEFFEC), бессонница (INSOMNIA), боли области сердца (HEARTACH), характер головных болей (HEADACHE) изменения на ЭКГ (ECG). Они ранжированы по весовым коэффициентам их дифференциально-диагностического потенциала, таблица 2.
Таблица 2.
Признаки-предикторы и их дифференциально-диагностические весовые коэффициенты
Признак | OPDISODS | MEMORYLO | SMOKAGE | LABEFFEC |
Весовой коэффициент | 9.3 | 8.3 | 5.8 | 5.4 |
Признак | INSOMNIA | HEARTACH | HEADACHE | ECG |
Весовой коэффициент | 4.8 | 4.6 | 4.6 | 1.8 |
Эти признаки-предикторы в классификационном дифференциально-диагностическом ансамбле ГА+АНК обеспечили суммарную точность классификации 80,2% таблица 3 [19].
Таблица 3.
Сопоставление точности распознания по технологиям АНК и ГА
Тип классификтора | Точность классификации (%) |
Только АНК | 77,2 |
Ансамблирование ГА+АНК | 80.2 |
Место генетического алгоритма и адаптивного нейросетевого классификатора в прогнозной диагностике подтипов ТИА
Таким образом, выкристаллизовывается целесообразность построения (ассемблирования) инструментального ансамбля из генетического алгоритма и адаптивного нейросетевого классификатора. Схематически место этого ансамбля в общей схеме решения дифференциально-диагностических задач приведено на рис. 2.


![]()
![]()



Рис. 2. Блок-схема решения распознавательно-диагностической задачи совместной работой ГА и АНК.
Выбор информативных признаков-предикторов автоматически осуществляет ГА (этап предподготовки) с последующим решением диагностической (распознавательной) задачи по алгоритму работы АНК. Верхние два блока схемы – область преимущественно обычной традиционной рутинной работы врача. Нижние блоки – предлагаемый нами формально-логический компонент общей схемы, выполненный в программном исполнении для компьютера.
Наши представления о подтипах транзиторных ишемических атак
Наши представления о ТИА с годами формировались под влиянием теории распознавания образов, нечеткой формальной логики, теории множеств с нечеткими границами («пушистые множества», fuzzy sets) [4-6, 11, 18-20, 44].
Интуитивно-клинически в математической трактовке подтипы ТИА как варианты цереброваскулярной патологии – это непересекающиеся множества с четкими границами и четким отграничением друг от друга (это желаемое, так хотелось, чтобы так было). В реальных же условиях – фактически, наоборот – границы между нозологиями нечеткие, расплывчатые, что, впрочем, и обусловливает необходимость в проведении дифференциальной диагностики. Подтипы ТИА, по нашему мнению, в этом аспекте скорее «пушистые множества», «множества с нечеткими границами», “fazzy sets”. Поэтому в наших исследованиях мы пользуемся понятием «подтип ТИА», а не «вариант ТИА». Так, этиопатогенетически гемодинамически значимые атероматозные изменения стенок кровеносных сосудов, кардиоэмболия и артериальная гипертензия «беспроблемно уживаются» друг с другом и могут сосуществовать в клинической картине одного пациента, но одно из этих проявлений, как правило, лидирует.
С подобной проблемой нередко приходится сталкиваться и при тестировании, когда из трех-четырех вариантов ответа на вопрос правильными могут быть два или даже все варианты.
Такую ситуацию можно смоделировать на конкретном примере, если необходимо ответить на вопрос, какой фактор риска определяет возникновение эпизода ТИА:
1) Атеросклеротические изменения стенки сосудов?
2) Нарушение сердечной деятельности (мерцательная аритмия)?
3) Артериальная гипертензия?
4) Экстравазальное стенозирование сосуда?
На клинико-интуитивном уровне понятно, что все эти факторы риска в той или иной степени могут быть и предпосылкой и причиной ТИА. Формально-логически, по своей симптоматике в соответствующем признаковом пространстве – это пересекающиеся множества. Положительная корреляция между нозологией ТИА и каждым из этих факторов не вызывает сомнения. Можно удовлетвориться этой констатацией. Но это мало что дает для проведения конкретных целенаправленных превентивных профилактических мероприятий. И совершенно ничего не дает для их унификации и стандартизации. Каждый врач волен по-своему характеризовать эти факторы и истолковывать их приоритетность, и исходя из своих личных представлений и предпочтений, назначать лечебно-профилактические мероприятия.
Уповать только на достигнутые результаты доказательной медицины не достаточно. Выводы из них не дают основы для получения этиотропного эффекта у каждого пациента с цереброваскулярной патологией. «Разговоры о доказательной медицине во многом спекулятивны, так как каждый пациент болеет и поправляется сугубо индивидуально» [27].
Даже самые современные руководства не содержат всех ответов на практические вопросы, которые возникают у врача при лечении ишемических поражений мозга. «К сожалению, стройные представления о механизмах ишемической гибели участка мозговой ткани, процессах эксайтотоксичности и индукции апоптоза не отражают полностью событий, происходящих в мозге» [17].
Наш опыт позволяет нам конкретизировать представления о нозологической единице ТИА. В нашем представлении, ТИА – это гетерогенная нозологическая единица, включающая в себя несколько подтипов, что предопределяет неоднозначный подход в проведении дифференцированных лечебно-профилактических мероприятий по их предотвращению. Аналогичное мнение высказывают J. Tejada et al. (2002). Мы полностью разделяем мнение авторов в том, что ТИА, с учетом сходства их клинической картины с развитием инфаркта мозга, должны классифицироваться по этиологическому принципу: атеротромбоз, кардиоэмболия, лакунарный инфаркт мозга, необычное течение и этиология не определена [44]. Этиопатогенетическая сложность происхождения подтипов ТИА, с учетом вовлеченности различных систем организма в патологический процесс, формально-математически может быть представлена как пересекающиеся, и, в то же время, достаточно обособленные множества, существующие в соответствующем признаковом пространстве.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



