3.Определяем валентность металла: В=![]() =
=![]() =1,96 ≈ 2
=1,96 ≈ 2
4.Определяем точную атомную массу: А=В·Э=2·43,8=87,6г/моль
Определение относительной молекулярной массы
газообразных веществ
Отношение молекулярной массы вещества к 1/12 части массы изотопа 12С называется относительной молекулярной массой вещества (Мr).
Относительная молекулярная масса веществ равна сумме относительных атомных масс атомов, составляющих вещество. Например: Мr(Al2(SО4)3) =27 · 2+ (32+16· 4)·3 = 342 г/моль
Для определения относительной молекулярной массы газа применяют закон Авогадро или законы идеальных газов Менделеева-Клайперона: PV=nRT
Итальянский ученый Амедео Авогадро (в1811) предложил такой закон: В равных объемах различных газов при одинаковых условиях (Р, Т) содержится одинаковое число молекул.
Из закона Авогадро вытекает два следствия:
1)1моль вещества при нормальных условиях (Т=0оС, Р=760мм. рт. ст.) равна 22,4 л.
2) Объем 1 моля газа, хотя и одинаковы (при одинаковых условиях), но молекулярные массы у них различны.
По следствиям закона Авогадро можно определить относительные молекулярные массы газов. Если даны одинаковые объемы двух различных газов, число молекул которых в единице объема обозначим через n, тогда масса газов в единице объема равняется: m =n·M m1=n·M1
Отношение масса газов с одинаковым объемом равна:
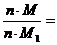
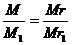
Отношение массы газа к массе другого газа, которые имеют одинаковые объемы, при одинаковых условиях называется плотностью первого газа ко второму и обозначается буквой D. В этом случае уравнение принимает такой вид: D=![]()
Если плотность газов определяется по отношению к воздуху или водороду, то используем такое уравнение: Dвозд.=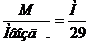 DН2=
DН2=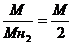
Этим способом молекулярные массы газов определяются только при нормальных условиях (Р=760 мм. рт. ст. ё 101,3кПа, Т=273К или t=0оС). Если молекулярная масса газа определяется при других условиях, то используют уравнение Менделеева-Клайперона: PV= nRT
Здесь Р-давление газа, V-объем газа, n=![]() -число молей газа, R- универсальная газовая постоянная равная 8,314 Дж/моль·К, Т-температура (273К).
-число молей газа, R- универсальная газовая постоянная равная 8,314 Дж/моль·К, Т-температура (273К).
Практическая часть
Прибор, посуда и реактивы. Штатив, 2 стакана объемом 500 мл и 200 мл, термометр, металл, спиртовка.
Опыт 1. Определение атомного веса металла по его удельной теплоемкости. В стакан объемом 500 мл налейте 250 мл воды и нагрейте. Взвешенный металл с точностью до 0,1 гр (m1) завяжите ниткой и опустите в кипящую воду. Держите так 10-15 минут. В это время в стакан объемом 200-250 мл налейте 100мл холодной воды и измерьте ее температуру (t1).
Нагретый металл до 1000С переместите в холодную воду. Помешивая, термометром измерьте повышенную температуру и запишите (t2). Температура кипящей воды 1000С. Следующими формулами определите атомную массу металла:
С mн2о (t2-t1) = mмет (t3-t2).
![]()
![]() ;
; ![]() ; А = Э ·В
; А = Э ·В
Опыт 2. Определение молекулярной массы углекислого газа. Двуокись углерода, полученная в аппарате Киппа действием 3н. или 10%-ного раствора соляной кислоты на мрамор, освобождается от хлороводорода в первой склянке, заполненной до половины раствором NaHCO3 и высушиваем концентрированной H2SO4.
Чистую и сухую колбу плотно закройте резиновой пробкой. Колбу с пробкой взвесьте на технохимических весах с точностью до 0.01г. Массу колбы (m1) запишите. Наполните колбу двуокисью углерода. Для этого опустите в колбу до дна газоотводную трубку и пропускайте двуокись углерода из аппарата Киппа в течение 3-4 минут. Затем, не закрывая кран, осторожно выньте стеклянную трубку и закройте колбу пробкой. После этого закройте кран аппарата Киппа. Взвесьте колбу с двуокисью углерода на технохимических весах с точностью до 0.01г (m2).
Повторите опыт с заполнением колбы двуокисью углерода и снова взвесьте. Масса (m3) должна отличаться от (m2) не более чем на ±0.01г. Если разница в массе превышает эту величину, заполните колбу в третий раз и снова взвесьте. Запишите температуру и атмосферное давление по барометру. Измерьте объем колбы, наполнив её водой до метки. Воду из колбы вылейте в мерный цилиндр. Объем воды равен объему двуокиси углерода V. Запишите эту величину.
Масса колбы с воздухом и пробкой | Масса колбы с СО2 и пробкой | Объем колбы в мл | Температура 0С | Давление (р) мм. рт. сб. |
b1 | b2=b3 |
Для определения молекулярной массы углекислого газа, необходимо знать массу СО2 в колбе. Для этого необходимо знать массу колбы без воздуха. Так как до реакции колба содержала воздух, поэтому массу воздуха определим по его объему. Для этого объем воздуха в колбе переведём в нормальные условия, так как масса 1 литра воздуха равна 1,293 гр, поэтому используем уравнение Бойл-Мариота и Гей-Люссака:
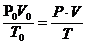 отсюда
отсюда ![]()
Составим пропорцию: 1л возд - 1,293 г
V0 - с
Найдите массу воздуха (с), а теперь найдите массу колбы (d) по разности (b1-c) d=b1-c. Масса углекислого газа (m) равняется разности b3- d. Теперь по объему грамм-молекул газов рассчитайте молекулярную массу углекислого газа. Для этого используйте следующую пропорцию:
г-МСО2 - 22,4л
m - V0 отсюда г-МСО2 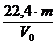 М(СО2)=?
М(СО2)=?
Молекулярную массу углекислого газа можно также определить по отношению к воздуху:
D=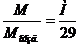 и М=29·Dвозд.
и М=29·Dвозд.
Напишите реакцию, происходящую в аппарате Киппа.
Упражнение
1.Удельная теплоемкость металла равна 0,13Дж/г. град. Вычислите атомную массу металла.
2.40,12 гр металла замещает 0,3872 гр водорода. Удельная теплоемкость металла равна 0,13Дж/г. град. Вычислите валентность и относительную атомную массу металла.
3.Оксид металла содержит 31,58% кислорода. Удельная теплоемкость металла равна 0,51Дж/г. град. Вычислите относительную атомную массу металла.
4.Масса 1л газа при 210С и давлении 96,23кПа равна 2,52 гр Вычислите относительную молекулярную массу газа и его плотность по отношению к водороду.
5.Масса 1л газа при нормальных условиях равна 1,43. Вычислите мольную массу газа и его плотность по отношению к водороду и к воздуху.
ЛАБОРАТОРНАЯ РАБОТА №4
Комплексные соединения
Строение молекул комплексных соединений выражается на основе координационной теории. Молекула комплексных соединений состоит из внутренней и внешней сферы, которые отделяются друг от друга квадратными скобками:
[Cu(NH3)4]SO4, K[BF4]
Внутренняя сфера комплекса состоит из центрального атома или иона называемым комплексообразователем, а также из противоположно заряженных ионов или нейтральных молекул, называемыми лигандами. Число лигандов выражает координационное число комплексообразователя. Внешнюю сферу составляют противоположно заряженные ионы. Комплексообразователем может быть металл или неметалл. Его степень окисления определяется по сумме зарядов лигандов и ионов внешней сферы. Комплексные соединения образуют донорно-акцепторную связь. Например, в комплексном соединении [Ag(NH3)2]Cl степень окисления иона Ag+ (+1), а координационное число равно 2.
Большее число комплексных соединений образуют элементы побочных подгрупп (в основном d - и f-металлы). Комплексные соединения, как и другие химические соединения, имеют способность вступать в реакцию обмена и окислительно-восстановительные, а также диссоциировать в водных растворах.
Электролитическая диссоциация комплексных соединений проходит по следующим ступеням: а) на комплексный ион и ион внешней сферы б)диссоциация комплексного иона в) диссоциация лигандов.
Электролитическая диссоциация большинства комплексных ионов является обратимым процессом и подчиняется закону действия масс и количественно равна константе диссоциации.
Например: [Ag(NH3)2]+→ Ag++2NH3
К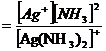
Так как константа диссоциации показывает устойчивость комплексного иона, поэтому её называют константой неустойчивости комплексного иона.
Практическая часть
Прибор, посуда и химические реактивы. 2-х молярный раствор хлорида аммония, щелочь калия, сульфат железа (II), гексацианоферрат калия, сульфат аммония, йодид калия, сульфид аммония, пробирка.
Опыт 1. В пробирку налейте немного раствора соли хрома (III), 2-3 капли раствора аммиака. В начале образуется осадок, который растворяется в избытке аммиака. Напишите уравнение реакции.
Опыт 2.Налейте пробирку 2-3 мл раствора соли цинка и прилейте 3 капли раствора K4[Fe(CN)6] и нагрейте до кипения. В результате образуется белый осадок K2Zn3[Fe(CN)6]2. Напишите уравнение реакции.
Опыт 3. В пробирку налейте 1-2 мл раствора соли алюминия и прилейте немного раствора щелочи. Образуется белый осадок. В полученный осадок прилейте избыток раствора щелочи. Напишите молекулярную и ионную реакцию.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |




