Опыт 4. Налейте в пробирку 1-2 мл раствора K4[Fe(CN)6] и прилейте 1-2 мл раствора сульфата меди. Какой осадок образуется. Напишите молекулярную и ионную реакцию.
Опыт 5. Налейте в пробирку 1 мл раствора Pb(NO3)2 и прилейте 1 мл раствора KJ. Часть осадка перелейте в другую пробирку и опять добавьте раствор KJ. Осадок растворится. Напишите уравнение реакции.
Опыт 6. В пробирку, содержащую раствор AgNO3 прилейте немного раствора KOH. К полученному осадку до полного растворения прилейте раствор NH4OH. Напишите уравнение реакции.
Опыт 7. В пробирку, содержащую раствор CuSO4 прилейте раствор (NH4)2S. Укажите цвет осадка. Напишите молекулярную и ионную реакцию
Опыт 9. В пробирку, содержащую раствор соли железа (III), прилейте немного раствор K4[Fe(CN)6]. Наблюдайте образование осадка берлинской лазури.
Опыт 10. Поместите несколько крупинок соли кобальта и несколько крупинок тиосульфата натрия в фарфоровую ступку. Растирая получившуюся смесь, заметьте появление синего комплексного соединения. Составьте уравнение реакции.
Упражнение
1.Назовите приведенные комплексные соединения:
А) К[AuBr4] В)[Сr(NH3)4(H2O)2]Br3 Д)[Ag(NH3)2]Cl
Б)Cu2[Fe(CN)6] Г)Na[Pt(NH3)Cl5]
2.Определите степень окисления и координационное число комплексных соединений:
a)[Cd(NH3)4]Cl2 г)[Сu(CN)4]SO4 в)[Сr(H2O)5Cl]Cl2
б)K2[HgI4] д)Na[Co(CN)4(H2O)2]
3. Напишите реакцию между Сu(NО3)2 и К4[Fe(CN)6], которая протекает с образованием Cu2[Fe(CN)6]. Напишите молекулярную и ионную реакцию процесса.
4.Для осаждения ионов Cl - из0,25 мл 0,1М раствора [Сr(H2O)5 Cl]Cl2, сколько миллилитров 0,1н раствора AgNО3 необходимо.
ЛАБОРАТОРНАЯ РАБОТА №5
Скорость химических реакций
Скорость химических реакций определяется изменением концентрации реагирующих веществ в промежутке времени. Концентрация-количество вещества, которое содержится в определенном объеме и массе исследуемой системы:
![]()
Среднюю скорость химических реакций можно определить по следующей формуле:
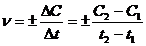
С1-концентрация вещества до реакции, С2-концентрация вещества после реакции, t-время.
Скорость химических реакций зависит от многих факторов, в том числе: природы реагирующих веществ, концентрации веществ, температуры и присутствия катализатора. Зависимость скорости химических реакций от концентрации веществ выражается законом действия масс, который выражается так:
Скорость химических реакций при постоянной температуре прямо пропорциональна произведению концентрации реагирующих веществ.
Эта зависимость действует для реакций, протекающих в гомогенных системах. Например, для реакции nA+mB=C закон действия масс выражается так: V=k[A]n·[B]m здесь - скорость реакции, К-коэффициент пропорциональности или константа скорости реакции. Величина К зависит только от температуры и природы реагирующих веществ. [A], [B] – молярная концентрация реагирующих веществ, n и m – коэффициенты.
Задача. Получение NH3 из N2 и H2 выражается так: N2 + 3H2 =2NH3 , Если в два раза увеличить концентрацию водорода, во сколько раз изменится скорость реакции.
Решение: Если обозначить [N2] = a, [H2]=b, то скорость реакции можно выразить так:
V1=К[a]·[b]3 =Кab3
После изменения концентрации водорода: V2=К[a] ·[2b]3 =8Кab3
Отсюда 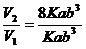 = 8
= 8
Скорость реакции увеличивается в 8 раз. В гетерогенных системах скорость реакций зависит от концентрации газообразных веществ или жидкости, также от площади поверхности фаз.
Влияние температуры на скорость химических реакций. Повышение температуры влияет на скорость реакций согласно закону Вант-Гоффа, которое выражается так: При повышении температуры на каждые 100С скорость реакции увеличивается в 2-4 раза:
Vt2=Vt1 · ![]()
Vt1- скорость реакции при температуре t1, Vt2- скорость реакции при температуре t2, γ- температурный коэффициент реакции.
Задача. При повышении температуры от 300С до 900С во сколько раз увеличится скорость реакции, если температурный коэффициент равен двум.
Решение: 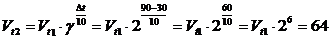
Скорость реакции увеличится в 64 раз.
Практическая часть
Прибор, посуда и химические реактивы. Штатив, пробирки, стакан объемом 250-400мл, 3 бюретки, термометр, секундомер, измерительный цилиндр.
Опыт 1. Зависимость скорости реакции от концентрации. Скорость реакции взаимодействия серной кислоты и тиосульфата натрия зависит от их концентрации. Реакция протекает по следующей схеме: Na2S2O3+H2SO4=H2S2O3+Na2SO4
H2S2O3=H2O+SO2+↓S
В результате образования свободной серы раствор мутнеет. Установите в штативе три бюретки. В первую налейте раствор тиосульфата натрия, во вторую воду, а в третью раствор кислоты. Согласно таблице проведите опыты. Каждый раз засекайте время секундомером и засекайте время помутнения раствора.
№ | Объем раствора мл | Время секунда | Концентрация a+b | Скорость реакции V=⅟t | ||
Na2S2O3 (а) | H2O (b) | H2SO4 (с) | ||||
1 | 6 | 0 | 6 | 1 | ||
2 | 4 | 2 | 6 | 2/3 | ||
3 | 3 | 3 | 6 | ½ | ||
4 | 2 | 2 | 2 | 1/3 |
Зависимость скорости реакции от концентрации изобразите виде графика.
Опыт 2. Зависимость скорости реакции от температуры. В 4 пробирки налейте из бюретки по 4 мл раствора тиосульфата натрия и в другие 4 пробирки по 4 мл налейте раствор кислоты. Первые пробирки тиосульфата и кислоты поместите в стакан с водой и измерьте температуру. После этого одну пробирку налейте в другую и засекайте время появления помутнения. Вторые две пробирки поместите в стакан с водой и повысьте температуру на 100 выше. Также прилейте одну пробирку в другую и засекайте время появления помутнения. Этот опыт проведите со всеми пробирками. Результаты опытов укажите в виде таблицы.
Номер пробирки | Температура опыта | Время реакции t1 | Скорость реакции V=⅟t |
1 | |||
2 | |||
3 | |||
4 |
Опыт 3. Скорость реакции в гетерогенных системах. В две пробирки по 20 мл на ¼ налейте раствор соляной кислоты (10%) . Возьмите два одинаковых кусочка мрамора (0,5г). Один целиком поместите в первую пробирку, а вторую измельчите и поместите во вторую пробирку. С помощью секундомера определите время прохождения реакции. Рассчитайте среднюю скорость реакции в обоих случаях. В какой пробирке реакция протекает быстрее. Напишите уравнение реакции.
Упражнение
1.Напишите математическое выражение приведенных реакций:
2Н2+О2→2Н2О
CuО+ Н2→ Cu+ Н2О
2 NО+О2→2NО2
2.Константа скорости реакции J2+ Н2→2НJ при 500С равна 0,16. Вычислите скорость реакции при следующих концентрациях: [J2 ]=0,03 моль/л и [Н2 ]=0,04 моль/л.
3.Уравнение окисления аммиака выражается так: 4NН3+ 5О2→4NО+6Н2О. Через определенный промежуток времени концентрация веществ стало [NН3]=0,01 моль/л, [О2]=0,02 моль/л, [NО]=0,03 моль/л. Вычислите начальную концентрацию аммиака и кислорода.
4. Во сколько раз увеличится скорость реакции при повышении температуры от 700С до 1200С, если температурный коэффициент равен двум.
5.При повышении температуры на 400С, скорость реакции повышается в 16 раз. Вычислите температурный коэффициент реакции.
ЛАБОРАТОРНАЯ РАБОТА №6
Приготовление растворов
Концентрация растворов обычно определяется по количеству или массе растворенного вещества. Для приготовления растворов необходимо знать способы выражения состава растворов. Для выражения состава растворов используют такие способы: процентная концентрация, молярная концентрация, нормальная концентрация и т. д. Состав растворов можно определять по их плотности. Плотность раствора зависит от концентрации раствора, т. е. с изменением концентрации, изменяется также плотность раствора (p![]() ).
).
Процентная концентрация. Показывает отношение массы растворенного вещества к общей массе раствора. Масса раствора равняется сумме массе растворенного вещества и массе растворителя: m раств= m1+ m2
m1- масса растворенного вещества, m2- масса раствора. Процентную концентрацию раствора определяют по формуле: С%![]() ·100%.
·100%.
Если, известны плотность и объем раствора, то формула процентной концентрации принимает вид:
С%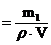 ·100% p
·100% p![]() отсюда m= pV
отсюда m= pV
Задача 1. Найдите процентную концентрацию раствора, который образуется при смешивании 15 гр NaCl и 65 гр воды.
Решение: m раств= m1+ m2= 15+65=80г
Масса раствора равна 80г тогда С%![]() =17,64%
=17,64%
Образуется 17,65% раствор.
Задача 2. Рассчитайте массу КОН который необходимо для приготовления 300 мл 20%-ного раствора (p=1,18 г/мл).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |




