Приборы, превращающие энергию химической реакции в электрическую называются гальваническими элементами. Для изучения и составления гальванического элемента необходимо знать значение электродного потенциала металлов. Величина потенциала, образующегося между металлической пластинкой и раствором электролита, называется электродным потенциалом.
Так как непосредственно определить разность потенциалов между металлической пластинкой и электролитом невозможно, поэтому в практике используют относительные электродные потенциалы.
Относительные электродные потенциалы металлов определяются по отношению водородному электроду, потенциал которого условно принята ноль, называется стандартным электродным потенциалом металла (Е0).
Если расположить металлы в ряд по увеличению значения стандартного электродного потенциала, то получим ряд напряжений металлов.
СТАНДАРТНЫЙ ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ
НЕКОТОРЫХ МЕТАЛЛОВ, E0
Электрод | E°,B | Электрод | E0, B |
Li+ /Li | -3,045 | Ni2+ /Ni | -0,25 |
К+ /К | -2,924 | Sn2+ /Sn | -0,136 |
Ва2+ /Ва | -2,90 | Pb2+/Pb | -0,127 |
Са2+ /Са | -2,87 | Fe3+/Fe | -0,037 |
Na+ /Na | -2,714 | 2H+ /H2 | 0,000 |
Mg2+ /Mg | -2,37 | Sb3+ /Sb | +0,20 |
AL3+/Al | -1,70 | Bi 3+ /Bi | +0,215 |
Ti2+ /Ti | -1,603 | Cu 2+ / Cu | +0,34 |
Mn2+/Mn | -1,18 | Cu+ /Cu | +0,52 |
Cr2+ /Cr | -0,913 | Hg22+/Hg | +0,79 |
Zn2+ /Zn | -0,763 | Ag+ /Ag | +0,80 |
Cr3+ /Cr | -0,74 | Hg2+ /Hg | +0,85 |
Fe2+ /Fe | -0,44 | Pt2+ / Pt | +1,19 |
Cd2+/Cd | -0,403 | Au3+ / Au | +1,50 |
Co2+ /Co | -0,277 | Au+ /Au | +1,70 |
С увеличением значения электродного потенциала металлов, уменьшается восстановительная способность этих металлов, окислительная способность увеличивается. То есть металл с меньшим значением электродного потенциала может вытеснять из растворов солей металл имеющий большее значение электродного потенциала. Например: Fe + CuSO4 →FeSO4 +Cu
В электрохимии на катоде протекает восстановление катионов, а на аноде протекает окисление анионов или анода. Во время работы гальванического элемента функцию анода выполняет металлическая пластинка с большим значением потенциала. Например: Ni/NiSO4/CuSO4/Cu
На катоде (-) Ni-2e-=Ni2+ (окисление)
На аноде (+) Сu2+ +2e-= Cu0 (восстановление)
Разность потенциалов металлов называется электродвижущей силой (ЭДС). При расчете ЭДС обычно от большего значения отнимают меньшее значение:
ЭДС=Е0Cu-Е0Ni =+ 0,34-(-0,25) = 0,59В.
Величина электродного потенциала зависит не только от металла, но и от среды и концентрации его ионов в растворе. Эту зависимость выражают с помощью уравнения Нернста:
Е= Е0 + ![]() · lgC
· lgC
Здесь: Е –потенциал металла в растворе
Е0- стандартный электродный потенциал металла
n – заряд иона металла
С – концентрация ионов металла в растворе соли (г·ион/л)
Если на систему, состоящую из двух электродов помещенных в раствор, пропустить постоянный электрический ток, то на электродах проходит окислительно-восстановительные реакции. Если через раствор или расплав электролита пропустить постоянный электрический ток, то отрицательно заряженные ионы перемещаются к положительному электроду (анод), а положительно заряженные ионы перемещаются к отрицательно заряженному электроду (катод). На аноде (+) восстановитель, отдавая электрон окисляется, на катоде (-) окислитель, принимая электрон восстанавливается.
Окислительно-восстановительные реакции, протекающие под воздействием постоянного электрического тока, называется электролизом.
Электролиз растворов протекает более сложно, чем электролиз расплава, потому, что в растворе кроме тонов электрода также присутствуют ионы воды Н+ и ОН-. Поэтому электролиз растворов электролитов протекает согласно следующим правилам:
1.Если катион металла расположен в ряду напряжений металлов до алюминия, то на катоде восстанавливаются катионы водорода.
2.Если катион металла расположен между алюминием и водородом, то на катоде восстанавливаются и катионы металла, и ионы водорода.
3.Если катион металла расположен после водорода, то на катоде восстанавливаются только эти катионы.
4.Если анион без кислорода, то на аноде окисляются эти анионы.
5.Если анион кислородсодержащий, то на аноде окисляется ионы гидроксила (ОН-) и выделяется кислород: 4ОН - -4е - =2Н2О +О2 . Среда раствора будет кислой.
Приведенные правила действуют только для нерастворимых (инертно-графитовых, платиновых) анодов. Если анод изготовлен из растворимого металла, то при электролизе анод растворяется, и концентрация электролита не изменяется. Например: а)Напишите электролиз растворов Cu(NO3)2 и BaCl2 с нерастворимым анодом.
1) Cu(NO3)2
катод К(-) анод А (+)
Cu2+ +2е-=Cu0 NO3-
Н+ 4ОН - -4е- =2Н2О +О2
В растворе: Н+ + NO3- = НNO3
2) BaCl2
катод К(-) анод А (+)
Ba2+ Cl - - е- =Cl0
Н+ +е-=Н Cl0+ Cl0= Cl2
Н+Н=Н2 ОН-
В растворе: Ba2+ + 2ОН-= Ва(ОН)2
б) электролиз раствора CuSO4 с растворимым анодом (медный)
CuSO4
катод К(-) анод А (+)
Cu2+ +2е-=Cu0 Cu0 -2е-=Cu2+
Количество вещества, выделяющегося на электродах, зависит от количества электричества прошедшего через раствор или расплав электролита. Эта зависимость выражается законами Фарадея. Согласно которым:
1.Масса веществ, образующихся на электродах, прямо пропорциональна количеству электричество прошедшего через раствор электролита. Математически это можно выразить так:
Q=I·t
Q - количество электричества (Кл), I - сила тока (А), t - время (секунда).
2.При образовании один эквивалент любого вещества на электродах, затрачивается одинаковое количество электричества (96500 Кл). Математически это можно выразить так:
m![]()
m-масса вещества, Э - эквивалентная масса вещества, I - сила тока, t - время.
Если полученное вещество находится в газообразном состоянии, то уравнение принимает вид:
V![]()
V - объем полученного газа, ЭV –эквивалентный объем газа.
Задача 1. При пропускании электрического тока силой 4А через раствор AgNO3, в течении 20 минут, сколько граммов серебра выделиться на катоде? Решение:
m![]()
Задача 2. При пропускании электрического тока силой 2А через раствор NaCl, в течении 10 мин, сколько литров кислорода выделиться (н. у.) на аноде? Решение:
V02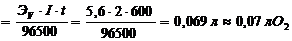
Практическая часть
Прибор, посуда и химические реактивы. Графитовые и медные электроды, провода, 1М раствор серной кислоты, раствор хлорида меди, йодид калия, карбонат натрия, раствор крахмала, источник постоянного тока, медная и цинковая пластинки, раствор соли цинка, гальванометр.
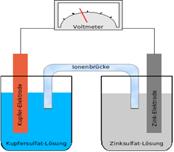
Опыт 1. Гальванический элемент. Налейте в отдельные стаканы 1М растворы соли меди и цинка. В стакан с раствором соли меди опустите медную пластинку, а в стакан с раствором соли цинка опустите цинковую пластинку. С помощью проводов присоедините измерительный прибор, а стаканы соедините с помощью U-образной трубки, который заполнен раствором, какого либо электролита. Рассчитай теоретическое значение ЭДС. Напишите процессы, происходящие на электродах.
Опыт 2. Электролиз раствора серной кислоты с медным анодом. Закрепите в штатив U-образную трубку и налейте раствор 1М-ной серной кислоты. Опустите графитовые и медные электроды в кислоту. Медный электрод присоедините к положительному полюсу, а графитовый к отрицательному полюсу и присоедините к источнику постоянного электрического тока. На катоде сначала выделяются пузырьки водорода, а после выделения водорода прекращается и электрод покрывается медью.
Опыт 3. Электролиз раствора хлорида меди. В U-образную трубку налейте 0,5 молярный раствор хлорида меди. Опустите графитовые электроды и пропустите постоянный электрический ток в течении 5-10 минут. После отсоедините от источника тока и наблюдайте поверхность катода. Какое вещество выделилось на катоде? В той части трубки, где расположен анод, прилейте несколько капель раствора крахмала. Что наблюдается? Напишите схему электролиза происходящие на электродах.
Опыт 4. Электролиз раствора йодида калия. В U-образную трубку налейте 0,5 молярный раствор йодида калия и несколько капель раствора фенолфталеина. Опустите с двух сторон графитовые электроды и пропустите постоянный электрический ток в течение 5-10 минут. Наблюдайте у катода выделения газа и появления фиолетового окраса. С той стороны трубки, где расположен анод, налейте в отдельную пробирку немного раствора и разбавьте водой. После добавьте несколько капель раствора крахмала. Что наблюдаете? Напишите схему электролиза и уравнение реакций происходящих на электродах.
Опыт 5. Коррозия металлов. Очищенную медную пластинку нагрейте на пламени спиртовки. Что наблюдаете? В чем суть этого процесса? Напишите уравнение реакции. После нагрейте железную пластинку (лезвие) и сразу поместите в стакан с холодной водой. Что наблюдается? Напишите уравнение реакции. Что общего между этими опытами? Какая из реакций является процессом коррозии? Назовите основные ее признаки.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |




