Решение: С%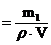 ·100%
·100%
m1=С· p·V= 20· 1,18 ·300 =70,8г КОН
Молярная концентрация. Показывает количество грамм-молекул растворенного вещества в одном литре раствора и обозначается См. Например, 2М (молярный) раствор показывает, что в одном литре раствора содержится две моли вещества. Его выражают в виде формулы:
СМ![]()
Здесь: СМ-молярная концентрация, m-масса растворенного вещества, М-мольная масса вещества, V-объем раствора.
Задача. Рассчитайте массу хлорида натрия, которое необходимо для приготовления 500 мл 0,2М раствора.
Решение: М(NaCl)=58,5 г/м
СМ![]() m
m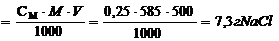
Нормальная концентрация. Показывает число грамм-эквивалентов растворенного вещества в одном литре раствора. Например, 2н раствор серной кислоты показывает, что в одном литре раствора растворено два грамм-эквивалента ил и98 грамм серной кислоты. Нормальную концентрацию выражают следующей формулой:
Сн![]()
здесь: Э - эквивалентная масса растворенного вещества, m - масса растворенного вещества, V-объем раствора.
Задача. Найдите нормальную концентрацию раствора в 200 мл которого растворено 3,92 гр серной кислоты.
Решение: Mr(H2SO4) =98 г/м ЭH2SO4 =49 г/м
Сн![]()
![]() =0,4 н
=0,4 н
Практическая часть
Опыт 1. Приготовление раствора определенной процентной концентрации.
Для приготовления определенного количества раствора заданной концентрации, нужно определить массу растворенного вещества и растворителя. Если растворяемое вещество имеет высокую концентрации, то по его плотности можно определить его массу. Количество воды можно измерить с помощью измерительной посуды (мензурка, цилиндр).
Количество растворяемого вещества с помощью воронки добавьте в посуду содержащего растворитель и перемешайте стеклянной палочкой до полного растворения. Определите плотность полученного раствора с помощью ареометра.
Правильность проделанной работы можно определить по значению плотности, рассчитав теоретически.
Опыт 2. Приготовление 200 гр 15%-ного раствора NaCl, NaOH, Na2CO3, CuSO4.
Вначале рассчитайте массы веществ, необходимые для приготовления раствора. Взвесьте их на техно-химических весах с точностью 0,01 гр. После этого навеску поместите в колбу содержащую небольшое количество воды и растворите. Потом прилейте остальную воду и ареометром измерьте плотность полученного раствора.
Опыт 3. Приготовление раствора с известной молярной концентрацией.
Для приготовления определенного объема раствора с известной молярной концентрацией, вначале нужно рассчитать массу растворенного вещества. Определенную массу вещества поместите в колбу и растворите в небольшом количестве воды до полного растворения. Объем доведите до одного литра.
Опыт 3. Приготовление 250 мл 0,5М раствора CuSO4·5H2O.
Вначале определите массу CuSO4·5H2O, необходимую для приготовления данного раствора с точностью до 0,01гр в технохимических весах, и поместите в измерительную колбу, растворив в небольшом количестве воды. Затем долейте воду до определенного объема. Измерьте плотность полученного раствора с помощью ареометра.
Опыт 4. Приготовление раствора с определенной нормальной концентрацией.
При приготовлении раствора необходимо вычислить грамм-эквивалент растворяемого вещества, растворить его в небольшом количестве воды и довести объем до одного литра.
Опыт 5. Приготовление 250 мл 1н раствора серной кислоты.
Рассчитайте массу серной кислоты необходимую для приготовления 250 мл 1н-ного раствора. С помощью ареометра определите плотность кислоты, которая находится в лаборатории. В зависимости от плотности найдите по таблице процентную концентрацию кислоты.
Определите объем кислоты и воды, необходимых для приготовления раствора. Необходимый объем кислоты возьмите в цилиндр. Определенный объем воды налейте в колбу и прилейте кислоту, небольшими частями постоянно помешивая. С помощью ареометра определите плотность полученного раствора. Сравните процентную концентрацию приготовленного раствора и теоретически рассчитанного.
ЛАБОРАТОРНАЯ РАБОТА №7
Ионное произведение воды. Гидролиз солей
Вода очень слабый электролит, но в небольших количествах подвергается диссоциации, которая протекает по схеме: Н2О=Н++ОН-
Этот процесс является обратимым и между молекулами воды и ионами устанавливается равновесие. Согласно закону действия масс константу диссоциацию воды можно записать так:
Кдисс.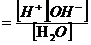 или Кдисс. ·[Н2О] =[Н+]·[ОН-]
или Кдисс. ·[Н2О] =[Н+]·[ОН-]
Степень диссоциации воды имеет очень маленькое значение, поэтому концентрацию недиссоциированных молекул воды принимают как постоянное значение и выражают так:
Кдисс.·[Н2О]=КН2О тогда Кдисс.·[Н2О]=КН2О
КН2О –называется ионным произведением воды. Значение КН2О при 220С равна 1· 10-14 г·ион/л.
В воде концентрация ионов Н+ и ОН - равна [Н+]=[ОН-]=1· 10-7 г·ион/л.
Если концентрация ионов воды равны, то среда раствора нейтральна. Обычно среду раствора определяют в зависимости от концентрации ионов водорода:
При кислой среде [Н+]>10-7 и [ОН-]<10 -7
При нейтральной среде [Н+]=10-7 ва [ОН-]=10 -7
При щелочной среде [Н+]<10-7 [ОН-]>10 -7
Чтобы избавиться от отрицательного значения концентрации ионов водорода [Н+], используют отрицательное значение десятичного логарифма величины [Н+], которое называется водородным показателем и обозначается рН: рН=- lg[Н+] = - lg1·10-7=7
если рН=7 среда нейтральная,
рН <7 среда кислая
рН > 7 среда щелочная
Если известна концентрация ионов Н+ , то можно определить концентрацию ионов ОН - и рН.
Пример. Концентрация ионов водорода равна [Н+]=10-5 моль/л. Вычислите концентрацию ионов ОН - и рН раствора.
Решение: 1) [Н+]·[ОН-]=1· 10-7 мол/л
[ОН-]=1· 10-14/10-5 =10-9 мол/л [ОН-]=10-9 мол/л
2) рН=-lg[Н+]= - lg10-5=5
Задача. Вычислите рН 0,0365 % - ного раствора НCl, плотность которого равна p=1,0 г/л.
Решение:а)Масса 1л раствора равна:
p![]() , p=V·p=1000·1=1000г
, p=V·p=1000·1=1000г
б)масса НCl в 1000г раствора
1000г - 100% Х![]() =0,365г
=0,365г
Хг - 0,0365%
с) СМ![]() =1·10-2
=1·10-2
Соляная кислота НCl одноосновная кислота, поэтому ее водный раствор имеет концентрацию ионов водорода [Н+]=10-2моль/л
д) рН=-lg [Н+]= - lg (10-2)=2
В промышленности используют в основном водные растворы веществ, определение рН которых является главной задачей. Для определения рН растворов можно применять индикаторы.
Индикаторы такие органические вещества, которые в зависимости от среды раствора могут изменить свой цвет.
Иногда при растворении веществ между растворителем и растворяемым веществом протекает химическая реакция. Такие реакции называются сольволизом (если растворителем является вода, то процесс называется гидролизом).
Многие химические соединения, как соли, белки, эфиры, жиры могут подвергаться гидролизу. В неорганической химии изучение гидролиза солей имеет особое значение.
Реакции между ионами соли и воды, в результате которого составные части воды меняются с составными частями соли, называется гидролизом.
В результате гидролиза солей происходит смещение равновесия электролитической диссоциации воды. Поэтому среда растворов большинства водных растворов солей может быть или кислотной или щелочной.
В зависимости от химического состава и условий образования солей гидролиз протекает четырьмя способами:
1.Гидролиз солей образованных от сильного основания и слабой кислоты (K2S, NaCN, K2CO3).
NaCN + Н2О = НCN + NaОН
Na++CN - +НОН = НCN+ Na+ + ОН-
CN - +НОН = НCN + ОН-
Процесс гидролиза протекает до восстановления равновесия. В результате гидролиза этой соли образуется малодиссоциируюшаяся соль НCN, то есть в растворе уменьшается концентрация ионов Н+. В результате концентрация ионов ОН - увеличится, то есть среда раствора становится щелочной, потому, что NaОН сильное основание.
2.Гидролиз солей образованных от слабого основания и сильной кислоты (NH4Cl, Al(NO3)3, Fe2(SO4)3).
NH4Cl+Н2О= NH4ОН + HCl
NH4 + +Cl - + Н2О = NH4ОН + H++Cl-
NH4 + + Н2О = NH4ОН + H+
В результате гидролиза таких солей образуется слабое основание и сильная кислота в результате, которого увеличивается концентрация ионов Н+. Среда таких растворов кислая.
3.Гидролиз солей образованных от слабого основания и слабой кислоты (CH3-COONH4, Fe(CN)3, ZnS).
CH3-COONH4 + Н2О = CH3-COOН +NH4ОН
При гидролизе таких солей среда раствора зависит от степени диссоциации основания и кислоты и среда может быть слабокислой, слабощелочной, но чаще бывает нейтральной. Гидролиз таких солей протекает до конца: Al2S3 + 6H2O→Al(OH)3↓+3H2S
4.Гидролиз солей образованных от сильного основания и сильной кислоты (NaCl, KNO3, Na2SO4).Такие соли гидролизу не подвергаются. Среда таких растворов всегда нейтральна (рН=7), потому, что при взаимодействии с водой не образуется слабый электролит.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |




