Задание №8. Пользуясь таблицей растворимости, напишите уравнения диссоциации следующих соединений:
КOH →
Н3РО4 ↔
Cr2(SO4)3 ↔
Решение.
калий гидроксида: КOH → К+ + ОН¯
ортофосфорной кислоты: Н3РО4 ↔ 3Н+ + РО43-
хром (III) сульфата: Cr2(SO4)3 →2Сr3++3SO42-
Задание №9. Закончить уравнения реакций и назвать продукты:
а) 2NH3 + H2SO4 ® б) N2O5 + CaO ® в) AlCl3 +3AgNO3®
Решение.
а) 2NH3 + H2SO4 ® (NH4 )2SO4 б) N2O5 + CaO ®Ca(NO3)2
аммоний сульфат кальций нитрат
в) AlCl3 +3AgNO3 ® Al(NO3)3 + 3AgCl;
алюминий нитрат хлорид серебра (I)
Задание №10. Закончите уравнение реакций и назовите полученные продукты. AgNO3 + KI ® ……….. Напишите полное ионное уравнение.
Решение. Закончим уравнение: AgNO3 + KI ® AgI↓ + KNO3;
Назовём полученные продукты. AgI – иодид серебра(I)
KNO3 – нитрат калия.
Напишем в полной ионной форме
Ag+ + NO3- + K+ + I - ® AgI↓ + K+ + NO3-;
Задание №11. Охарактеризуйте реакцию, используя все классификации: 2Na + 2Н2O → 2NaOH + Н2 + Q
Решение. Реакция замещения, окислительно-восстановительная, экзотермическая, необратимая (выделяется газ), некаталитическая, гетерогенная (твердое вещество + жидкость).
Задание №12. Составьте ионные уравнения реакций, соответствующих схемам превращений. Дайте названия исходных и конечных продуктов.
Са ® СаО ® Са(ОН)2 ® CaCO3
Решение. Пронумеруем цепочку и назовем соединения:
1 2 3
Са ® СаО ® Са(ОН)2 ® CaCO3
кальций кальций кальций кальций
оксид гидроксид карбонат
1. 2Са + О2 = 2СаО
2. СаО + Н2О = Са(ОН)2
вода
3. Са(ОН)2 + CО2 = CaCО3 + Н2О
углекислый газ
Задание №13. Расставить коэффициенты методом электронного баланса в уравнении окислительно-восстановительной реакции. Указать окислитель и восстановитель: KMnO4 + HCl ® KCl + MnCl2 + Cl2 + H2O.
Решение. Для подбора коэффициентов методом электронного баланса составляют схему реакции, определяют элементы, изменившие степень окисления, и составляют отдельные схемы электронного баланса для процессов окисления и восстановления. Те наименьшие числа, на которые необходимо умножить обе схемы, чтобы уравнять число отданных и присоединенных электронов, и будут коэффициентами при окислителе и восстановителе.
Определим степени окисления элементов
K+Mn+7O-24 + H+Cl - ® K+Cl - + Mn+2Cl-2 + Cl02 + H+2O-2.
Составим уравнения электронного баланса по элементам, которые изменили свою степень окисления.
 2Cl - - 2ē → Cl02 5 восстановитель; процесс окисления
2Cl - - 2ē → Cl02 5 восстановитель; процесс окисления
Mn+7+ 5ē → Mn+2 2 окислитель; процесс восстановления
2KMnO4 + 16HCl ® 2KCl + 2MnCl2 + 5Cl2 + 8H2O.
Mg + H2SO4(конц.) ® MgSO4 + H2S + H2O;
0 +1 +6 -2 +2 +6 -2 +1 -2 +1 -2
![]() Mg + H2SO4(конц.) ® MgSO4 + H2S + H2O;
Mg + H2SO4(конц.) ® MgSO4 + H2S + H2O;
S+6+8ē→S-2 1 окислитель; процесс восстановления
Mg0―2ē → Mg+2 4 восстановитель; процесс окисления
.4Mg + 5H2SO4(конц.) ® 4MgSO4 + H2S + 4H2O
KMnO4 + NaNO2 + H2O ® MnO2 + NaNO3 + KOH.
+ +7 -2 + +3 -2 + -2 +4 -2 + +5 -2 + -2 +
б) KMnO4 + NaNO2 + H2O ® MnO2 + NaNO3 + KOH.
![]() Mn+7+3ē→Mn+4 2 окислитель; процесс восстановления
Mn+7+3ē→Mn+4 2 окислитель; процесс восстановления
N+5―2ē → N+3 3 восстановитель; процесс окисления
.2KMnO4 + 3NaNO2 + H2O ® 2MnO2 + 3NaNO3 + 2KOH.
Задание №14. Напишите структурные формулы следующих соединений:
а) 2-метилбутена-2; б) 5-этилгептена-2;
Решение: структурные формулы следующих соединений:
СН3
│
а) 2-метилбутен-2 Н3С─СН═С─СН3;
б) 5-этилгептен-2 С2Н5
│
Н3С─СН═СН─СН2─СН─СН2─СН3;
Задание №15. Для Cu(OH)2 дано количество 5 моль. Найти массу и число частиц
Решение: В химических расчетах используется единица количества вещества – моль. Один моль любого вещества содержит число Авогадро (NA=6,02×1023) частиц, из которых оно состоит. Масса одного моль вещества называется молярной массой (М)
1. Найдём массу m=n·M = 5 · 98 = 490 г, где М(Cu(OH)2) = 98г/моль.
2. найдём число частиц N = n·NА = 5·6,02·1023 =30,1·1023 частиц
Задание №16. Для NH3 дан объём 44,8 л Найти число моль, массу и число частиц
Решение:
1. найдём молярную массу NH3 М = 14 + 3 = 17 г/моль и массу m=n·M = 2 · 17 = 34 г
2. найдём число моль n = V/·Vm = 44,8/22.4= 2 моль
3. найдём число частиц N = n·NА = 2 · 6,02·1023 =12,04·1023 частиц
Задание №17. Вычислить массовые доли каждого из элементов, входящих в состав углеводорода, формула которого C6H12.
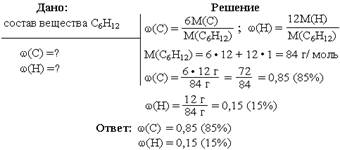
Задание №18. Какой объем метана (н. у.) выделится при взаимодействии 10 г карбида алюминия (Al4C3) с 10 г воды?
Решение:
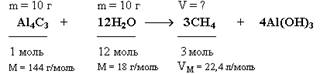
Находим количества вступивших в реакцию веществ:
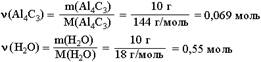
Так как на 1 моль Al4C3 требуется в 12 раз большее количество вещества воды, то на 0,069 моль Al4C3 необходимо 0,828 моль воды. Следовательно, 0,55 моль воды недостаточно для реакции с 0,069 моль Al4C3, который взят в избытке и прореагирует неполностью.
Определим ν(CH4) по веществу, взятому в недостатке:
ν(CH4)= 12∙0,55/3 = 0,137 моль
Рассчитаем объем метана, образовавшегося в реакции:
V(CH4) = ν(CH4) • Vm = 0,137 моль • 22,4 л/моль = 3,07 л
Ответ: V(CH4) = 3,07 л
Задание №19. Рассчитайте количество теплоты, выделившейся при сгорании 0,25 моль метана, используя термохимическое уравнение реакции горения метана:СН4 + 2О2 = СО2 + 2Н2О + 890 кДж
Решение:
![]()
При сгорании 1 моль CH4 выделяется 890 кДж. Следовательно, количество теплоты, выделяемое при сгорании 0,25 моль метана, будет равно:
Q = 0,25 моль · 890 кДж/1 моль = 223 кДж.
Ответ: Q = 223 кДж
Задание №20. Какой объём 50%-ного раствора КOH плотностью 1,538 г/см3 потребуется для приготовления 3 л 6%-ного раствора плотностью 1,048 г/см3?
Решение:
1. Найдём массу 6% раствора. m=ρ*V=1.048* 3000= 3144 г
2. Найдём массу КОН.
m(KOH) = m(р-ра)*ω = 3144*0,06=188,64г.
3. Найдём массу 50% раствора.
m(50%р-ра) = 188,64/0,5=377,28г.
4. Найдём объем 50% раствора: V= m/ρ = 377,28/1,538= 245,3 мл.
Ответ: 245,3 мл.
Задание №21. Из 700 г 60%-ной серной кислоты выпариванием удалили 200 г воды. Чему равна массовая доля оставшегося раствора?
Решение:
1. Найдем массу вещества в растворе: m = ω·m = 0,6·700= 420
2. Найдем массу нового раствора: m = 700-200=500
3. Найдем массовую долю оставшегося раствора ω = 420/500 =0,84 или 84%
Ответ: 44%
Задание №22. При электролизе раствора СuСl2 на аноде выделилось 560 мл газа (н. у.). Найдите массу меди, выделившейся на катоде.
Решение: X 0,56 л
CuCl2 → Cu + Cl2
64 г/моль 22,4 л/моль
Х = 1,6 г Cu.
Ответ: на катоде выделилось 1,6 г Cu.
Задача №23. Имеется смесь фенола с этанолом. К одной половине смеси добавили избыток металлического натрия, получив водород объёмом 672 мл (н. у.). К другой половине смеси добавили избыток раствора брома, при этом образовался осадок массой 6,62 г. Определите массовые доли фенола и этанола в смеси.
Решение:
1.Смесь фенола С6Н5Он и этанола С2Н5Он реагирует с металлическим натрием по уравнениям, и выделяется 0,672/22,4 = 0,03моль Н2:
0,02моль 0,01моль
I) 2 С6Н5Он + 2Na →2С6Н5ОNa + н2
2моль 1моль
0,04моль 0,02
II) 2 С2Н5Он + 2Na →2С2Н5ОNa + н2
2моль 1моль
2. С избытком брома реагирует только фенол:
III) С6Н5Он + 3Br2 →С6Н2 Br3ОН↓ + 3нBr
1моль 1моль
3. Найдем хмическое количество и массу фенола по уравнению III:
n(С6Н2Br3ОН)= n(С6Н5Он) = m(С6Н2 Br3ОН)/M(С6Н2 Br3ОН) = 6,62/331=0,02моль;
m(С6Н5Он) = M(С6Н5Он) * n(С6Н5Он ) = 94*0,02=1,88г
4.Если в реакцию I вступает 0,02 моль фенола, то выделяется 0,01моль Н2.
Значит, на в реакции с этанолом выделится 0,03 – 0,01 = 0,02мольН2.
5.Найдем массу этанола в смеси:
m(С2Н5Он) = M(С2Н5Он) * n(С2Н5Он )= 46*0,02*2= 1,84г
6. Определим массовые доли фенола и этанола в смеси:
m(смеси) = 1,88+1,84 = 3,72г
ω(С2Н5Он) = 1,84 * 100%/3,72 =49,46%
ω(С6Н5Он) = 1,88 * 100%/3,72 = 50,54%
Ответ: ω(С2Н5Он) = 49,46%; ω(С6Н5Он) = 50,54%
Задача №24. При полном каталитическом разложении при нагревании смеси KClO3 и KMnO4 массой 56,1 г получено 8,96 дм3(н. у.) кислорода. Определить массовую долю (%) солей в смеси.
Решение. Пусть в смеси х моль KMnO4 и у моль KClO3.
Составим уравнения реакций:
у моль 1,5у моль
2KClO3→2KCl + 3O2
122,5г/моль
хмоль 0,5х моль
2KMnO4 →2K2MnO4 + MnO2 + О2
158г/моль
Найдём химическое количество О2 :
n(O2)=V(О2)/Vm = 8,96/22,4= 0,4моль.
Составим систему уравнений.
158х + 122,5у = 56,1
0,5х + 1,5у = 0,4
получаем: х = 0,2моль или 0,2∙158 = 31,6г KMnO4;
ω(KMnO4) = 31,6/51,6 = 0,563
у = 0,2моль или 0,2∙122,5 = 24,5г KClO3
ω(KClO3) = 24,5/51,6 = 0,437
Ответ: ω(KMnO4) = 56,3%, ω(KClO3) = 43,7%
Задача №25. Вычислите массовую долю хлорида меди (II) в растворе, если известно, что при добавлении к 150 г этого раствора избытка раствора сульфида натрия образовалось 4,78 г осадка. Сколько молей растворенного вещества содержалось в 150 г раствора сульфата меди (П)?
Решение. Реакция взаимодействия солей СuCl2 и Na2S в растворе идет с образованием осадка сульфида меди CuS:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



