2. репаративная органическая химия. М.: Мир, 2004. – 704 с.
3. Органикум: в 2-х т. М.: Мир, 1992. т. 1 – 487 с., т. 2 – 472 с.
4. еханизмы реакций в органической химии. М.: Химия, 1991. – 447 с.
5. рганическая химия. М.: Химия, 1979. – 832 с.
6. , Куплетская УФ-, ИК-, ЯМР - и масс-спектроскопии в органической химии. М.: МГУ, 1979. – 240 с.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ПЕРВОЙ КОНТРОЛЬНОЙ РАБОТЕ
Выполнение контрольной работы № 1 требует от студента теоретической подготовки в вопросах классификации органических соединений по функциональным группам, изомерии, заместительной и радикально-функциональной номенклатуры, электронного строения химических связей атома углерода, электронных и пространственных эффектов в органических молекулах, стереоизомерии, классификации реакций и реагентов (присоединение, замещение, отщепление, перегруппировки; радикальные, электрофильные, нуклеофильные), механизмов реакций, кислотных и основных свойств органических соединений, а также строения, способов получения и химических свойств углеводородов.
Определение принадлежности соединений к определенным классам органических соединений
Функциональная группа и строение углеродного скелета являются основными классификационными признаками органических соединений. При отнесении соединений к определенным классам органических соединений следует руководствоваться следующей схемой:
Пример 1. Мезатон
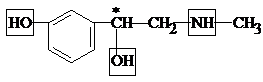 |
Молекула мезатона содержит фенольный гидроксил, вторичный спиртовый гидроксил, вторичную аминогруппу. Следовательно, его можно отнести к следующим классам соединений: фенолы, вторичные спирты, вторичные амины. Молекула содержит один асимметрический атом углерода (отмечен звездочкой).
Пример 2. Аспирин (ацетилсалициловая кислота)
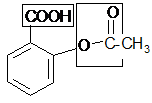
Молекула аспирина содержит карбоксильную и сложноэфирную группы. Следовательно, его можно отнести к следующим классам соединений: ароматическим карбоновым кислотам, сложным эфирам уксусной кислоты.
Химическая связь
Этот раздел курса предусматривает изучение типов химических связей в органических молекулах, видов гибридизации атомных орбиталей углерода, их пространственное расположение в зависимости от вида гибридизации, ковалентных d - и p-связей, электронного строения двойной и тройной углерод-углеродных связей и их основных характеристик (длины, энергии, полярности, поляризуемости).
Подробное изложение материала по данной контрольной работе см. в рекомендуемых учебниках и учебно-методическом пособии «Номенклатура органических соединений. Теоретические основы органической химии».
МЕТОДИЧЕСКИЕ УКАЗАНИЯ КО ВТОРОЙ КОНТРОЛЬНОЙ РАБОТЕ
Вторая контрольная работа включает важнейшие классы гомо - и гетерофункциональных органических соединений. Вопросы составлены с учетом электронных представлений в органической химии и физико-химических методов установления строения органических соединений.
Для успешного выполнения заданий второй контрольной работы необходимо освоить материал по номенклатуре, строению, способам получения и химическим свойствам классов органических соединений. Данный материал изложен в рекомендуемой литературе.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ТРЕТЬЕЙ КОНРОЛЬНОЙ РАБОТЕ
Третья контрольная работа включает материал по углеводам, нуклеиновым кислотам, гетероциклическим соединениям, алкалоидам, липидам, качественным реакциям на функциональные группы и их спектральным характеристикам.
Углеводы.
Моносахариды могут существовать как в открытой (оксоформе), так и в циклических формах. В растворе эти изомерные формы находятся в динамическом равновесии (таутомерии). Оксоформа моносахаридов изображается с помощью формул Фишера, циклические – с помощью формул Колли-Толленса и Хеуорса. Циклические формы моносахаридов образуются в результате взаимодействия карбонильной группы молекулы с гидроксильной группой при пятом или четвертом по счету углеродах от карбонильной. В зависимости от этого образуются соответственно шестичленные (пиранозные) или пятичленные (фуранозные) циклы. В процессе циклизации из углерода карбонильной группы образуется хиральный центр – атом углерода, с которым связана полуацетальная гидроксильная группа. Этот атом называют аномерным, а два соответствующих стереоизомера - α- и β-аномерами. У α-аномера конфигурация аномерного центра одинакова с конфигурацией нижнего хирального центра молекулы, определяющего принадлежность к D- или L-ряду, а у β-аномера – противоположна.
При переходе от формулы Колли-Толленса к формуле Хеуорса заместители, находящиеся справа от углеродной цепи, располагают под плоскостью цикла, т. е. внизу, а заместители, расположенные слева, - над плоскостью, т. е. вверху. У альдогексоз D-ряда в пиранозной форме (и у альдопентоз D-ряда в фуранозной форме) СН2ОН-группа всегда располагается над плоскостью цикла, что служит формальным признаком принадлежности к D-ряду.
Таутомерные формы моносахаридов с помощью формул Фишера, Колли-Толленса и Хеуорзса предлагается изобразить по следующей схеме:
δ-

D-глюкоза α-D-глюкопираноза β-D-глюкопираноза ф-лы Хеуорса
ф-ла Фишера ф-лы Колли-Толленса (пиранозный цикл)
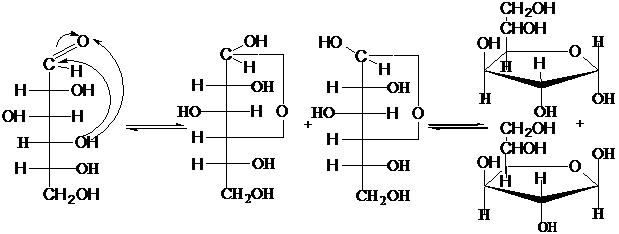
D-глюкоза α-D-глюкофураноза β-D-глюкофураноза ф-лы Хеуорса
ф-ла Фишера ф-лы Колли-Толленса (фуранозный цикл)
Идентификация органических соединений
Большинство органических веществ представляют собой соединения углерода с водородом, кислородом, азотом, серой или галогенами. Все эти элементы могут быть определены с помощью качественного анализа. Для более детального качественного анализа определяют функциональную принадлежность органических соединений и на функциональные группы проводят качественные реакции. Результатом качественных реакций является изменение цвета, появление осадка, выделение газообразных продуктов.
На функциональные группы необходимо привести следующие качественные реакции:
®Фенольный гидроксил: комплексообразование с хлоридом железа, окисления (индофеноловая проба), с реактивом Марки (формальдегид с конц. серной кислотой), бромной водой, азосочетания с солями диазония.
®Спиртовый гидроксил: образование сложных эфиров, окисление первичных и вторичных спиртов бихроматом калия в сернокислой среде, пробу Лукаса (с хлоридом цинка в хлороводородной кислоте) и образование комплексных соединений с сульфатом меди в щелочной среде для многоатомных спиртов.
®Карбоксильная группа: реакция на лакмус, реакция натриевых или аммониевых солей кислот с растворами солей Ag, Pb, Co, Cu, Fe и реакция этерификации.
®Первичная ароматическая аминогруппа: образование азокрасителей, оснований Шиффа с п-диметиламинобензальдегидом в кислой среде, изонитрильную пробу, бромирование бензольного кольца, пробу Гинсбурга (взаимодействие с бензолсульфохлоридом).
®Первичная и вторичная алифатические аминогруппы: с азотистой кислотой, с хлороформом в щелочной среде, образование азометинов, пробу Гинсбурга (взаимодействие с бензолсульфохлоридом).
®Карбонильная группа: с 2,4-динитрофенилгидразином, гидросульфитом натрия, аммиачным раствором оксида серебра (проба Толленса), раствором Фелинга, реактивом Несслера (раствор тетрайодмеркурата калия в щелочи), йодоформную реакцию на метилкетоны.
®Кратные связи: с бромной водой, окисление перманганатом калия в нейтральной или щелочной среде (реакция Вагнера), образование ацетиленида серебра (определение концевой тройной связи).
®Галогены: восстановление галогенопроизводных этилатом натрия с последующим осаждением образующегося галогенид-иона нитратом серебра, пробу Бельштейна.
®Тиольная группа: образование нерастворимых солей меркаптидов металлов (с нитратом или ацетатом свинца), с ферроцианидом калия Fе4[Fе(СN)6]3 в щелочной среде, с нитропруссидом натрия Nа2[Fe(CN)5NO] в насыщенном растворе бикарбоната натрия.
®Сульфоновая группа: образование солей с тяжелыми металлами (Со, Zn, Ва), с аминами (п-толуидином), сплавление сульфокислот со щелочами.
®Амидная и сложноэфирная группы: гидроксамовая проба, кислотный или щелочной гидролиз амидов карбоновых кислот и сложных эфиров и идент®Нитрогруппа: взаимодействие со щелочью, азотистой кислотой, восстановление до аминогруппы и идентификация аминопроизводных соответствующими методами.
®Простые эфиры: расщепление йодистоводородной кислотой и идентификация образующихся продуктов расщепления соответствующими методами.
При выполнении заданий по данной теме необходимо привести уравнения указанных качественных реакций.
КОНТРОЛЬНАЯ РАБОТА № 1
Тема 1: Теория строения . Органическая химия как базовая дисциплина в системе фармацевтического образования. Номенклатура полифункциональных соединений.
1. Дайте определение органической химии. Сформулируйте основные положения теории химического строения . Напишите структурные формулы следующих соединений: а) N-(n-гидроксифенил)амида уксусной кислоты б) кетона, содержащего главную цепь из 8 атомов углерода, двойную и тройную связи, амино-, гидрокси-, винильную группы. Укажите, к каким классам соединений они относятся, обозначьте асимметрические атомы углерода. Соединение «б» назовите по международной номенклатуре.
2. Укажите значение органической химии в системе фармацевтического образования. Рассмотрите классификацию органических соединений по природе функциональной группы. Напишите структурные формулы следующих соединений: а) этилового эфира 3-амино-2-гидрокси-4-пентеновой кислоты, б) альдегида, содержащего главную цепь из 8 атомов углерода, двойную и тройную связи, амино-, нитро-, метильную группы и атом галогена. Укажите, к каким классам соединений они относятся, обозначьте асимметрические атомы углерода. Соединение «б» назовите по международной номенклатуре.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




