Число всех молекул газа
![]() (3)
(3)
где NA - постоянная Авогадро, ν - количество вещества.
Если учесть, что количество вещества ![]()
где m - масса газа, μ - молярная масса газа, то формула (3) примет вид
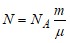
Подставив полученное выражение в формулу (2), имеем
![]() (4)
(4)
Произведем вычисления, учитывая, что для кислорода μ=32⋅10-3кг/моль
![]()
Ек=6.02⋅1023⋅(4⋅10-3/32⋅10-3)⋅4.83⋅10-21 Дж=364 Дж
Пример 11. Кислород массой 2 кг занимает объем 1 м3 и находится под давлением 0.2 Мпа. Газ был нагрет сначала при постоянном давлении до объема 3 м3, а затем при постоянном объеме до давления 0.5 МПа. Найти изменение ΔV внутренней энергии газа, совершенную им работу А и теплоту Q, переданную газу. Построить график процесса.
Решение. Изменение внутренней энергии газа
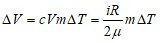 (1)
(1)
где i - число степеней свободы молекул газа (для двухатомных молекул кислорода i=5), ΔТ=Т3-Т1 - разность температур газа в конечном (третьем) и начальном состояниях.
Начальную и конечную температуру газа найдем из уравнения Менделеева-Клапейрона: ![]() , откуда
, откуда ![]() .
.
Работа расширения газа при постоянном давлении выражается формулой
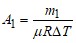
Работа газа, нагреваемого при постоянном объеме равна нулю:
А2 = 0
Следовательно, полная работа, совершаемая газом
А=А1+А2=А1
Согласно первому началу термодинамики, теплота, переданная газу, равна сумме изменения внутренней энергии ΔV и работы А:
Q = ΔV + A
Произведем вычисления, учитывая, что для кислорода μ=32⋅10-3кг/моль:



![]()
A=A1=0.4 МДж
![]()
Q=(3.24+0.4)МДж=3.64МДж
График процесса приведен на рис.4
Рис.4
Пример 12. Объем аргона, находящегося при давлении 80 кПа, увеличился от 1 до 2 л. На сколько изменится внутренняя энергия газа, если расширение производилось: а) изобарно; б) адиабатно?
Решение. Применим первый закон термодинамики. Согласно этому закону, количество теплоты Q, переданное системе, расходуется на увеличение внутренней энергии ДU и на внешнюю механическую работу А:
Q=ДU+A, (1)
где
ДU= ![]()
![]()
![]() CхДT. (2)
CхДT. (2)
Здесь m – масса газа, Cх – молярная изохорная теплоемкость:
Cх= ![]()
![]() R, (3)
R, (3)
где i – число степеней свободы. Тогда выражение (2) примет вид
ДU= ![]()
![]() RДT. (4)
RДT. (4)
Запишем уравнение Клапейрона – Менделеева для начального и конечного состояний газа при изобарном процессе pV1=![]()
![]() RT1 и pV2=
RT1 и pV2=![]()
![]() RT2 или
RT2 или
![]() . (5)
. (5)
Подставив (5) в (4), получим
![]() (6)
(6)
При адиабатном расширении газа теплообмена с внешней средой не происходит, поэтому Q=0. Уравнение (1) запишем в виде
ДU+A=0. (7)
Это соотношение устанавливает, что работа расширения газа может быть произведена только за счет уменьшения внутренней энергии газа (знак минус перед ДU):
А= - ДU. (8)
Работа, совершаемая газом при адиабатном процессе,
![]()
![]()
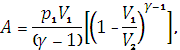 (9)
(9)
где г=Ср/Сх=(i+2)/i – показатель степени адиабаты. Для аргона – одноатомного газа (i=3) – имеем г=1,67.
Найдем изменение внутренней энергии при адиабатном процессе для аргона, учитывая формулы (8) и (9):
![]()
![]() (10)
(10)
Подставляя числовые значения в (6) и (10), получаем:
а) при изобарном расширении
ДU=![]() ·0,8·105 Па·(2·10-3 м3 – 10-3 м3)= 120 Дж;
·0,8·105 Па·(2·10-3 м3 – 10-3 м3)= 120 Дж;
б) при адиабатном расширении
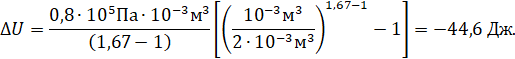
Ответ: а) ДU=120Дж; б) ДU= - 44,6 Дж.
Пример 13. Температура нагревателя тепловой машины 450 К. Температура холодильника 300 К. Определить КПД тепловой машины, работающей по циклу Карно и полную мощность машины, если нагреватель ежесекундно передает ей 1525 Дж теплоты.
Решение. КПД тепловой машины
![]() или
или ![]() (1)
(1)
Из выражения (1) находим 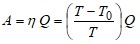
Произведем вычисления:
![]()
А = 0.33⋅1525 Дж = 508 Дж
Эта работа совершается за 1 с, следовательно, полная мощность машины
![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



