В качестве кинетических параметров определялись: начальная скорость реакции, псевдо-константа скорости реакции, порядок реакции. При статистической обработке экспериментальных данных рассчитана относительная погрешность результатов исследований, которая составила 4 % для начальной скорости реакции, 5 % для псевдо-константы скорости реакции.
Процесс окисления диоксанлигнина осуществлялся при непрерывной подаче кислорода через анализируемый раствор и контролировался в течение 6 часов с временным интервалом – 2 часа по изменению массовой доли карбоксильных групп в препарате, которую определяли методом кондуктометрического титрования. По данным статистической обработки экспериментальных результатов исследований абсолютная погрешность определения содержания карбоксильных групп не превышала ± 0,10 масс. %.
Экспериментальная часть
Поиск и характеристика каталитических системна основе марганца (II)
Одним из свойств соединения, предполагаемого на роль катализатора процессов химической переработки лигносодержащего сырья, является его способность избирательно воздействать на лигнинную составляющую. Анализ литературных данных показал, что такими селективными свойствами обладают соединения марганца (II).
С целью выявления наиболее эффективной каталитической системы на основе Mn (II) исследовано влияние концентрации и природы лигандов на кинетику процесса окисления модельных соединений структурного звена лигнина – ванилина, изоэвгенола, феруловой кислоты - растворенным кислородом в щелочных водной и водно-этанольной (содержание этанола – 50 об. %) средах.
Полученные зависимости имеют экстремальный характер (Рис. 1, 2), при этом природа окисляемого вещества и среда, в которой осуществляется процесс каталитического окисления, не влияют на вид данных зависимостей.
|
|
Рисунок 1 – Зависимость псевдо-констан-ты скорости реакции окисления ванилина от концентрации лиганда (L) в водно-этанольно-щелочной среде (содержание спирта – 50 об. %): 1– 1-(2-пиридил-азо)-нафтол-2, 2– изофталевая кислота, 3– 8-оксихинолин, 4– ацетилацетон, 5 –1,10-фенантролин. | Рисунок 2 – Зависимость псевдо-константы скорости реакции окисления фенольных соединений (1 – изоэвгенол, 2,4 – ванилин, 3,5 – феруловая кислота) от концентрации ацетилацетона в водно-щелочной (1,2,3) и этанольно-водно-щелочной (содержание спирта – 50 об.%) (4,5) средах. |
Максимум каталитической активности катализатора наблюдается при соотношении катализатор : лиганд (L) равном 1:1, что соответствует составу каталитически активной формы катализатора – [Mn2+L]. При образовании данного координационно-ненасыщенного комплекса создаются благоприятные условия для вхождения в координационную сферу иона металла молекул окисляемого вещества и кислорода, между которыми в дальнейшем и происходит взаимодействие.
Исследованные лиганды по своей эффективности воздействия на кинетику процесса располагаются в следующий ряд: 1-(2-пиридил-азо)-нафтол-2 < изофталевая кислота ≈ щавелевая кислота < 8-оксихинолин ≈ ацетилацетон < 1,10-фенантролин < дифенилкарбазон < N-фенилантрани-ловая кислота (Табл. 2).
Таблица 2 - Влияние природы органического лиганда в составе
комплекса [Mn2+L] на псевдо-константу скорости реакции окисления ванилина
в этанольно-водно-щелочной (содержание спирта – 50 об. %) среде
Лиганд | kobs∙103, мин-1 |
1-(2-пиридил-азо)-нафтол-2 | 3,60±0,03 |
щавелевая кислота | 3,72±0,05 |
изофталевая кислота | 3,73±0,05 |
8-оксихинолин | 3,76±0,04 |
ацетилацетон | 3,82±0,03 |
1,10-фенантролин | 4,05±0,06 |
дифенилкарбазон | 4,11±0,06 |
N–фенилантраниловая кислота | 4,20±0,04 |
Различие в их действии заключается в отличительной способности данных органических соединений увеличивать эффективный заряд центрального иона за счет образования координационной связи, что приводит к увеличению электрофильности металла и, в свою очередь, способствует ускорению передачи электрона от окисляемого вещества к молекулярному кислороду, в результате чего скорость реакции возрастает (Схема 1).
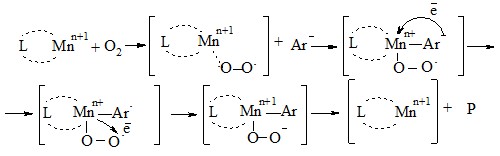
Схема 1–Механизм действия катализатора: L – лиганд, Mnn+ – марганец, Аr– – ионизированная форма окисляемого вещества, Р – продукты реакции окисления.
На основании проведенных исследований разработан и запатентован катализатор окисления (Патент на изобретение № 000) на основе комплексного соединения Mn (II) с органическими соединениями (предпочтительно ацетилацетон, N-фенилантраниловая кислота) состава [Mn2+L].
При исследовании каталитической активности комплексных соединений марганца (II) установлена корреляционная зависимость между наблюдаемым в области 970-1020 нм максимумом поглощения (λmax) в спектрах комплексных ионов [Mn2+L] (Рис. 3), обусловленным d-d-электронным переходом металла-катализатора, и псевдо-константой скорости реакции (Рис. 4):
| (1) |
где а=-2,714, b=-2,816 – параметры, зависящие от химической природы лиганда.
|
|
I | II |
|
|
III | IV |
Рисунок 3 – Спектр комплексов марганца (II) с органическими лигандами: I– с сульфосалициловой кислотой; II– с изофталевой кислотой; III– с ацетилацетоном; IV– с N–фенилантраниловой кислотой: 1– спектр комплекса (с =5∙10-2 моль/л), 2– спектр органического лиганда (с=5∙10-2 моль/л), 3– спектр MnCl2 (с=5∙10-2 моль/л).
Полученная зависимость может быть использована для предварительной оценки каталитической активности комплексных соединений марганца (II) с органическими лигандами в процессах окисления соединений фенольного ряда.
2. Изучение кинетики каталитического окисления родственных лигнину фенольных соединений гваяцильного ряда растворенным кислородом
С целью определения оптимальных условий проведения каталитического процесса; установления основных закономерностей превращений лигнинных веществ в процессе гомогенного каталитического окисления; разработки кинетической модели процесса окисления исследовано влияние рН раствора, концентрации катализатора, окисляемого вещества, окислителя, состава растворителя (концентрации этанола), температуры на кинетику процесса окисления модельных соединений структурного звена лигнина растворенным кислородом в щелочных водной и в водно-этанольной средах.
В качестве объектов исследований использованы ванилин, феруловая кислота и изоэвгенол, моделирующие структурные фрагменты хвойных лигнинов, содержащие различные заместители в пара-положении к фенольному гидроксилу:
| где R – СОН – ванилин; – СН=СН–СООН – феруловая кислота; –СН =СН-СН3 – изоэвгенол |
Катализаторами процесса служили хлорид марганца (II) и полученное на его основе комплексное соединение марганца с ацетилацетоном – [Mn2+Acac].
Результаты исследования влияния рН среды показали, что максимальная скорость реакции достигается при рН раствора близком значению рKа+1, (Ka– константа ионизации окисляемого вещества), что соответствует образованию 99% ионизированной формы фенольного соединения, которая в основном и подвергается окислению (Рис. 5, 6, табл. 3).
В случае присутствия катализатора дальнейшее увеличение рН раствора приводит к избыточному содержанию ОН––ионов, которые в свою очередь взаимодействуют с катализатором с образованием гидроксокомплексов, при этом доля каталитически активной формы катализатора в растворе снижается, что приводит к уменьшению скорости реакции (Рис. 6). Введение органической составляющей в растворитель не влияет на вид зависимостей начальной скорости реакции от рН раствора.
|
|
Рисунок 5 – Зависимость начальной скорости реакции окисления ванилина (А), феруловой кислоты (Б) и изоэвгенола (В) от рН раствора в отсутствие катализатора в водно-щелочной среде при cок. в.=5·10-5моль/л, cкат.= 5·10-6моль/л, I = 0,01 моль/л, Т=298 К. | Рисунок 6 – Зависимость начальной скорости реакции окисления ванилина (А), феруловой кислоты (Б) и изоэвгенола (В) от рН раствора в водно-щелочной среде при cок. в.=5·10-5 моль/л, I=0,01моль/л, Т=298 К в присутствии катализатора: 1– MnCl2, 2– [Mn2+Acac], cкат.= 5·10-6 моль/л. |
Таблица 3 – Начальная скорость окисления фенольных соединений

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |