Исследование влияния состава растворителя на процесс каталитического окисления диоксанлигнина (Рис. 14) указывает на то, что при концентрации спирта 50 об. % наблюдается наибольшее содержание карбоксильных групп, причем введение [Mn2+Acac]-комплекса в реакционную среду интенсифицирует процесс окисления на 100 % по истечении шести часов от начала эксперимента.
На основании приведенных выше экспериментов, можно сделать вывод о том, что при исследовании процесса каталитического окисления нативных препаратов лигнина можно использовать те же подходы, что и при изучении процесса окисления модельных соединений структурного звена лигнина. Использованный [Mn2+Acac] – катализатор проявляет каталитическую активность, как при окислении модельных соединений структурного звена лигнина, так и при окислении диоксанлигнина. Анализ литературных данных и полученные экспериментальные данные позволяют предположить, что механизм каталитического окисления, при этом носит активационный характер, связанный с образованием промежуточного комплекса металл-фенольное соединение-кислород, в котором реализуются взаимная активация, как окисляемого вещества, так и кислорода.
4 Разработка кинетической модели механизма каталитического окисления соединений фенольного ряда растворенным кислородом
Проведенные исследования свидетельствуют о тождественности основных закономерностей и факторов, влияющих на процесс каталитического окисления соединений фенольного ряда и диоксанлигнина, вследствие этого разработана единая кинетическая модель механизма гомогенного каталитического окисления фенольных структур лигнина.
При окислении фенольных соединений растворенным кислородом в отсутствие катализатора полученные экспериментальные данные позволяют представить процесс в виде следующей кинетической схемы:
Kа АrН k1 Аr– + О2 | (2) (3) |
где P1 – продукты окисления.
Применяя к реакции (2) метод квазиравновесных концентраций, получаем следующее выражение для скорости реакции:
| (4) |
где v0(б/к) – начальная скорость реакции окисления фенольных соединений кислородом без катализатора;
Kа – константа равновесия реакции (2);
k1 – константа скорости реакции (3);
[ArH]0 – общая исходная концентрация окисляемого вещества;
[O2] – начальная концентрация кислорода в растворе.
[H+] – начальная концентрация ионов водорода в растворе.
С целью определения значений констант ионизации Kа и скорости реакции окисления k1 с помощью программы Curve Expert 1.3 построены линейные зависимости 1/v0=f([H+]) и определены параметры уравнения, которые позволили рассчитать константы Kа и k1.
Расчетные значения констант ионизации совпадают со значениями Ka, приведенными в литературе и определенными независимыми методами (потенциометрическое, кондуктометрическое, спектрофотометрическое титрование) (Табл. 6). Это является дополнительным подтверждением адекватности кинетической схемы (2)–(3).
Таблица 6 – Значения констант ионизации фенольных соединений Кa и скорости
реакции окисления k1 фенолсодержащих соединений в отсутствии катализатора.
Соединение | k1, М-1∙с-1 | Kа∙109 | pKа | |
I | II | |||
Водно-щелочная среда | ||||
Ванилин | 0,11 | 24,00±0,12 | 7,61 ±0,01 | 7,38±0,05 |
Феруловая кислота | 0,13 | 0,80±0,04 | 9,10±0,02 | 9,31±0,16 |
Изоэвгенол | 0,09 | 0,30±0,02 | 9,52±0,03 | 9,81±0,08 |
Этанольно-водно-щелочная среда (содержание спирта – 50 об. %) | ||||
Ванилин | 0,10 | 2,14±0,11 | 8,67±0,02 | 8,50 |
Феруловая кислота | 0,16 | 0,04±0,01 | 10,40±0,09 | 10,20 |
Примечание: I – рассчитанное по экспериментальным данным значение рKа; II – значение рKа согласно литературным данным /, , //Химия древесины.-1984.-№5.-С. 23-29, , // Химия древесины.-1983.- № 1.- С. 106-112/
В случае окисления фенольных соединений растворенным кислородом в присутствии катализатора было установлено, что основную роль в каталитическом цикле играет ион металла (Mn2+), роль органического лиганда (L) сводится к увеличению активности катализатора и не отражается
на кинетической схеме процесса. Поэтому кинетическая схема в данном случае состоит из уравнений (2)-(3) и уравнений, следующего вида:
KI Mn2+ + O2 k2 Mn2+ O2+ Ar─ KII Mn2+ + ОН─ KIII MnOH+ +ОН─ KIV Mn(OH)2 +Ar─ k3 Mn(OH)2Ar─ +O2 KV MnOH+ + Ar─ k4 Mn(OH)Ar + O2 | (5) (6) (7) (8) (9) (10) (11) (12) |
где Р2, P3, P4 – продукты окисления.
Применяя метод квазистационарных концентраций и предполагая, что [Mn2+]0<<[Ar]0; KI[O2]<<1; KIV·KIII·KII[OH-]2[Ar-]<<1; KV·KII[OH–][Ar–]<<1 получим следующее уравнение для скорости реакции:
| (13) |
где v0(кат) – начальная скорость реакции в присутствии катализатора;
KW –константа ионизации воды, KW =10-14;
KII–константа равновесия реакции (7);
KIII – константа равновесия реакции (8);
kкат = k/кат + k//кат [OH-] + k///кат[OH-]2, где k/кат = k2KI k//кат = k4KVKII k///кат = k3KIVKIIIKII | (14) |
С целью проверки адекватности модели проведена обработка экспериментальных данных в области оптимальных значений рН раствора (рKa …рKa+1), в результате чего получена зависимость (15) и рассчитано значение константы k/кат (Табл. 7).
| (15) |
где ∆v0(кат)= v0(кат)– v0(б/к)
Таблица 7 – Значения константы k/кат, полученные расчетным методом.
Модель | k/кат·10-3 | |
В присутствии MnCl2 | В присутствии [Mn2+Acac] | |
Водно-щелочная среда | ||
Ванилин | 5,44 | 14,50 |
Феруловая кислота | – | 18,90 |
Изоэвгенол | 10,60 | 11,20 |
Этанольно-водно-щелочная среда (содержание спирта – 50 % об.) | ||
Ванилин | 8,25 | 15,70 |
Феруловая кислота | – | 26,70 |
| |
I | II |
Рисунок 14 – Зависимость ∆v0(кат) от концентрации OH–-ионов при окислении ванилина в присутствии MnCl2 в водно-щелочной среде (I), и в этанольно-водно-щелочной среде (содержание спирта – 50 об.%) (II): 1 – кривая, полученная расчетным методом; 2 – кривая, полученная по экспериментальным данным. | |
|
|
I | II |
Рисунок 15 – Зависимость ∆v0(кат) от концентрации OH–-ионов при окислении ванилина в присутствии [Mn2+Асас]–катализатора в водно-щелочной среде (I) и в этанольно-водно-щелочной среде (содержание спирта – 50 об. %) (II): 1– кривая, полученная расчетным методом; 2 – кривая, полученная по экспериментальным данным. |
Сопоставление зависимостей ∆v0(кат)=f([OH-]), полученных по экспериментальным и расчетным данным (Рис. 14, 15) указывает на адекватность предложенной кинетической схемы.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




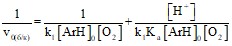 ,
,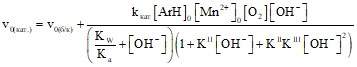 ,
,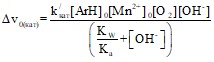 ,
,


