Сульфиды металлов обычно получают катодным осаждением в водных растворах, которые содержат Na2S2O3 и соли соответствующего металла, входящего в состав соединения. В литературе можно найти различные представления о реакциях, описывающих формирование CdS. Например, предлагается следующая последовательность реакций:
- на начальном этапе происходит диспропорционирование тиосульфат иона
![]()
- на второй стадии происходит катодное восстановление элементарной серы
![]()
- образовавшийся анион взаимодействует с катионами кадмия, образуя труднорастворимое соединение.
Приведенное объяснение вызывает справедливую критику, т. к. этими реакциями обосновывают возможность осаждения соединения в нанопористую матрицу. Однако, образование соединения не локализуется на поверхности электрода. В то же самое время результаты электронной и атомно-силовой микроскопии указывают на конформное заполнение наноразмерных пор в органической пленке.
Иногда предполагают, что ионы металла взаимодействуют с ионами серы, образующейся в результате следующей реакции
![]()
Однако и в этом случае отсутствие твердого вещества, образующихся на подложке, затрудняет понимание образование хорошо связанных с подложкой осадков.
Для протекания процесса образования полупроводниковых пленок сульфидов на поверхности электрода (не в объеме раствора) необходимо, чтобы отдельные компоненты или в целом соединение восстанавливались в твердом виде на поверхности. Например, частично отвечают этим требованиям следующие две электродные реакции:
![]()
![]()
Если бы реакция выделения элементарной серы была электрохимической, а не химической, то предложенный механизм мог бы объяснить наблюдаемые зависимости состава полупроводника от кислотности и концентрации электролита. В частности, наблюдается уменьшение концентрации серы с ростом рН и независимость соотношения концентраций компонентов в осадке от концентрации соли олова в растворе. Однако, на базе предложенных реакций невозможно объяснить резкое увеличение содержания серы в пленке при низких катодных смещениях и низких рН.
Наряду с отмеченными проблемами прослеживается четкая аналогия в результатах электроосаждения халькогенидов практически любых металлов. Более того, электрохимическое поведение материалов этого ряда являлось предметом большого числа работ в связи с разработкой фотоэлектрохимических источников тока. Известные данные о коррозионном поведении халькогенидов металлов указывают на обратимость реакций осаждения-растворения в водных растворах. Это является существенной предпосылкой для применения равновесной термодинамики при анализе процесса осаждения полупроводников.
Наиболее простым способом определения оптимальных условий осаждения твердой фазы в обратимых электрохимических реакциях является применение диаграмм рН-потенциал (диаграмм Пурбе). Данный подход ранее нашел широкое применение в области геологической разведки (при анализе минерального состава подземных вод) и в практике коррозионной защиты металлов. В электрохимии полупроводников названная методика применялась очень редко.
При выяснении вероятности протекания той или иной реакции в гетерогенной электрохимической системе в данных конкретных условиях очень полезными оказываются диаграммы электрохимического равновесия. Последние отражают зависимость между равновесным потенциалом электрода, pH раствора и активностями (или концентрациями) прочих компонентов, участвующих в реакции.
На рис.1 представлена частная диаграмма рН-потенциал системы Cd-S-H2O, построенная на основании уравнений равновесия. Диаграмма такого типа позволяет определять области стабильности веществ, образующихся в результате химических и электрохимических реакций, условия протекания которых зависят от концентрации вводимых реагентов. Согласно проведенным расчетам в изучаемой системе возможны различные последовательности катодных реакций, протекающих в водном растворе солей CdSO4 и Na2S2O3.
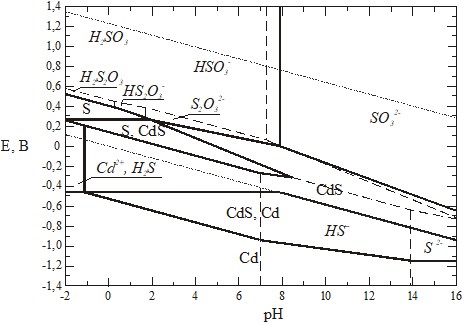
Рис.1. Диаграмма электрохимического равновесия системы CdS-H2O
Если в сильнокислых растворах первой катодной реакцией является осаждение элементарной серы, то в более щелочных растворах первой катодной реакцией оказывается образование полупроводникового осадка, который в зависимости от величин рН-показателя и потенциала может быть обогащен серой либо металлом. Однако известно, что равновесные диаграммы носят полуколичественный характер. Предсказанные последовательности реакций могут изменяться в результате кинетических ограничений некоторых стадий реакций. Например, возможно существенное отличие измеренных потенциалов от равновесных для реакций, в которых протекает восстановление компонентов, содержащих соединения серы. Это следует из того, что тиосульфат-анионы доставляются в зону катодной реакции только посредством диффузии. Поэтому только сопоставление результатов расчета и экспериментально наблюдаемых электродных процессов не позволяет определить механизмы протекающих реакций.
Если поляризация электрода сопровождается выделением на нем труднорастворимых или нерастворимых продуктов реакций, то для изучения механизмов протекающих реакций можно использовать циклическую вольтамперометрию (ЦВА). Эта методика представляет собой измерение плотности тока, протекающего через исследуемый электрод, при циклическом изменении разности потенциалов между рабочим и вспомогательным электродами. Так как CdS и большинство других халькогенидов металлов имеют низкие значения произведения растворимости, то ЦВА позволяет с высокой степенью точности определять потенциалы осаждения и растворения этих веществ.
Результаты ЦВА измерений для системы Cd-S-H2O представлены на рис.2. Как следует из результатов исследований, пики катодных (С) и анодных (А) реакций смещаются в сторону отрицательных потенциалов по мере увеличения рН раствора, что соответствует предсказываемой диаграммой Пурбе (рис.1) закономерности.
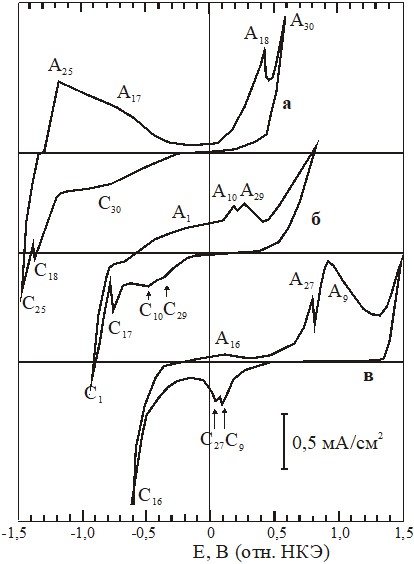
Рис.2. Кривые циклической вольтамперометрии, полученные при рН=2 (а), рН=7 (б) и рН=10 (в)
На основании представленных экспериментальных данных можно сделать следующие выводы о последовательности электродных процессов, протекающих в изучаемой системе:
1. В кислой среде при рН=2 (рис.2,а), по мере увеличения катодного смещения, на электроде сначала осаждается элементарная сера (пик С9), затем осадок содержит смесь S и CdS (С27), а на последнем этапе двухфазный осадок частично обедняется серой из-за образования H2S (С16). Изменение направления поляризации сопровождается вначале плохо выраженным пиком А16, соответствующим окислению H2S до элементарной серы, затем растворяется CdS (А27) и затем S (А9). Невысокая интенсивность пика А16 объясняется низкой концентрацией в растворе сероводородной кислоты, образующейся при катодной поляризации. Такая последовательность катодных и анодных реакций подтверждается измерениями в более узком диапазоне потенциалов. Так, если катодную поляризацию прекращали сразу после регистрации пика С27, то в анодной области пик окисления H2S (A16) исчезал, а если катодную поляризацию осуществляли до появления пика С27, то и пик растворения CdS (А27) отсутствовал на кинетической зависимости (рис.2).
2. В нейтральной среде при рН=7 (рис.2,б) реакция осаждения CdS (С29) предшествует процессу образования элементарной серы (С10). Кроме того, наблюдается пики катодного выделения HS - (C17) и Cd (С1). В анодной области ЦВА зависимости последовательно наблюдаются растворение Cd (А1), восстановление HS - до S (А17) и растворение S (A10) и CdS (А29).
3. В щелочной среде при рН=10 (рис.2в) обнаружены последовательно расположенные пики осаждения CdS (С29), выделения HS - (C18) Сd (С3) и соответствующие анодные пики и А3, A18 и А29.
Выводы о соответствии между пиками тока и механизмами протекающих процессов находятся в согласии с результатами ряда работ, выполненных разными авторами.
Наблюдаемое соответствие между кинетикой и термодинамикой процесса катодного осаждения CdS из водных растворов, содержащих ионы Cd2+ и S2O32- демонстрирует возможность применения диаграмм Пурбе для определения механизмов и оптимизации режимов электрохимического синтеза халькогенидов металлов. Так при необходимости получения сплошных пленок полупроводника можно работать в широком диапазоне катодных потенциалов, где образуется CdS и не происходит осаждение металлического Cd. Однако если требуется заполнить полупроводником узкие и глубокие каналы в диэлектрических масках (например, поры в анодном оксиде алюминия), то требования к выбору режима осаждения изменяются. В этом случае потенциал осаждения должен выбираться таким образом, чтобы избежать образования кислоты H2S и ее диссоциированных форм, которые вступают в химическое взаимодействие с ионами кадмия, стимулируя выпадение CdS в объеме раствора. В результате входные отверстия каналов «зарастают», и заполнение полупроводником нижележащих областей затрудняется (рис.3).
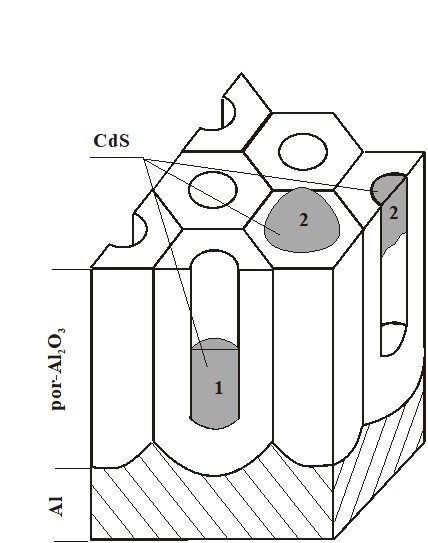
Рис.3. Возможные пути осаждения CdS в por-Al2O3: 1 - формирование наноразмерных нитей;
2 - образование неупорядоченной структуры в результате объемного выделения полупроводника
Катодное заполнение нанометровых диэлектрических пористых матриц халькогенидами металлов необходимо проводить в условиях, когда объемное выделение осадка минимально. Следует кратко остановиться на технологической особенности использования пористого анодного оксида алюминия в качестве размер задающей маски.
Известно, что ПАОП Al характеризуется наличием барьерной оксидной пленки в донной части поры. Толщина этого оксида определяется режимами формирования пленки и составом электролита. Незначительные различия в толщине барьерной пленки могут приводить к неоднородному заполнению пор полупроводником при катодном осаждении. Поэтому необходимо использовать оксиды, в которых толщина барьерного слоя минимальна. Это достаточно просто реализуется следующим образом:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



