Метаболизм аминокислот с разветвленной цепочкой. Речь идет о 3 аминокислотах.: лейцин, изолейцин, валин. Эти аминокислоты помимо участия в формировании полипептидных цепочек, подвергаются окислительному декарбоксилированию с участием высокоспецифичных ферментов. В отдельных случаях возможны генетические дефекты катаболизма этих аминокислот, которые проявляются в формировании заболевания «болезнь клинового сиропа» Моча пахнет кленовым сиропом.
15Белок или протеин – высокомолекулярное азотосодержащее вещество органическое вещество, молекулы которых построены из аминокислот. Живая природа отличается рядом свойств:1)разнообразие строения живых существ;2)живые системы способны к воспроизведению себе подобных;3)способность к движению;4)обновление составных частей. Для каждой живой системы характерен свой набор белков, например: а)кишечная палочка – примерно 3000 белков, все из них построены из двадцати л-аминокислот;б)человек – примерно 100тысяч белков. В природе обнаружено ![]()
![]() белков, все из них построены из двадцати л-аминокислот. Все аминокислоты линейно последовательны в белках, линейная последовательность аминокислот закодирована в ДНК.
белков, все из них построены из двадцати л-аминокислот. Все аминокислоты линейно последовательны в белках, линейная последовательность аминокислот закодирована в ДНК.
16Функции белков: 1)каталитическая – способность белков ускорять достижение равновесия химической реакции; 2)транспортная – участие белков в переносе молекул различной степени сложности; 3)защитная – белки нейтрализуют агрессивное воздействие веществ; 4)сократительная – способность специализированных белков изменять свои линейные параметры, или длину; 5)структурная (пластическая) – формирование структуры каждой клетки и ее органеллы, формирование основ ткани и органов; 6)гормональная (регуляторная) – обеспечение регуляторных воздействий в клетках и тканях; 7)питательная – белки могут быть использованы в виде трофического источника; 8)энергетическая – белковая молекула, отработав свой ресурс, подвергается деполяризации и освободившиеся аминокислоты вовлекаются в окислительный распад; энергетическая ценность 1 гр. Белка = 4,1 кКалл.
17Микроорганизмы, растения и животные отличаются по количеству белков в клетках, больше всего в животных тканях. Белки отличаются по аминокислотному составу, и чем сложнее организм, тем выше требования к соблюдению аминокислотного состава. Количественное отличие по содержанию белков предопределяет пищевую ценность данного источника белка, например: из 100 гр. мяса получается 20 гр. белка. Элементарный состав белков: углерод, кислород, водород, азот, сера.
18 Белки представляют собой сложные полипептиды, в которых отдельные аминокислоты связаны друг с другом пептидными связями, возникающими при взаимодействии –COOH и NH2-.
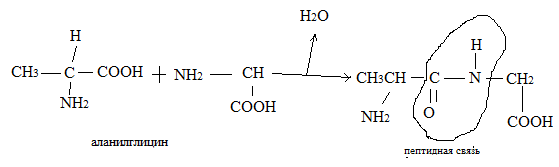
1)запись начинается с N-концевой аминокислоты, т. е. с той, которая имеет свободную аминогруппу, другой конец представлен С-концевой аминокислотой; 2)название полипептида начинается с названия N-концевой аминокислоты, далее добавляется последовательно С-концевая; конец первой меняется с «ин» на «ил».
19Под первичной структурой белка любого биополимера подразумевают последовательность соединения мономеров. Алгоритм определения первичной структуры белка:1)выделить свободную полипептидную цепь:
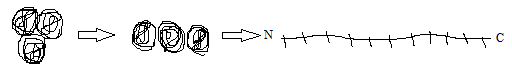
2)гидролиз цепи: узнать, из каких частей она состоит;3)последовательное отщепление аминокислот с любого конца. Характеристика первичной структуры белка: 1)первичная структура белка уникальна и генетически детерминирована: каждая белковая молекула имеет строго определенную последовательность аминокислот;2) стабильность первичой структуры обеспечивается ковалентными пептидными связями;3) полипептидная связь может быть сформирована разнообразными комбинациями аминокислот.
20Под вторичной структурой белка подразумевают конфигурацию полипептидной цепи, т. е. способ свертывания, скручивания полипептидной цепи в спиральную или какую-либо другую конфигурацию. Процесс этот не хаотичен. Две основные конфигурации полипептидных цепей: 1) л-спираль: отдельные участки цепи закручиваются по часовой стрелке, выявляется ряд закономерностей: а) на каждый виток приходится 3,6 аминокислотных остатка; б) через каждые пять витков (18 аминокислот) конфигурация спирали повторяется; 2) в-структура: две или более линейные полипептидные цепи располагаются параллельно, между ними формируются водородные связи, в образовании которых участвует N-, H-, CO - группы. Надвторичные структуры (домены) – отдельные участки полипептидной цепи, обладающие собственной вторичной структурой, и и связанные между собой в своеобразные функциональные комплексы.
21полипептидной спирали или способ укладки полипептидной цепи в определенном объеме. Различают две основные формы третичных конфигураций, это Т-форма – напряженная форма и R-форма – расслабленная форма; эти формы могут взаимопереходить друг в друга, образуя на каком-то этапе трансформации оптимальную третичную конфигурацию. Полипептидная цепь предопределяет особенность третичной структуры, однако в некоторых случаях было обнаружено, что практические одинаковые полипептиды образуют различные трехмерные структуры; полипептиды с разными последованиями аминокислот имеют одинаково последовательную структуру.
22Под четвертичной структурой белка подразумевают объединение отдельных полипептидных цепей, каждая из которых обладает первичной структурой, вторичной структурой, третичной структурой в единую функционально-активную молекулу, обеспечивающую ту или иную функцию, например: молекула гемоглобина. В биосистемах четвертичная структура чаще построена из четного числа субъединиц (по отдельности которые не обладают биологической активностью). Многие из ферментов построены с использованием четвертичной структуры. Для отдельных органов и тканей характерно наличие ферментов, состоящих из субъединиц в различных соотношениях; на основании этого было выяснено явление изофермии ферментов, и доказана диагностическая значимость определения активности изомеров при патологии тех или иных органов.
23В соответствии с функциональным принципом выделяют 12 классов белков: 1)белки-ферменты;2) белки-гармоны;3) белки-регуляторы;4) защитные белки;5) транспортные белки;6) сократительные белки;7) рецепторные;8) таксические;9) мембранные;10) белки вирусных оболочек;11) ингибиторы-ферменты;12) с иными функциями. В зависимости от химического состава:1)простые (состоят из аминокислот); 2)сложные (состоят из простого белка и небелкового компонента).
24Физико-химические свойства белков: 1)белки амфотерны; 2)способны к буферному взаимодействию; 3)имеют заряд на молекуле белка; 4)явление светорассеяния – используется при количественном определение белков; 5)гидрофильность белка – формирование онкатического давления; 6)белки не способны к диффузии. Молекулярная масса белков: определение молекулярной массы проводится физико-химическими методами, к которым относят: а)седиментационныйанализ; б)дихромотографию; в)электрофорез. Современные методы диэлектрофореза позволяют достаточно точно и бычтро определить молекулярную массу белка по скорости его миграции. В тех случаях, когда известен молекулярный состав белка, его молекулярную массу определяют исходя из молекулярного веса конкретных аминокислот.
25Природные белковые тела наделены определенной, строго заданной пространственной конфигурацией и обладают рядом характерных физико-химических и биологических свойств при физиологических значениях температуры и pH среды. Под влиянием различных химических и биологических факторов белки подвергаются свертыванию и выпадают в осадок, теряя нативные свойства. Денатурация – нарушение общего плана уникальной структуры нативной молекулы белка, преимущественно ее третичной структуры, приводящее к потере характерных для нее свойств. Большинство белков денатурирует при нагревании их растворов выше 50 – 60 градусов по цельсию. Наиболее прочные – пептидные связи, закрепляющие первичную структуру, расщепление их происходит при сильном изменении условий среды. Так же денатурацию могут вызвать кислоты и щелочи высокой концентрации, концентрированные растворы неорганических солей и органических соединений. На первых этапах денатурации возможно восстановление исходной структуры – ренатурация. Суммарный заряд на молекуле белка придает ей устойчивость. Как правило, белок имеет тот или иной заряд, изменение кислотности среды нейтрализует заряд на белковой молекуле вплоть до полного его исчезновения, это состояние – изоэлектрическая точка.
26Наиболее часто встречаемые простые белки животных тканей – альбумины и глобулины, протамины и гистоны. Альбумины растворимы в дистиллированной воде, а глобулины нет, что связано с молекулярной массой их: у альбуминов 40 – 70 тысяч, у глобулинов 150 и более тысяч. Синтез белков плазмы крови осуществляется в печени, в моноцитах крови. В плазме крови: альбумины 40 - 60 г/л, глобулины 20 - 40 г/л, фибрины 2 – 4 г/л. Фибрин в неактивной плазме представляет собой глобулярный белок, но при запуске механизма свертывания он превращается в фибрин. Альбумины формируют в плазме крови онкатическое давление (метаболический обмен между кровью и тканями в капиллярах), обеспечивают вязкость крови. Белки плазмы крови участвуют в поддержании кислотно-основного баланса, выступают в роли резерва аминокислот, обеспечивают свертывание крови. Методы исследования белкового состава крови: 1. Электрофорез на бумаге – выделено 5 фракций белков, электрофорез в агаровом геле – выделено 8 фракций, в полиакриламиновом геле – 17 фракций.
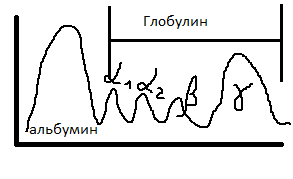
Альбумин: период полураспада составляет около семи дней, участвует в транспорте стироидных структур, принимает участие в транспорте гормонов.
27 Гаммаглобулин – совокупность иммуноглобулинов, совокупность антител плазмы крови. Гаммаглобулин вырабатывается В-лимфоцитами. Дефицит гаммаглобулина – любая ситуация, которая приводит к имунодифициту. Главная причина избытка гаммаглобулина – опухолевое перерождение (В-лимфоциты продуцируют избыточное количество гаммаглобулина).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



