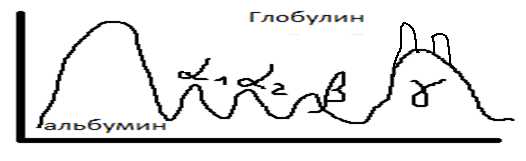
Пики указывают на избыток данной фракции гаммаглобулина. Бывает генетически обусловленная недостаточность гуморального иммунитета, когда отсутствуют В-лимфоциты → нет гаммаглобулинов (болезнь Бруттена, агаммаглобулинемия).
28При различных патологических изменениях в организме, а так же при нарушении баланса при взаимодействии с внешней средой в организме происходят количественные и качественные изменения белков в плазме крови. 1 – гипердиспротеинемия: увеличение количества белков в плазме крови: а)относительная гипердиспротеинемия: пропорциональное увеличение концентрации всех белковых фракций; б)абсолютная: неадекватное образование белковых фракций. 2 – гиподиспротеинемия: снижение количества белков в плазме крови: а) потеря белков из организма, здесь такие болезни, как асцит, нефратический синдром; б) нарушение синтеза белков в печени: атрофия печени, жировая дистрофия; в)белковая недостаточность рациона: голодание, истощение.
29Гаптоглобин – необходим для обеспечения катаболической фазы гемоглобина. Каптоглобин с гемоглобином формируют комплексы, которые задерживаются макрофагами ткани, и этот комплекс подвергается деполяризации. 2. Трансферин – относится к бетта-глобулинам. Этот белок осуществляет рециркуляцию железа в организме. 3. Церулоплазмин – при его недостаточности развивается гепотоцелибральная дистрофия, при этом заболевании нарушается структура и функция печени, а так же головного мозга, отвечающего за кинематику движений. 4. Криоглобулин – в норме отсутствует, но при при некоторых патологических процессах криоглобулин начинает циркулировать в крови (поражение печени, опухоли крови).
30В крови постоянно циркулируют постоянные ферменты: 1. Секретные ферменты: чаще синтезируются в печени, секретируются в кровь, где выполняют ту или иную функцию; 2. Экскреторные ферменты: образуются в печени, и в физиологических условиях выделяются в состав желчи и далее. 3. Клеточные ферменты: в норме они почти не содержаться в крови, при разрушении клеток, они вымываются в кровь, и наличие их в крови можно определить по их активности. Современные методы исследования позволяют определить не только общую активность данного элемента, но и установит изферментный спектр этого фермента. 4. Протамины и гистоны: эти белки отличаются своеобразием аминокислотного состава, в них преобладают основные аминокислоты, которые придают этим белкам способность взаимодействовать с карбоксильными радикалами. В протаминах содержание альгенина доходит до 60-80 %. Протамины хорошо растворимы в воде, сложно растворимы в солевых растворах.
31Протамины и гистоны: эти белки отличаются своеобразием аминокислотного состава, в них преобладают основные аминокислоты, которые придают этим белкам способность взаимодействовать с карбоксильными радикалами. В протаминах содержание альгенина доходит до 60-80 %. Протамины хорошо растворимы в воде, сложно растворимы в солевых растворах. Растительные белки – проламины и глютелины, они содеожаться в семенах злаков. В зависимости от злаков, выделяют специфические белки этих злаков, например: из кукурузы выделяют зиин, ячменя – гордеин, из пшеницы – глиалин и т. д. Эти белки отличаются друг от друга составом аминокислот. При гидролизе в пищеварительном тракте из этих белков могут образоваться короткие пептиды, обладающие для некоторых людей токсическим эффектом.
32Пептиды – короткие полипептидные цепочки, содержащие около десяти аминокислот. В организме у человека обнаружены эти пептидов, и исследованы их физиологические функции. В соответствии с этим подразделяют: пептиды, обладающие гормональной активностью; пептиды, регулирующие процессы пищеварения; пептиды, регулирующие гомеостаз; нейропептиды – пептиды нервной ткани.
33Сложные белки состоят их двух компонентов: 1)белковая часть – полипептидная цепь, 2)вещество любой химической природы, но не белковой, которое химически связано с белковой частью. Хромопротеиды – белки, имеющие ту, или иную окраску. В подавляющем большинстве хемопротеиды принимают участие в обменах, связанных с превращением энергии; обеспечивают фотосинтез, дыхание клеток, транспорт кислорода; входят в состав дыхательной цепи ферментов. Хемопротеины: 1)гемопротеины, 2) хлорофиллы, 3) флавопротеины. Гемопротеиды: 1)гемоглобин, и его производные, 2)меоглобин, 3)гемосодержащие ферменты, 4)железопорферины – небелковые компоненты.
34Структура белковой части гемоглобина: состоит из четырех полипептидных цепей, а точнее из двух пар. В зависимости от того, какие полипептидные цепи входят в состав данного гемоглобина, различают несколько его разновидностей: 1)гемоглобин взрослый (гемоглобин А): две альфа и две бета полипептидные цепи, в альфа-цепи 141 аминокислота, в бета-цепи 146, отсюда вся молекула белка в структуре гемоглобина содержит 574 аминокислоты. 2) гемоглобин F: состоит из двух альфа - и двух гамма-цепей. В процессе жизни и деятельности человека возможно нарушение структуры полепептидных цепей гемоглобина, причем важную роль играет локализация мутации в объеме трехмерной конфигурации. Если замена аминокислоты происходит на поверхности молекулы гемоглобина, то это мутация первого класса, она не приводит к развитию патологии, если происходит замена аминокислоты в непосредственной близости от гемо, то формируется клиническая картина заболевания. В структуру гемо встроена в качестве основной структурной единицы – железо. Часто количество гемоглобина определяется количеством железа, при его недостатке: железодифицитная анемия (в составе эритроцитов не хватает гемоглобина). В этом случае, если гемоглобин соединяется с кислородом, то его называют оксигемоглобином, если он отделяется от кислорода – восстановленный гемоглобин. Гемоглобин может присоединить окись углерода – карбоксигемогобин. Карбоксигемоглобин – обычный гемоглобин, занятый выполнением своих функций. При воздействии на гемоглобин оксидов азота в различных вариантах происходит изменение валентности железа.
35Структура белковой части гемоглобина: состоит из четырех полипептидных цепей, а точнее из двух пар. В зависимости от того, какие полипептидные цепи входят в состав данного гемоглобина, различают несколько его разновидностей: 1)гемоглобин взрослый (гемоглобин А): две альфа и две бета полипептидные цепи, в альфа-цепи 141 аминокислота, в бета-цепи 146, отсюда вся молекула белка в структуре гемоглобина содержит 574 аминокислоты. 2) гемоглобин F: состоит из двух альфа - и двух гамма-цепей. В процессе жизни и деятельности человека возможно нарушение структуры полепептидных цепей гемоглобина, причем важную роль играет локализация мутации в объеме трехмерной конфигурации. Если замена аминокислоты происходит на поверхности молекулы гемоглобина, то это мутация первого класса, она не приводит к развитию патологии, если происходит замена аминокислоты в непосредственной близости от гемо, то формируется клиническая картина заболевания. В структуру гемо встроена в качестве основной структурной единицы – железо.
36Структура белковой части гемоглобина: состоит из четырех полипептидных цепей, а точнее из двух пар. В зависимости от того, какие полипептидные цепи входят в состав данного гемоглобина, различают несколько его разновидностей: 1)гемоглобин взрослый (гемоглобин А): две альфа и две бета полипептидные цепи, в альфа-цепи 141 аминокислота, в бета-цепи 146, отсюда вся молекула белка в структуре гемоглобина содержит 574 аминокислоты. 2) гемоглобин F: состоит из двух альфа - и двух гамма-цепей. В процессе жизни и деятельности человека возможно нарушение структуры полепептидных цепей гемоглобина, причем важную роль играет локализация мутации в объеме трехмерной конфигурации. Если замена аминокислоты происходит на поверхности молекулы гемоглобина, то это мутация первого класса, она не приводит к развитию патологии, если происходит замена аминокислоты в непосредственной близости от гемо, то формируется клиническая картина заболевания. При мутации полипептидной цепи внутри молекулы – чаще всего летальный исход. Наиболее распространенная болезнь, связанная с нарушением структуры гемоглобина – гемоглабинопатия, в которой происходит мутационная замена одной или нескольких аминокислот; наиболее известна – серповидно-клеточная анемия, суть этого дефекта – в бета-цепи в шестом положении глютолиновая кислота заменена на валин (гемоглобин S в составе эритроцитов выпадает в осадок, что приводит к изменению формы эритроцитов). Другой вариант патологии – талассемия: изменение соотношения цепей в молекуле гемоглобина.
37Липопротеин – белок, в состав которого в качестве небелкового компонента входят липиды (нейтральный жир, холестерин, холестерол). Липиды обладают следующими функциями: 1) липиды являются главными структурными компонентами всех клеточных мембран; 2) выполняют ряд специфических функций, например: обеспечивают сохранение объема и структуры альвеолы в легких; 3) входят в структуру миелиновых оболочек нервных волокон. Большинство нервных островков нейрона заключено в миелиновую оболочку, которая изолирует отростки нервных клеток друг от друга. В крови у человека содержаться липиды в различных формах, которые являются транспортными системами, обеспечивающими доставку липидов в клетки; вывод «отработавших» липидов к местам выведения. Транспортные формы липидов синтезируются в слизистой оболочке кишечника. В печени осуществляется синтез липопротеинов, которые доставляют липиды к нуждающимся в них клеткам ткани, при этом синтезируются липопротеины очень низкой плотности. По мере «выедания» клетками липидов, они превращаются в липопротеины промежуточной плотности, которые после осуществляют выбор «отработавших » липидов из органов и тканей.
38Липопротеин – белок, в состав которого в качестве небелкового компонента входят липиды (нейтральный жир, холестерин, холестерол). Липиды обладают следующими функциями:1) липиды являются главными структурными компонентами всех клеточных мембран; 2) выполняют ряд специфических функций, например: обеспечивают сохранение объема и структуры альвеолы в легких; 3) входят в структуру миелиновых оболочек нервных волокон. Большинство нервных островков нейрона заключено в миелиновую оболочку, которая изолирует отростки нервных клеток друг от друга. В крови у человека содержаться липиды в различных формах, которые являются транспортными системами, обеспечивающими доставку липидов в клетки; вывод «отработавших» липидов к местам выведения. Транспортные формы липидов синтезируются в слизистой оболочке кишечника. В печени осуществляется синтез липопротеинов, которые доставляют липиды к нуждающимся в них клеткам ткани, при этом синтезируются липопротеины очень низкой плотности. По мере «выедания» клетками липидов, они превращаются в липопротеины промежуточной плотности, которые после осуществляют выбор «отработавших » липидов из органов и тканей. В организме существует баланс между этими двумя группами липопротеинов. При нарушении этого баланса, возможна избыточная поставка липидов в органы и ткани, в том числе и холестерина, что приводит в конечном итоге к избыточному накоплению холестерина. В том случае, если происходит накопление холестерина в клетках артерии в виде артериальных бляшек, говорят о развитии атеросклероза, поэтому группу липидов ЛПОНП и ЛПНП называют атерогенными липопротеинами, а ЛППП и ЛПВП носят название антиатерогенных липопротеинов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



