Реактивы: смесь этилового спирта C2H5OH и концентрированной серной кислоты H2SO4 (соотношение 1:3), бромная вода Br2⋅aq,
Сухие или концентрированные вещества: | Растворы солей 5%-ные: |
натрия ацетат CH3COONa (кр.), натронная известь (смесь NaOH+Ca(OH)2) , кальция карбида СаС2 , | калия перманганат KMnO4 . |
Опыт 1. Получение и свойства метана.
В лабораториях метан получаю нагреванием смеси ацетата натрия с натронной известью (NaOH+Ca(OH)2)
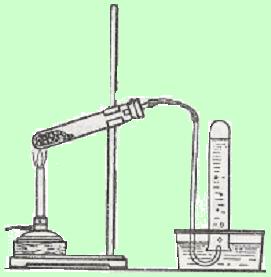
В сухую пробирку, снабженную пробкой с газоотводной трубкой, поместите смесь из обезвоженного ацетата натрия и натронной извести (высота слоя 4-6 мм, вещества необходимо хорошо перемешать). Соберите прибор, как показано на рисунке (Рис. 1.). Укрепите пробирку в зажиме штатива горизонтально и нагрейте смесь в пламени спиртовки. Напишите уравнение реакции, происходящей между ацетатом натрия и гидроксидом натрия.
Рис. 1. Установка для получения метана. | Подожгите выделяющийся газообразный метан у конца газоотводной трубки. Метан горит голубоватым пламенем. Напишите уравнение реакции горения метана. Нагревая реакционную смесь, пропустите выделяющийся метан поочередно в пробирки с раствором перманганата калия и бромной воды. Почему метан не обесцвечивает раствор перманганата калия и бромную воду? |
Опыт 2. Получение и свойства этилена.
Соберите прибор, как показано на рисунке (Рис. 2).
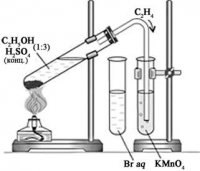
В пробирку, укрепленную в штативе, налейте 5 мл выданной вам смеси этилового спирта с серной кислотой (1:3), добавьте в смесь немного песка (для равномерного кипения жидкости). Закройте пробирку пробкой с газоотводной трубкой. Смесь нагревайте осторожно на пламени спиртовки. Объясните наблюдаемые явления. Составьте уравнения реакций. Когда начнется выделение этилена, пропускайте газ в пробирку с 2-3 мл бромной воды. Как только бромная вода обесцветится, смените пробирку и пропускайте этилен через подкисленный раствор перманганата калия. Составьте уравнения реакций. После обесцвечивания раствора перманганата калия газоотводную трубку необходимо вынуть из пробирки и повернуть ее отверстием вверх. Подожгите выделяющийся этилен. Обратите внимание на характер пламени (светящееся или бесцветное). Затем погасите пламя спиртовки. Составьте уравнения реакций.
Рис. 2. Установка для получения этилена. |
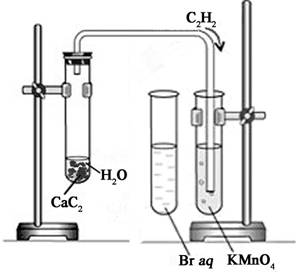
Рис. 3. Установка для получения ацетилена. |
Опыт 3. Получение ацетилена и его свойства.
Соберите прибор как показано на рисунке (Рис. 3).
Поместите в пробирку кусочек карбида кальция СаС2 , затем налейте ј пробирки воды. Закройте пробирку пробкой с газоотводной трубкой. Наблюдайте происходящую реакцию. Напишите уравнения реакции получения ацетилена. Подожгите выделяющийся газ. Напишите уравнения реакции горения ацетилена. Пропустите полученный ацетилен через бромную воду и раствор KMnO4 до их обесцвечивания. Напишите уравнения реакций взаимодействия ацетилена с бромом, обесцвечивания раствора KMnO4. Объясните наблюдаемые явления.Задание. Проведите сравнительную характеристику углеводородов (на примере алканов, алкенов, алкинов). Оформить в виде таблицы:
Сравнительная характеристика углеводородов
Алканы | Алкены | Алкины |
Общая формула | ||
Формула простейшего гомолога | ||
Тип гибридизации атомов углерода | ||
Отношение к раствору KMnO4 | ||
Отношение к бромной воде Br2 |
Задание. Из приведенного перечня реакций:
Нитрование, Полимеризация, Гидратация, Хлорирование, Гидрирование;выберите реакции характерные для предельных и непредельных углеводородов; составьте соответствующие уравнения с указанием условий проведения реакций. Оформите в виде таблицы:
Тип реакции | Уравнения реакций |
Предельные УВ | Непредельные УВ |
Нитрование. | |
Полимеризация. | |
Гидратация. | |
Хлорирование. |
Лабораторная работа №3. Химические свойства спиртов и фенолов.
Оборудование: Штатив с пробирками, СПИРТОВКИ, пробиркодержатели.
Реактивы: бромная вода Br2⋅aq,
Сухие или концентрированные вещества: | Растворы кислот и щелочей 5%-ные: | Растворы солей 5%-ные: |
бензол C6H6 , глицерин C3H5(OH)3 , спирт этиловый C2H5OH, фенол C6H5OH, | кислота серная H2SO4 , калия гидроксид КОН, натрия гидроксид NaOH, | калия дихромат K2Cr2O7 , меди (II) сульфат CuSO4 . |
Опыт 1. Окисление спиртов.
Налить в пробирку 1-3 мл раствора K2Cr2O7 , 2 мл разбавленной серной кислоты и прибавить примерно 1 мл этилового спирта. Осторожно нагреть пробирку. Заметить слабый запах уксусного альдегида и изменение окраски раствора. Дихромат калия выполняет роль окислителя.
Задание. Составьте уравнение реакции.
Свойства глицерина.
Опыт 2. Растворимость глицерина в воде.
В пробирку с 0,5 мл воды добавьте порциями по 0,5 мл, тщательно взбалтывая содержимое, 2 мл глицерина. Какие выводы можно сделать о растворимости глицерина в воде?
Опыт 3. Взаимодействие глицерина с гидроксидом меди (II).
К 1 мл раствора щелочи в пробирке добавьте равное количество раствора медного купороса. К образовавшемуся раствору гидроксида меди (II) прилейте 0,5 мл глицерина.
Задание. Объясните, какие изменения произошли. Составьте уравнения реакций. Будут ли наблюдаться такие же изменения, если вместо глицерина добавить этиловый спирт?
Свойства фенолов.
Опыт 4. Взаимодействие фенола с бромной водой.
К 1 мл водной эмульсии фенола добавьте равное количество бромной воды. Взболтайте смесь. Объясните, какие изменения произошли. Составьте уравнение реакции. Будут ли наблюдаться такие же изменения, если вместо фенола взять бензол?
Опыт 5. Взаимодействие фенола с раствором щелочи.
К 1 мл водной эмульсии фенола добавьте несколько капель раствора щелочи.
Задание. Объясните, какие изменения произошли. Составьте уравнение реакции.
Лабораторная работа №4. Химические свойства карбоновых кислот.
Оборудование: Штатив с пробирками, штативы с лапками, пробки с газоотводными трубками, стаканы на 50 мл, пробки резиновые для пробирок, СПИРТОВКИ, пробиркодержатели, пипетки.
Реактивы: раствор мыла, р-р фенолфталеина (капельница), бромная вода Br2⋅aq,
Сухие или концентрированные вещества: | Растворы кислот и щелочей 5%-ные: | Растворы солей 5%-ные: |
кислота серная H2SO4 (конц.), натрия ацетат CH3COONa (кр.) олеиновая кислота C17H33СОOH, | кислота уксусная CH3СОOH, | калия карбонат К2CO3 , калия перманганат KMnO4 , кальция хлорид CaCl2 , натрия карбонат Na2CO3 , натрия ацетат CH3COONa, железа(III) хлорид FeCl3 . |
Опыт 1. Получение уксусной кислоты.
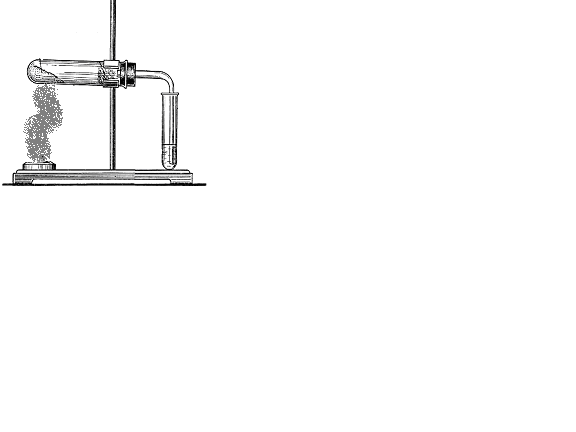
Соберите прибор как показано на рисунке (Рис. 4). В пробирку насыпьте 0,5 гр ацетата натрия (на кончике чайной ложки) и прилейте 5-6 капель концентрированной серной кислоты, чтобы она только смочила соль. Пробирку закройте пробкой с газоотводной трубкой, свободный конец которой опустите в пустую пробирку, находящуюся в стакане с водой.
Рис. 1. Установка для получения уксусной кислоты. | Нагревайте смесь до тех пор, пока в пробирке – приемнике - соберется немного уксусной кислоты, обратите внимание на запах. Напишите уравнения реакций взаимодействия ацетата натрия с серной кислотой. Полученную кислоту сохраните для следующего опыта, разбавив ее дистиллированной водой в два раза. |
Опыт 2.Образование солей.
а) К 0,5 мл раствора карбоната натрия прилейте равное количество разбавленной уксусной кислоты. Раствор начинает пениться. Объясните это явление. Составьте уравнение реакции.
б) В пробирку с раствором мыла добавьте несколько капель раствора хлорида кальция. Выпадет белый осадок нерастворимой соли. Составьте уравнение реакции.
Опыт 3. Непредельный характер олеиновой кислоты.
а) Окисление олеиновой кислоты.
В пробирку поместите 2 капли олеиновой кислоты, 2 капли перманганата калия, 1 каплю раствора карбоната калия. Встряхните пробирку. Розовая окраска раствора исчезает, что указывает на окисление олеиновой кислоты по месту двойной связи. Составьте уравнение реакции,
б) Присоединение брома к олеиновой кислоте. В пробирку налейте 0,5 мл бромной воды, добавьте 3-4 капли олеиновой кислоты и энергично взбалтывайте до обесцвечивания раствора. Составьте уравнение реакции.
Лабораторная работа №5. Химические свойства глюкозы, сахарозы, крахмала.
Оборудование: Штатив с пробирками, пипетки, ложка для крахмала, стакан на 50 мл, стакан на 250 мл, плитки электрические, СПИРТОВКИ, пробиркодержатели.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |