3. Результаты и их обсуждение.
Стимулом к изучению стволовых клеток человека служит то, что они таят в себе колоссальные возможности как с чисто научной точки зрения, так и в том, что касается их применения в клеточной терапии. Прежде всего речь идет о тех преимуществах, которые дает их использование при трансплантации. Если бы удалось получить стволовую клетку от взрослого индивида, стимулировать ее деление и изменить специализацию.
В тоже время следует найти способ индуцировать нужную спецификацию клеток. Одним из путей этой цели является трансфекция их различными ростовыми факторами под контролем подходящих промоторов. Удобной моделью для поиска таких промоторов служат гены флуоресцентных белков.
Для получения и исследования трансгенных клеточных культур, экспрессирующих зеленый флуоресцентный белок GFP, который в последствии будет использован в качестве маркера. Маркерный ген необходим для визуализации нахождения интересующего нас белка после трансплантации в мозг млекопитающих.
В работе использовался вектор pEGFP-N1 (GenBank Accession # U55762) (рисунок 1).
![]()
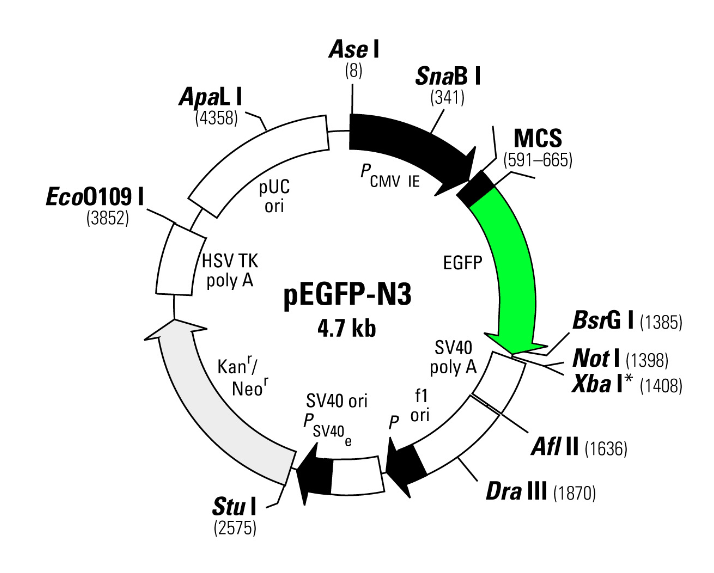
Рисунок 1. Схема векторной плазмиды pEGFP-N1.
После выделения и очистки вектор pEGFP-N1 был введен в культуру клеток HEK-293 методом трансфекции с использованием реагента ExGene 500 (Fermentas). Трансфекция производилась согласно протоколу. Культура клеток линии HEK-293 инкубировалась при 370С в СО2 инкубаторе. После селекции на гентамицине в течение 10 дней трансфекцированные клетки были рассеяны на 25см2 культуральные флаконы. Далее необходимо было отобрать под флуоресцентном микроскопом колонии клеток, который экспрессировали зеленый флуоресцентный белок GFP (рисунок 2).
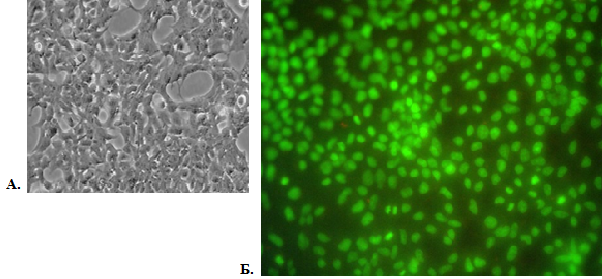
Рисунок 2. Клетки линии НЕК293, трансфицированные EGFP-N1 (микроскоп – Olympus CX41, увеличение х200). А – трансфицированные клетки линии НЕК293 в проходящем свете, Б – те же клетки в свете флуоресценции, свечение белка EGFP.
Эмбриональные стволовые клетки мыши (линия R1) pЕGFP-N1. Экспрессию EGFP детектировали через 48-72 часа по зеленому свечению клеток при просмотре в микроскоп Olympus СХ41 при соответствующей длине волны. Эффективность трансфекции составляла около 10 %. При культивации в присутствии G418 (200 мкг/мл) были получены стабильно трансфицированные клетки (рисунок 3).
 А.
А.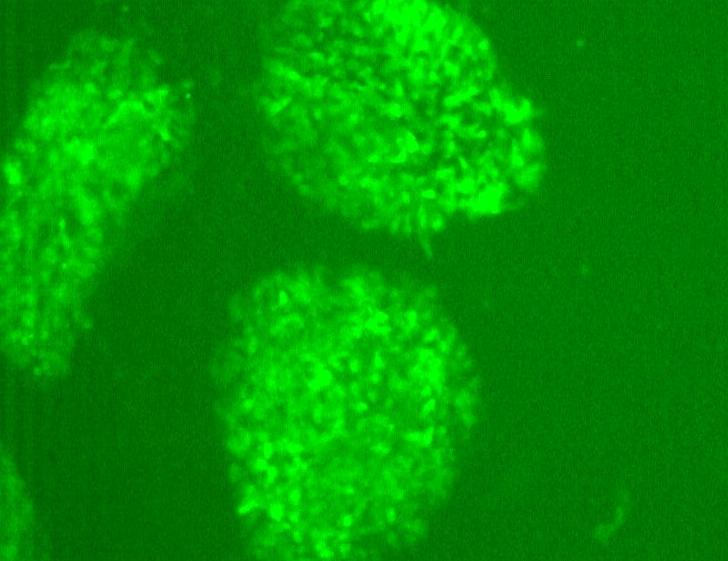 Б.
Б.
Рисунок 3. Эмбриональные стволовые клетки мыши (линия R1), трансфицированные EGFP-N1 (микроскоп – Olympus CX41, увеличение х200). А – колонии трансфицированных клеток, фазовый контраст; Б – свечение белка EGFP в трансфицированных клетках
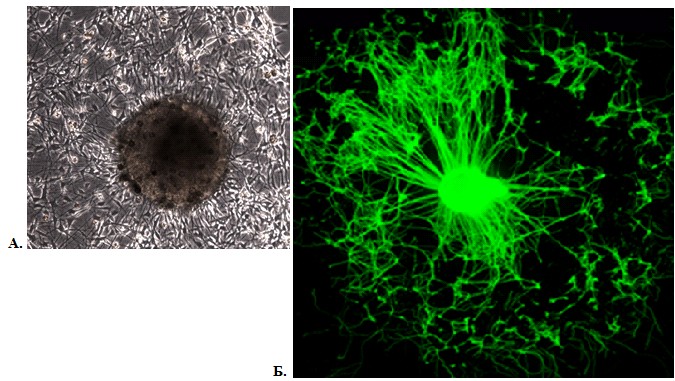
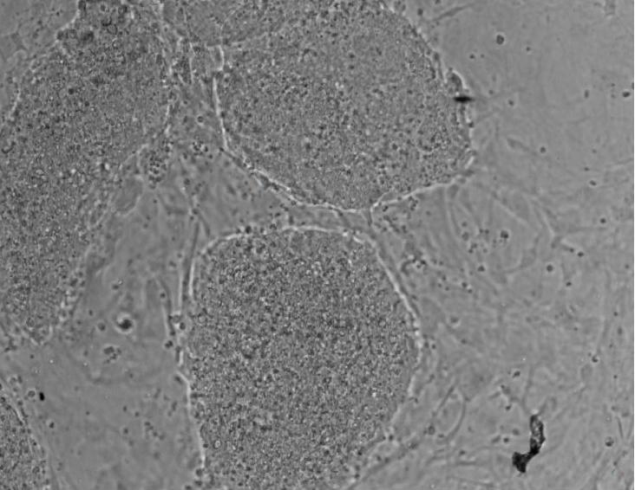
В экcпериментах с эмбриональными стволовыми клетками мыши (линия bNCSC), трансгенных по GFP мы также обнаружили свечение зеленого флуоресцентного белка после трансфекцией изучаемым вектором pEGFP-N1 (рисунок 4).
Рисунок 4. Эмбриональные стволовые клетки мыши (линия bNCSC), трансфицированные EGFP-N1 (микроскоп – Olympus CX41, увеличение х200). А –нейросфера трансфицированных клеток, фазовый контраст (нейросфера на подложке культурального пластика); Б – свечение белка EGFP в трансфицированных клетках.
Таким образом, можно утверждать, что GFP экспрессируется в трансгенных клетках эмбрионального происхождения, что было обнаружено с подтверждено с помощью Вестерн-блот-гибридизации и визуального контроля. Тем не менее, мы проверили наличие нашей конструкции в клетках. Для этого была выделен из данной культуры клеток, для последующего анализа с помощью Вестерн - блот гибридизации (рисунок 5).
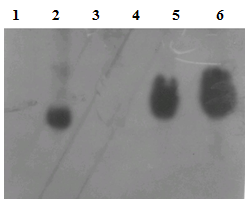
Рисунок 5. Вестерн-блот анализ лизата трансгенных клеток с антителами против GFP. Вестерн-блот гибридизация. 1. – Белок, выделенный из клеток НЕК293 2.- Белок, выделенный из трансгенных клеток линии НЕК293/GFP 3.- Белок, выделенный из эмбриональных стволовых клеток мыши (линия R1) 4.- Белок, выделенный из эмбриональных стволовых клеток мыши (линия bNCSC) 5.- Белок, выделенный из трансгенных клеток R1/GFP 6.- Белок, выделенный из трансгенных клеток bNCSC /GFP.
Данное исследование является фрагментом большой работы, проводимой в лаборатории ИБГ РАН по изучению возможностей использования эмбриональных и стромальных стволовых нейральных клеток млекопитающих для трансплантации в различных областях клеточной терапии, в частности, для лечения нейродегенеративных заболеваний.
Такая разнообразная система эмбриональных клеток млекопитающих и человека позволит не только использовать векторные системы, но и многообразные генетические конструкции, содержащие факторы, стимулирующие рост и развитие различных типов нейронов, которые гибнут при нейрогенеративных заболеваниях. Нами показано, что эмбриональные клетки подвергаются трансфекции, поэтому могут быть использованы в качестве носителей химерных генов при генной трансплантации.
4. Выводы.
В ходе исследования были получены следующие выводы:
Показано многообразие белков в природе; Описано понятие флуоресценция и ее значимость в медицине; Рассмотрено строение флуоресцентных белков, на примере зеленого флуоресцентного белка GFP; Проведен анализ экспрессии зеленого флуоресцентного белка GFP в клетках млекопитающего; Проанализировано свечение зеленого флуоресцентного белка после трансфекции эмбриональных стволовых клеток человека и млекопитающих.5. Список литературы.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |


