Окисляемость, характеризующая содержание органических веществ в профильтрованной воде, выражается в мг кислорода или мг перманганата калия (КМnО4), необходимых для окисления органических веществ, содержащихся в 1 л воды.
Жесткость определяется содержанием в воде ионов накипеобразователей — солей щелочноземельных металлов Са и Мg. Различают жесткость карбонатную (временную) Нк и некарбонатную (постоянную) Нp; сумма их дает общую жесткость Н0.
Карбонатная жесткость обусловливается наличием бикарбонатов Са и Мg, которые при нагревании воды разлагаются. Постоянная жесткость определяется содержанием в воде тех солей Са и Мg, которые при нагревании не разлагаются.
Прежде в качестве единицы измерения жесткости был принят немецкий градус жесткости (°Н), соответствующий содержанию 10 мг СаО в 1 л воды. Позднее введена новая единица — миллиграмм-эквивалент на 1 л (мг экв/л) для измерения высоких жесткостей и микрограмм-эквивалент на 1 л (мкг экв/л) для измерения малых жесткостей. Соотношения между различными единицами измерения жесткости приведены в табл. 3.13
Таблица 3.13. Пересчёт различных единиц измерения жесткости
в миллиграмм-эквиваленты
Единицы измерения жесткости
Миллиграмм-эквивалент
Немецкий градус
Французский градус
Английский градус
Американский градус
1 миллиграмм-эквивалент в
литре………………………
1 немецкий градус……….
1 французский градус……
1 английский градус......
1 американский градус.....
1
0,35663
0,19982
0,28483
0,01998
2,804
1
0,5603
0,7987
0,0560
5,005
1,7843
1
1,4255
0,1
3,511
1,2521
0,7015
1
0,0702
50,045 17,847
10
14,255
1
В табл. 3.14 приведены значения молекулярного веса и содержания различных соединений, эквивалентные единицам жесткости.
Таблица 3.14. Содержания различных соединений,
эквивалентные единицами жесткости
Химическая формула
Молекулярный
вес
Эквивалент в мг/л
Химическая формула
Молекулярный
вес
Эквивалент в мг/л
1 мг экв/л
1о Н
1 мг экв/л
1о Н
А12 (SО4)3
СаС12
СаСO3
СаО
Са (ОН)2
СаSО4
Cl2
СО2
FеSО4
МgСl2
МgСО3
342,12
111,00
100,09
56,03
74,10
136,14
70,92
44,00
151,92
95,24
84,32
57,02
55,50
50,045
28,04
37,05
68,07
35,46
22,00
75,96
47,62
42,16
20,34
19,90
17,85
10,00
13,21
24,28
12,65
7,85
27,09
17,00
15,03
Мg (НСО3)2
MgO
Мg (ОН)2
МgSO4
NаСl
N2СО3
NаНСОз
NаОН
SiO2
SiО3
SiО4
146,36
40,32
58,34
120,38
58,45
106,00
84,00
40,00
76,06
80,06
96,06
73,18
20,16
29,17
60,19
58,45
53,00
84,00
40,00
38,03
40,03
48,03
26,10
7,19
10,41
21,50
20,85
18,90
30,00
14,27
13,60
14,28
17,13
Соотношение растворенных в воде веществ определяет реакцию воды, придавая ей кислый или щелочной характер. Критерием является концентрация водородных ионов Н+ в 1 л воды; он обозначается индексом рН:
![]()
Чистая химическая вода имеет рН = 7. Общепринята следующая шкала, характеризующая реакцию воды: рН < 5,5 — реакция воды сильно кислая; рН =5,5 ÷ 6,5 − реакция слабокислая; рН= 6,5 ÷ 7,5 − нейтральная; рH=8 ÷ 10 − слабо щелочная; рН > 10 − сильно щелочная.
Различают две категории водопользования. К первой категории относится использование водного объекта в качестве источника централизованного или нецентрализованного хозяйственно-питьевого водоснабжения, а также водоснабжения предприятий пищевой промышленности; ко второй категории — использование водного объекта для купания, спорта и отдыха населения, а также использование водных объектов, находящихся в черте населенных мест.
При сбросе сточных вод в черте города (или любого населенного пункта) первым пунктом водопользования является данный город (или населенный пункт); в этих случаях требования к составу и свойствам воды водоема или водотока должны относиться к самим сточным водам. Состав и свойства воды водного объекта в пунктах хозяйственно-питьевого и культурно-бытового водопользования ни по одному из показателей не должны превышать установленные нормативы (табл. 3.15).
Запасы воды на Земле достаточно велики: три четверти земной поверхности покрыто водой, но пресной воды лишь 2,5 % . Она сосредоточена в основном в ледниках − 24 млн. км3, в подземных водах − 10 млн. км3, пресные озера, болота и реки содержат около 100 тыс. км3. Пресной водой считается вода, в которой концентрация солей не более 1кг/м3.
Динамика мирового потребления (в км3/год) воды выглядит так:
1900 г.
20
30
360
1940 г.
40
120
660
1975 г.
147
633
2700
2000 г.
440
1900
3400
1. Бытовое использование воды
2. Промышленное использование
3 Сельскохозяйственное использование (орошение и пр.)
В настоящее время ежесуточно на 1 человека в бытовых целях расходуется (л/сут.): Лондон − 250, Санкт-Петербург − 370, Париж − 500, Москва и Нью-Йорк − 600.
Существующие системы водоснабжения можно разделить на прямоточные, в которых вода забирается из природного источника, очищается, используется в технологических процессах, снова очищается и сбрасывается в природный источник и оборотные, в которых вода забирается из природного источника, очищается, используется в технологических процессах, очищается и снова используется в технологических процессах.
При оборотном водоснабжении практически не образуется накипи на стенках котлов, труб, отпадает необходимость в их периодической очистке, значительно сокращается расход воды. В соответствии с правилами охраны поверхностных вод рекомендуется оборотная система водоснабжения. В нашей стране 65% общего водоснабжения для промышленных целей обеспечивается путем оборотного и повторного водоснабжения.
Таблица 3.15. Общие требования к составу и свойствам воды водных объектов у пунктов хозяйственно-питьевого и культурно-бытового водопользования
Показатели состава и свойств воды водоема или водотока
Категория водопользования
- для централизованного или нецентрализованного хозяйственно-питьевого водоснабжения, а также для водоснабжения пищевых предприятий
- для купания, спорта и отдыха населения, а также для водоемов в черте населенных мест
Взвешенные вещества
Плавающие примеси
Запахи, привкусы
Окраска
Температура
Реакция
Минеральный состав
Растворенный кислород
Биохимическая потребность в кислороде
Возбудители заболеваний
Ядовитые вещества
Содержание взвешенных веществ не должно увеличиваться больше, чем на:
0,25 мг/л ( для I категории) и 0,75 мг/л (для II категории)
Для водоемов, содержащих в межень более 30 мг/л природных минеральных веществ, допускается увеличение взвешенных веществ в воде в пределах 5% Взвеси со скоростью выпадения более 0,4 мм/с для проточных водоемов и более 0,2 мм/с для водохранилищ к спуску запрещаются
На поверхности водоема не должны обнаруживаться плавающие пленки, пятна минеральных масел и скопление других примесей
Вода не должна приобретать запахи и привкусы интенсивностью более 2 баллов, обнаруживаемых:
непосредственно или при последующем │ непосредственно.
хлорировании.
Вода не должна сообщать посторонних запахов и привкусов мясу рыбы
Не должна обнаруживаться в столбике:
20см |10см
Летняя температура воды в результате спуска сточных вод не должна повышаться более, чем на 3°С по сравнению со среднемесячной температурой воды самого жаркого месяца года за последние 10 лет.
Не должна выходить за пределы 6,5—8,5 рН.
Не должен превышать по сухому остатку
1000 мг/л, в том числе хлоридов Нормируется по приведенному выше
350 мг/л и сульфатов 500 мг/л. показателю «Привкусы».
Не должен быть менее 4 мг/л в любой период года в
пробе, отобранной до 12 ч дня
Полная потребность воды в кислороде при 20°С не
должна превышать:
3,0 мг/л | 6,0 мг/л
Вода не должна содержать возбудителей заболеваний. Сточные воды, содержащие возбудителей заболеваний, должны подвергаться обеззараживанию после соответствующей очистки.
Отсутствие содержания в воде возбудителей заболеваний достигается путем обеззараживания биологически очищенных бытовых сточных вод до коли-индекса1 не более 1000 при остаточном хлоре не менее 1,5 мг/л.
Не должны содержаться в концентрациях, могущих оказать прямо или косвенно вредное влияние на здоровье населения.
1 Коли-индекс – число бактерий в 1 л воды.
Полностью замкнутый водооборотный цикл достигается сегодня при производстве фосфорной кислоты, аммофоса, едкого натрия, хлорида, а также в технологии целлюлозно-бумажного производства.
Контроль расхода воды стал осуществляться последние 10-15 лет и оценивается двумя коэффициентами:
1. Коэффициент оборота воды
Kо= Qо/(Qо+Qn+Qm), (3.54)
где Qо − расход оборотной воды; Qn − расход свежей воды; Qm − расход воды, поступающей вместе с материалами; среднее значение коэффициента Ко для машиностроительной промышленности равно 0,55, но существуют предприятия, на которых Ко = 0,75 − 0,96.
2. Коэффициент использования воды
Ки = (Qn+Qm− Qc)/(Qn+Qm), (3.55)
где Qc - вода, сбрасываемая в водоем.
Свойства сточной жидкости, определяющие методы ее очистки, зависят от степени дисперсности внутренней фазы. Если составляющие ее частицы имеют крупность меньше 1∙10-7 см, то дисперсная фаза образует истинный раствор (однофазную систему). Поскольку в любой точке объема истинного раствора концентрация вещества одинакова, растворы называют однородными, или гомогенными системами.
При крупности частиц больше 1∙10-5 см дисперсная фаза образует взвешенные вещества. К основным свойствам таких частиц относится их неспособность удерживаться во взвешенном состоянии, которая зависит от размера суспендированных частиц и интенсивности внешнего воздействия.
Состояние кинетической устойчивости наблюдается у частиц, диаметр которых близок или меньше 1∙10-5 см. Более крупные частицы теряют эту устойчивость и приобретают способность к осаждению или всплыванию, при этом частицы крупностью 1∙10-5 − 1∙10-4 см выделяются из воды весьма медленно. Частицы, имеющие степень дисперсности 1∙10-5 − 1∙10-7 см, образуют коллоидные растворы, причем частицы диаметром 1∙10-6 – 1∙10-7 см создают системы, свойства которых приближаются к истинным растворам, а частицы диаметром 1∙10-5 − 1∙10-6 см − к нерастворимым веществам.
Наиболее легко разделяются фазы в тех случаях, когда дисперсная фаза состоит из достаточно крупных частиц, размер которых превышает 1∙10-4 см. Такие частицы относятся к механическим примесям в воде.
Проблема очистка промышленных сточных вод (СВ) химического производства, металлургических, текстильных, целлюлозно-бумажных и машиностроительных предприятий, и особенно сельскохозяйственного использования, далека от своего решения.
В настоящее время находят широкое применение следующие способы очистки сточных вод: механический, физико-химический, химический и биохимический. Основным фактором при выборе метода обработки воды является фазовое состояние вещества.
Названные способы очистки подразделяются на рекуперационные и деструктивные: рекуперационные предусматривают извлечение из сточных вод и дальнейшую переработку ценных веществ; при деструктивных способах ЗВ подвергают разрушению путем окисления или восстановления. Продукты разрушения удаляют из воды в виде газов или осадков.
Механическая очистка служит для отделения нерастворенных веществ, размер которых больше 1∙10-4 см, путем процеживания, отстаивания, фильтрования и центрифугирования.
Для задержки различных веществ, плавающих на поверхности сточных вод (масел, жиров, нефти, смол и т. п.), служат различные сооружения: масло-, жиро -, нефте -, смолоуловители.
Во многих случаях сточные воды содержат мельчайшие частички, находящиеся во взвешенном состоянии, называемые суспензиями. Для их отделения прибегают к фильтрованию вод через специальные сетки или песчано-гравийные и шлаковые фильтры.
Процеживание предназначено для выделения из СВ механических примесей (dr³25 мм) вертикальными или наклонными решетками.
При эксплуатации решетки очищаются с помощью вертикальных и поворотных граблей, а при небольших расходах воды (Q< 4000 м3/ч) - вручную. Примеси, снятые с решеток, измельчаются и, в зависимости от их ценности, сбрасываются в поток СВ за решеткой или направляются на переработку. В настоящее время в основном используют решетки-дробилки РД-200, РД-900.
Отстаивание предназначено для выделения из СВ нерастворимых и частично коллоидных механических загрязнений минерального происхождения. Этот процесс основан на осаждении в жидкости твердых частиц.
Расчет отстойников СВ основывается на скорости осаждения (или витания) твердых частиц в жидкости, которая определяется из решения уравнения Стокса для движения сферической частицы в жидкости с учетом влияния силы гидравлического сопротивления, массовых сил и сил Архимеда (тяжести):
Uв= (gd2r/18)∙[(rr −rж)/mж] , (3.56)
где mж − динамический коэффициент вязкости жидкости; g − ускорение свободного падения; dr − диаметр частиц; rr, rж − плотность частиц и жидкости.
Отстаивание осуществляется в песколовках, отстойниках, жиро-нефте-смоло - и маслоуловителях. Песколовки применяют для задержания тяжелых нерастворимых примесей: песка (в стоках литейных цехов), окалины (отходы прокатных цехов) и т. д. со средним размером частиц до 250 мкм.
В зависимости от направления потока сточных вод песколовки делятся на: вертикальные, горизонтальные с прямолинейным и круговым движением воды, аэрированные − для разделения загрязнений по фракционному составу или плотности.
Некоторые из устройств водоочистки в виде принципиальных схем показаны на рис. 3.11. Здесь а) – радиальный отстойник; б) – песчано-гравийный фильтр; в) – песколовка; г) – ловушка для нефти.
Очистку сточных вод от механических примесей можно осуществить с помощью гидроциклона и центрифуги, в которых воде придается вращательное движение с выделением частиц взвеси.
Открытые гидроциклоны применяют для частиц со скоростью витания Uв > 0,02 м/с и используют для очистки СВ больших расходов, т. к. они отличаются малыми потерями напора.
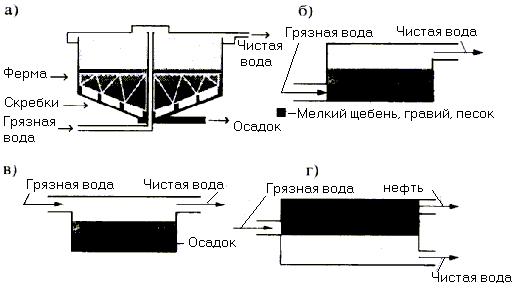
Рис. 3.11. Схемы устройств очистки воды
Для очистки частиц с Uв < 0,02 м/с используют напорные гидроциклоны (схема аналогична циклону для очистки воздуха от сухой неслипающейся пыли) и центрифуги. Промышленность использует напорные гидроциклоны НГЦ диаметром цилиндрической части 0,05−0,5 м.
Фильтрование СВ предназначено для очистки их от тонкодисперсных механических загрязнений в небольшой концентрации. Процесс фильтрования часто проходит 3 ступени: циклон, фильтр с металлической сеткой, а затем рукавный фильтр. Такую схему применяют на участках очистки воды от бериллия. Используются фильтры с зернистым слоем (песок, доломит, доменный шлак, керамические отходы, металлические опилки, отходы асбестового производства и др.), а также микрофильтры для тонкой очистки (барабанные или пластинчатые конструкции).
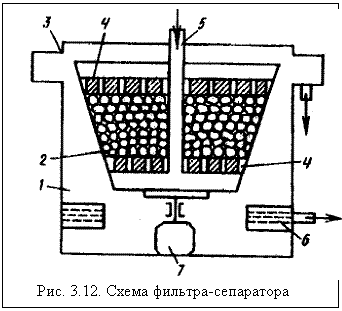
На рисунке 3.12 [3] показана схема фильтра-сепаратара с фильтрующей нагрузкой (например, из частиц пенополиуретана), предназначенного для очистки СВ от маслопродуктов и твёрдых частиц. Сточную воду по трубопроводу 5 подают на нижнюю опорную решётку 4. Затем вода проходит через фильтрующую нагрузку в ротор 2, верхнюю решётку 4 и очищенная от примесей переливается в приёмный кольцевой карман 6, затем выводится из корпуса 1. При концентрации маслопродуктов и твёрдых частиц до 0,5 кг/м3 эффективность очистки составляет соответственно 0,92 и 0,9, а время непрерывной эксплуатации фильтра 16−24 ч. Фильтрующая нагрузка может вращаться электродвигателем 7. В результате частицы пенополиуретана под действием центробежных сил отбрасываются к внутренним стенкам ротора, маслопродукты выжимаются, поступают в карманы 3 и направляются на регенерацию. Время полной регенерации фильтра 0,1 ч.
Очистка от примесей, содержащихся в сточных водах в небольшом количестве, производится отстаиванием, обработкой в гидроциклонах, флотацией и фильтрованием. Конструкции маслоловушек аналогичны конструкции горизонтального проточного отстойника с маслосборным устройством. Для очистки охлаждающих жидкостей, используемых на металлорежущих станках, применяют специальные реагенты, способствующие коагуляции загрязнений в эмульсиях (реагенты Na2CO3, H2SO4, NaCl, Al2(SO4)3 и др.).
 Механическую очистку применяют как предварительную при использовании других способов очистки.
Механическую очистку применяют как предварительную при использовании других способов очистки.
Химический и физико-химический способы применяют для очистки производственных сточных вод от коллоидных и растворенных веществ.
К основным химическим способам очистки относятся: окисление или восстановление загрязняющих воду веществ, нейтрализация с введением в сточные воды веществ с кислой или щелочной реакцией с целью обеспечения в них рН в пределах 6,5 − 8,5.
Во многих случаях загрязняющие вещества выделяются в виде осадков.
При физико-химической очистке используются следующие методы:
- коагулирование − введение в сточные воды веществ-коагулянтов, способствующих ускорению выделения из них нерастворенного и части растворенного загрязнения;
- адсорбция − добавление некоторых веществ, способных концентрировать на своей поверхности вещества, находящиеся в сточных водах;
- экстракция − введение в сточные воды вещества, не смешивающегося с ними, но способного растворять находящиеся в них загрязнения;
- флотация − пропуск через сточную воду воздуха, пузырьки которого при движении вверх захватывают загрязняющие воду вещества;
- эвапорация − пропуск через нагретую сточную воду водяного пара;
- ионитовый метод − фильтрование сточных вод через ионообменный материал, что обеспечивает удаление из воды катионов и анионов;
- электрохимический метод − инициирование различных химических реакций под воздействием электрического тока.
Выбор метода зависит от того, в каком состоянии находится вещество − в молекулярном или диссоциированном на ионы. Для веществ, находящихся в молекулярно-растворенном состоянии, могут быть использованы различные сорбенты (активированные угли, бентониты, диатомит, хлопья гидроксидов и т. д.), обработка воды окислителями (для веществ органического происхождения) и др.
При очистке воды от веществ, диссоциированных на ионы, используют методы, направленные на образование малорастворимых соединений, перевод токсичного иона в нетоксичные комплексы (например, перевод цианидов в ферроцианиды), образование малодиссоциирующих молекул (при взаимодействии водородных и гидроксильных ионов), извлечение из воды ионов (электродиализ), замену токсичных ионов безвредными (например, при Н+ и ОН--ионировании) и т. п.
В последнее время все большее применение получают такие методы физико-химической обработки воды, как экстракция, сорбция, ионный обмен, электродиализ, озонирование, электрохимическое окисление и восстановление, окисление под высоким давлением, выпаривание, сжигание, обработка воды ультразвуком, ультрафильтрация и обратный осмос (гиперфильтрация). Под влиянием ультразвука интенсивно протекают окислительные процессы трудно окисляющихся веществ.
Нейтрализация СВ на заводах ведется для удаления из них кислот (H2SO4, HCl, HNO3, H3PO4) и щелочей (NaOH, KOH), а также солей металлов, образованных на основе кислот и щелочей. В результате содержащиеся в воде ионы водорода Н+ и гидроксильная группа ОН - объединяются в молекулы воды.
В последние годы успешно разрабатывается метод окисления органических веществ при высоком (до сотен атмосфер) давлении и высокой (порядка тысячи градусов) температуре. Возможность утилизации выделяющейся при этом теплоты повышает экономическую рентабельность метода.
Перспективен метод окисления органических загрязнений производственных стоков озоном. Применение озона не связано с расходом привозных реагентов, производство его может быть организовано на месте при наличии озонаторной установки и электроэнергии. Для очистки промышленных сточных вод озон более удобен, чем другие окислители, включая активный хлор.
Производственные и бытовые стоки, прошедшие очистку, теряют часть содержащихся в них бактерий, однако их полное уничтожение возможно лишь с помощью дезинфекции, которая производится путем хлорирования, электролиза, использования бактерицидных лучей и т. д.
Биохимическая очистка базируется на способности некоторых микроорганизмов использовать для своего развития органические вещества, содержащиеся в сточных водах в коллоидном и растворенном состоянии. Этот способ применяют после того, как сточная вода очищена от минеральных и нерастворимых органических веществ. Он позволяет почти полностью удалить загрязнения органического происхождения. Биохимическая очистка производится в естественных условиях − на полях орошения, полях фильтрации или в биологических прудах, а также в искусственных условиях − в биологических фильтрах и аэротенках.
Использование полимеров в качестве загрузочного материала позволило существенно повысить эффективность биофильтров, при этом они могут работать и как самостоятельные биоокислители, и в различных комбинациях с аэротенками.
Биологическая (биохимическая) очистка сточных вод считается основной для обезвреживания органических примесей, в результате которой происходит очищение сточных вод вследствие способности микробов расщеплять, окислять и восстанавливать органические и некоторые минеральные соединения, содержащиеся в сточных водах. Этот процесс может происходить в естественных условиях (в реках, озерах, водохранилищах, а также в верхних слоях почвы) или в специальных очистных сооружениях (в аэротенках, окситенках и биофильтрах).
Схема аэротенка с принудительной подачей воздуха показана на рис. 3.13.
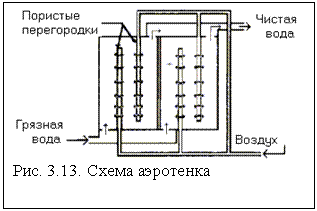 В СВ обычно содержится 150 – 200 мг/л взвешенных твёрдых частиц, 150 – 200 мг/л органического вещества (определяемого как биологическая потребность в кислороде) и 20−40 мг/л аммонийного азота.
В СВ обычно содержится 150 – 200 мг/л взвешенных твёрдых частиц, 150 – 200 мг/л органического вещества (определяемого как биологическая потребность в кислороде) и 20−40 мг/л аммонийного азота.
Биохимическое потребление кислорода (БПКt) – количество кислорода, потребное при биохимическом окислении содержащихся в воде веществ в аэробных условиях. БПК выражается в мг О2/л. Например: БПК5 – биохимическое потребление кислорода в течение 5 суток. БПК20 − биохимическое потребление кислорода в течение 20 суток; БПКпол − биохимическое потребление кислорода для полного окисления органики.
Пользуются также понятием «химическое потребление кислорода» (ХПК) – количество кислорода, потребное при химическом окислении содержащихся в воде органических и неорганических веществ под действием окислителей (выражается в мг О2/л).
Очистка СВ в аэротенке колеблется от 4 до 24 ч и более в зависимости от вида СВ, требуемой глубины очистки, типа процесса и отделения очищенной жидкости от частиц активного ила в отстойнике.
Частицы активного ила представляют собой флокулированную смесь бактерий и простейших. Как правило, из множества видов бактерий, находящихся в активном иле, выделяют только три основные группы: углеродокисляющие флокулообразующие бактерии, углеродокисляющие нитчатые бактерии и бактерии-нитрификаторы. Флокулообразователи способствуют быстрому осаждению ила в отстойнике, а нитрификаторы превращают аммонийный азот в нитраты:
NH3 + O2 ® NO2‾, NO2‾ +O2 ® NO3‾.
Продолжительность ta (в часах) аэрации СВ в аэротенке оценивается по формуле:
tа = (La - Lt) / [а (1 − S) r], (3.57)
где La и Lt – БПКt исходной и очищенной СВ; а − доза активного ила, г/л; доля зольности примесей S = 0,3÷0,35; r − средняя удельная скорость окисления загрязнений, мг/(г. ч).
Некоторые значения r для заданных величин La, Lt, а приведены таб. 3.16. Для Lа< 500 мг/л применяют аэротенки с сосредоточенной подачей смеси СВ и активного ила в начале сооружения.
При отсутствии данных о средней удельной скорости окисления можно использовать формулу:
r = rm Lt CО /[(Lt CО + Ko Lt + K1CО ) (1 + j a)] , (3.58)
где CО − концентрация растворенного кислорода, мг/л; rm − максимальная скорость окисления загрязнений, равная 85 мг/(г. ч); Ko=0,5 − константа для кислорода; K1 - константа БПК (для городских СВ K1=33); j − коэффициент ингибирования (для слабо концентрированных СВ j = 0,07 л/г).
Таблица 3.16. Средние удельные скорости окисления загрязнений
БПКполн исходной воды, мг/л
БПКполн очищенных сточных вод Сt, мг/л
15
29
25
30
40
50 и более
При а £ 1,8 г/л
100
200
20
22
22
24
24
28
27
32
35
42
47
57
При а > 1,8 г/л
150
200
300
400
500
18
20
22
23
24
21
23
26
28
29
23
26
30
33
35
26
29
34
38
41
35
37
44
53
58
45
50
60
73
82
Время пребывания органического вещества в аэротенке связано с нагрузкой Р на ил выражением [32]:
Р = La Q / (a Wa) = La / (a ta) , (3.59)
где Q − расход СВ, м3/сут; Wa − объем аэротенка, м3.
Существуют три основных типа процессов очистки: быстрая (Р = 0,5÷5), стандартная (Р = 0,25÷0,45) и продленная (Р = 0,05÷0,2) аэрация.
Продленный тип аэрации обеспечивает весьма высокие качества выходного стока: полная нитрификация; БПК < 10 мг/л; концентрация взвешенных частиц меньше 10 мг/л; аммонийного азота меньше 5 мг/л. Стандартная аэрация позволяет обеспечить качество стока от полной нитрификации на нижней границе интервала до отсутствия нитрификации на его верхней границе. Быстрый тип аэрации делает возможным увеличить скорость удаления БПК на единицу массы ила; качество выходного стока может быть выше в среднем в 20−30 раз при достаточной подаче кислорода.
Устанавливая нагрузку органики на ил в сутки, рекомендуется принимать рабочую концентрацию иловой смеси в пределах 1,5−5 г/л. Выбор этой величины зависит от типа СВ и от возраста tи ила, определяемого по формуле:
tи = a Wa / ( mу + Q Ct) , (3.60)
где mу − количество удаляемого ила, кг/сут; Ct − концентрация ила в выходном стоке, кг/м3.
Управляя скоростью отвода ила, можно управлять нагрузкой по органическому веществу − главным параметром, влияющим на качество выходного стока.
Рабочая концентрация растворенного кислорода вычисляется на основе расчетной потребности установки. Для полной нитрификации следует выбирать СО ³ 2 мг/л, а для других целей (окисление углерода, денитрификация) достаточны меньшие значения.
Величина
СО =103 R/Q , (мг/л) , (3.61)
где R (кг/сут) − суточная потребность в кислороде для окисления углерода в установке со стандартной нагрузкой вычисляется по формуле:
R = 0,75 La + 0,048 a Wа. (3.62)
Здесь параметры имеют размерность: La (г/л), а (г/л), Wа (м3).
Для систем продленной аэрации, содержащих не осевший ил, значение
R = La + 4,34 NNН3 + 2,85 Nо + 0,024 Wа r q (t-20) , (3.63)
где NNНЗ и Nо - количество удаляемого в сутки азота аммонийного и общего соответственно, кг/сут; r - скорость эндогенного дыхания, принимается равной 3,9 мг О2 / (гила. сут); q = 1,07; t - температура жидкости, ˚С.
Отношение количества кислорода, требуемого для обработки 1 м3 СВ, к количеству кислорода, используемого с 1 м3 подаваемого воздуха, определяется по формуле
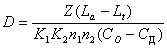 , (3.64)
, (3.64)
где D − удельный расход воздуха при аэрации; Z − удельный расход кислорода, мг/мг БПКп (при неполной очистке Z= 0,7÷0,9; при полной Z=1÷1,2; при нитрификации Z=1,5÷2,4); К1 − коэффициент, учитывающий тип аэрации (по размеру пузырька), для мелких пузырьков является функцией отношения площади, занятой аэраторами, к площади зеркала воды; К2 − коэффициент, учитывающий глубину погружения аэратора; n1 − коэффициент, учитывающий температуру (среднемесячную) СВ (n1 = 1+0,02(Тср-20)); n2 − коэффициент, учитывающий скорость переноса кислорода в иловой смеси к скорости переноса его в чистой воде (n2 = 0,5-0,8); Сд - допустимая минимальная концентрация кислорода в СВ, которая не лимитирует скорости окислительного процесса (принимается равной 2 мг/л); СО − растворимость кислорода воздуха в воде (мг/л) в зависимости от высоты Р (м) столба воды над аэратором:
СО = ОТ(10,3+0,5 Р)/ 10,3 (3.65)
Здесь ОТ − растворимость кислорода воздуха в СВ в зависимости от температуры:
ОТ = [468/(31,6+Т)]∙b [мг/л], (3.66)
где Т − температура СВ (˚С), а газовая фаза − воздух под давлением 0,1 МПа; b − коэффициент, учитывающий загрязнение воды, равный 0,7−0,9.
Общий объем (м3) аэрационной части равен
Wa = ![]() ta /
ta /
Суммарная площадь проектных аэротенков равна
F = W / H. (3.68)
Типовые аэротенки имеют длину L = 49,15 м, ширину b = 15м и глубину Н = 3м.
Потребное количество аэротенков определяется по формуле:
N = W / (n H L b), (3.69)
где n − количество коридоров аэротенка.
Для выделения из СВ взвешенных веществ применяют первичные (до аэротенка) отстойники, в которых под действием гравитационных сил происходит выпадение осадка на дно отстойника. Основная масса взвешенных частиц выпадает в осадок в течение tот=1,5 ч отстаивания. При расходах СВ до 10000 м3/сут применяют вертикальные отстойники. При расходах ![]() ³ 10000 м3/сут применяют горизонтальные или радиальные отстойники с диаметром 18−54 м.
³ 10000 м3/сут применяют горизонтальные или радиальные отстойники с диаметром 18−54 м.
Продолжительность tот нахождения СВ во вторичном вертикальном отстойнике рекомендуется выбирать из условия, когда скорость осаждения ила больше скорости восходящего потока воды, равной ~ 0,1 мм/с. Можно принять tот » 2 ч, поскольку эффект осветления СВ через 2 ч достигает значения более 99%. Применение флокулянтов позволяет уменьшить время tот.
Объем отстойника равен
Wот = ![]() tот /
tот /
Степень очистки СВ определяется по формуле
h = ((La - Lt)/ La) ∙ 100% . (3.71)
Практика эксплуатации аэротенков показала, что нестабильность сброса сточных вод затрудняет их обработку по технологиям, обусловленным стационарностью рабочих режимов и постоянством концентраций лимитирующего субстрата и биомассы.
Для анализа непрерывной очистки СВ активным илом с учетом вторичного отстойника и рециркуляции биомассы используется уравнение материального баланса в виде:
для лимитирующего фактора
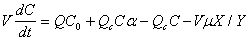
![]() (3.72)
(3.72)
и для биомассы
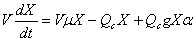 . (3.73)
. (3.73)
Здесь С − концентрация субстрата, С0 − начальная его концентрация; a − доля выходного стока из биореактора, которая подвергается рециркуляции; m − удельная скорость роста бактериальной биомассы с концентрацией Х, измеренная по сухому веществу; Qc − расход жидкости из биореактора; g − коэффициент, учитывающий концентрацию биомассы в отстойнике; Y − коэффициент выхода бактериальной биомассы при гетеротрофном росте на источнике углерода и энергии:
![]() . (3.74)
. (3.74)
На рис.3.14 показана схема проточного биореактора непрерывного действия, работающего в режиме полного смешения, с отстойником и рециркуляцией сконцентрированной микробной биомассы.
Расход жидкости из биореактора Qc связан с потоком жидкости Q в реактор уравнением:
Qc = Q (1−a). (3.75)
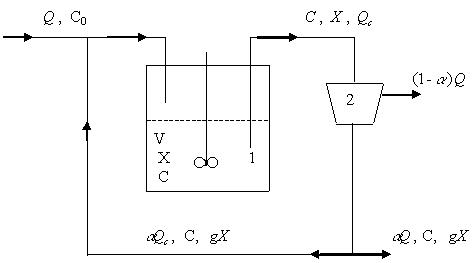
Рис.3.14. Схема проточного биореактора;1–биореактор; 2–отстойник
Зависимость между удельной скоростью роста биомассы и концентрацией лимитирующего субстрата выражается уравнением Моно:
m = mm С/(С+КC), (3.76)
где mm − максимальное значение субстратной составляющей m, когда концентрация кислорода С много больше КC − константы насыщения по кислороду (константы Моно); КC=С, когда m=0,5mm.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 |



