Между частотой обнаружения неполной кишечной метаплазии и стадией хронического гастрита была выявлена прямая сильная корреляционная связь (rs=0,78, р=0,003). Изолированно для неполной кишечной метаплазии типа III тоже обнаружена прямая корреляционная связь средней силы (rs=0,56, р=0,012) между частотой встречаемости кишечной метаплазии типа III и стадией хронического гастрита. Это совпадает с характером корреляционной связи между аналогичными параметрами в группе H. pylori-ассоциированного хронического атрофического гастрита. Иначе говоря, при длительной персистенции гастроинтестинального фенотипа, о чем свидетельствует формирование кишечной метаплазии типа III (Tsukamoto T. et al., 2006), параллельно нарастают атрофические изменения, то есть стадия хронического гастрита.
В клетках железистого желудочного эпителия обнаруживали фокусы экспрессии CDX-2 значительно чаще, чем в других ранее описанных группах: экспрессия маркера в желудочном эпителии вне зоны опухоли была выявлена в 86% случаев рака желудка кишечного типа, из них в 74% исследованных фрагментов слизистой оболочки антрального отдела и в 32% исследованных фрагментов слизистой оболочки тела желудка.
При раке желудка диффузного типа преобладал антрум-гастрит с наличием фокусов атрофии при преобладании полной тонкокишечной метаплазии. При этом не установлено различий в пролиферативной активности между метаплазированным эпителием и желудочным. Экспрессия Р53 в клетках желудочного эпителия и в участках кишечной метаплазии была выявлена в 7 случаях из 18.
Основным фенотипом хронического гастрита при раке желудка кишечного типа, в отличие о язвы желудка, является атрофический пангастрит с увеличением уровня экспрессии Р53 в мукоцитах и метаплазированном эпителии, что, возможно, предшествует развитию дисплазии/неоплазии при эволюции атрофического пангастрита. При раке желудка диффузного типа подобная перестройка слизистой оболочки отсутствует.
Закономерности морфогенеза атрофических изменений слизистой оболочки желудка
При обсуждении вопроса о морфогенезе атрофии слизистой оболочки желудка необходимым является учет условий формирования дефицита желез и изменения программы дифференцировки клеток с развитием метаплазии (рис. 4). При H. pylori-позитивном хроническом поверхностном антрум-гастрит после повреждения пилорических желез цитокинами воспалительного инфильтрата происходит абсолютное уменьшение числа, объема желез и/или замещение специализированных клеток в них метаплазированным эпителием. Дефицит пилорических желез, возникающий вследствие дисбаланса между регенераторной пролиферацией и апоптозом эпителиальных клеток, превращает поверхностный антрум-гастрит в атрофический антрум-гастрит (, 2008).
Процесс формирования кишечной метаплазии и, следовательно, метапластической атрофии, обеспечивается работой гена cdx-2, функционирующего как антионкоген в условиях повышенной пролиферативной активности в генеративном компартменте, обеспечивающей репарацию эпителиального покрова (Barros R. et al., 2010; Martin J et al., 2010), именно в данной зоне первоначально локализуется экспрессия CDX-2 клетками желудочного эпителия.
При длительной H. pylori-колонизации антрального отдела желудка возникает индукция гипергастринемии сигнальными молекулами H. pylori и воспалительными цитокинами ( и соавт., 2008; Peek R. et al., 2008; Takaishi S. et al., 2009). Эта гипергастринемия приводит в течение 10-20 лет к «истощению» функции париетальных клеток в теле желудка (Malferteiner P. et al., 2008; Weis V. G. et al., 2009). Происходит уменьшение выработки соляной кислоты, что увеличивает рН в просвете желудка и вызывает миграцию бактерии в тело желудка. Колонизация слизистой

![]()
![]() Рис. 4. Гипотетическая схема, отражающая направления морфогенеза атрофии слизистой оболочки желудка при хроническом гастрите, хронической язве желудка, раке желудка кишечного типа.
Рис. 4. Гипотетическая схема, отражающая направления морфогенеза атрофии слизистой оболочки желудка при хроническом гастрите, хронической язве желудка, раке желудка кишечного типа.
Условные обозначения: – снижение или повышение экспрессии.
оболочки тела желудка H. pylori индуцирует в ней воспаление. Формируется хронический гастрит тела.
Гибель париетальных клеток за счет апоптоза, индуцированного цитокинами клеток воспалительного инфильтрата, приводит к еще большему снижению секреции соляной кислоты и возрастанию рН просвета желудка, что может являться триггером экспрессии кишечного фактора транскрипции CDX-2 в желудочном эпителии (Jeong M. S. et al., 2009; Stairs D. B. et al., 2010). Параллельно в качестве ответной реакции на повреждение желудочного эпителия происходит повышение экспрессии желудочного фактора транскрипции – Shh в покровно-ямочном эпителии и появлением экспрессирующих Shh муцинпродуцирующих клеток в зонах пилорической метаплазии тела желудка. Пилорическая метаплазия также характеризуется широким распространением в фундальных железах желудочного муцина MUC6.
Кишечный фактор транскрипции – CDX-2 появляется в клетках генеративных зон слизистой оболочки тела желудка и приводит к развитию кишечной метаплазии. Так формируется мультифокальный атрофический гастрит: наличие участков атрофии (метапластической атрофии) слизистой оболочки в антральном отделе и теле желудка.
Экспрессия CDX-2 в ядрах мукоцитов на этой форме-стадии эволюции хронического гастрита приводит к появлению так называемого гастроинтестинального фенотипа слизистой оболочки. Этот фенотип характеризуется тем, что между CDX-2-позитивными бокаловидными клетками, синтезирующими кишечный муцин MUC2 и желудочный муцин MUC5AC, располагаются цилиндрические CDX-2-позитивные и CDX-2-негативные клетки с экспрессией MUC5AC и наличием гистохимически определяемых сиало - и нейтральных муцинов. Фенотипически это выглядит как неполная кишечная метаплазия. Бокаловидные клетки содержат преимущественно сиаломуцины, располагаются между цилиндрическими клетками, слизь в которых имеет синий или красный цвет в зависимости от преобладания выявляемых гистохимически сиало - или нейтральных муцинов.
При повышении экспрессии CDX-2 кишечная метаплазия становится полной, то есть исчезает экспрессия желудочного муцина MUC5AC в цилиндрических клетках, в них появляется щеточная каемка, и в них же исчезает экспрессия Shh.
При снижении экспрессии CDX-2 фенотип эпителия продолжает оставаться смешанным – неполная кишечная метаплазия с появлением в цилиндрических клетках гистохимически выявляемых сульфомуцинов. Такой тип кишечной метаплазии чаще обнаруживается при длительно существующих атрофических изменениях слизистой оболочки желудка и более характерен для атрофического пангастрита, который, вероятно, является дальнейшим этапом эволюции мультифокального атрофического гастрита. Хотя и не всегда. И на этот счет нет единого мнения (El-Zimaiti H. et al., 2008; Vannella L. et al., 2010).
При атрофическом пангастрите нарастает экспрессия Р53 в клетках желудочного и, особенно, цилиндрического метаплазированного эпителия. В желудочном эпителии повышается уровень экспрессии кишечного фактора транскрипции CDX-2, снижается экспрессия желудочных муцинов MUC5AC и MUC6. Снижается экспрессия Shh в участках полной кишечной метаплазии. Повышается уровень экспрессии Shh в желудочном эпителии и в участках неполной кишечной метаплазии, причем гиперэкспрессия белка на данном этапе может отражать появление клеточной линии интенсивно регенерирующего эпителия с высоким индексом пролиферации.
Интересно, что уровень экспрессии Р53 с учетом использованных в нашем исследовании антител как к «дикому» так и мутантному его вариантам может являться маркером, косвенно отражающим давность повреждения ДНК. Высокий уровень экспрессии Р53 более характерен для наличия долгоживущего (имеющего больший по сравнению с «диким» период полураспада) мутантного варианта гена р53, ассоциированного с накоплением мутаций и формированием «стартовой площадки» опухолевого роста (Zhang Y. et al., 2010; Sugai T. et al., 2010). Однако, целиком рассматривать группу атрофического пангастрита как факультативный предрак не представляется возможным в силу высокой гетерогенности показателей, отражающих клеточное обновление эпителия слизистой оболочки желудка (табл. 5). При атрофическом пангастрите отмечается наличие высокого уровня экспрессии не только Р53 и маркера пролиферации Ki-67, но и Cpp32 – каспазы-3 – эффекторного фермента апоптоза. Вероятно, условиям такой «стартовой площадки» будут отвечать отдельные случаи с высоким темпом пролиферации и наличием повреждений ДНК (экспрессия Р53) при сравнительно низком уровне апоптоза мукоцитов слизистой оболочки желудка.
Ассоциация стадии хронического гастрита (распространенность и выраженность атрофии) с раком желудка кишечного типа
При применении разработанной визуально-аналоговой шкалы для оценки стадии хронического гастрита у пациентов с наличием H. pylori-ассоциированного хронического атрофического гастрита (при расчете исключены данные пациентов с поверхностным антрум-гастритом) наиболее часто встречалась II стадия хронического гастрита – 34,4% (рис. 5). Стадии I и III встречались с частотой 24,4% и 25,2% соответственно. В 16,0% случаев была обнаружена стадия IV хронического гастрита. Стадии III и IV суммарно встречались в 41,2% случаев.
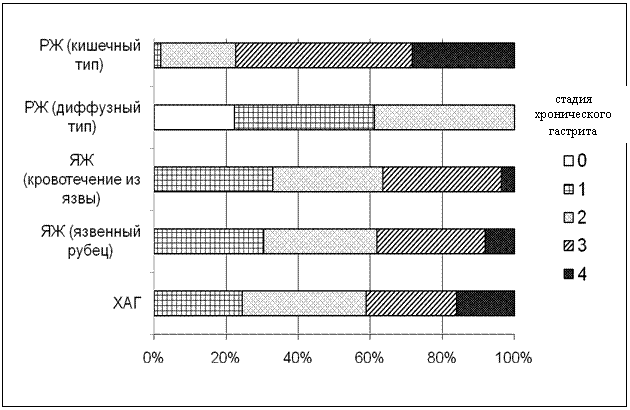
Рис.5. Диаграмма, отражающая соотношение стадий хронического гастрита (0-IV) в исследованных группах.
Сокращения: РЖ – рак желудка, ЯЖ – язва желудка, ХАГ – хронический атрофический гастрит.
Доля больных раком желудка кишечного типа со стадиями хронического гастрита III и IV составила 77,4%. Стадия I хронического гастрита была обнаружена только у одного больного раком желудка кишечного типа. Отсутствия атрофических изменений в слизистой оболочке (стадия 0) у больных раком желудка кишечного типа обнаружено не было.
В группе больных раком желудка диффузного типа преобладали стадии I и II хронического гастрита с общей частотой 77,8%. В 22,2% случаев слизистая оболочка желудка у больных раком желудка диффузного типа характеризовалась отсутствием атрофических изменений, что соответствовало стадии 0 хронического гастрита. Стадий III и IV хронического гастрита у данных больных обнаружено не было. Данное обстоятельство отражает различие канцерогенеза двух основных вариантов рака желудка: этапное нарастание атрофических изменений в слизистой оболочке желудка с возрастанием риска развития рака кишечного типа (P. Correa, 1991, 2008; и соавт., 2007; , 2009; Graham D. et al., 2010) и быстрое развитие рака диффузного типа без предварительной перестройки эпителия и атрофии желез (Vauhkonen M. et al., 2006; Shibata T. et al., 2010).
Достоверные значения коэффициента корреляции средней и умеренной силы между стадией хронического гастрита и возрастом больных были обнаружены в группах больных хроническим атрофическим гастритом и раком желудка кишечного типа (rs=0,67, p=0,004 и rs=0,45, p=0,001 соответственно).
Между группами пациентов с наличием язвы желудка с кровотечением и с язвенным рубцом не было обнаружено статистически достоверных различий по соотношению стадий хронического гастрита (р=0,34). В обеих группах встречались больные со стадиями хронического гастрита от I до IV. Чаще обнаруживались стадия II и III. Был обнаружен достаточно высокий процент больных с наличием стадии III и IV. Суммарная доля этих стадий в группе больных язвой желудка с кровотечением из язвы и с рубцеванием язвы составила 36,1% и 38,2% соответственно. Сопоставимая доля стадий III и IV хронического гастрита при язве желудка наблюдалась и в японской популяции (Satoh K. et al., 2008). Достаточно высокий удельный вес стадии III и IV хронического гастрита у больных язвой желудка, по-видимому, указывает на возможность развития у них рака желудка кишечного типа, что, например, показано в пролонгированном исследовании (Mabe K. et al., 2009).
Ассоциацию между формами атрофического гастрита и риском развития рака кишечного типа или язвы желудка удобно продемонстрировать на рисунке 6, где представлены детали морфогенеза метапластической атрофии, с отнесением неполной кишечной метаплазии с увеличением экспрессии Р53 в сторону риска развития рака желудка кишечного типа. На схеме отражена возможность развития как язвы так и рака желудка при мультифокальном атрофическом гастрите, что важно учитывать при организации пролонгированного наблюдения за пациентами по результатам биопсийного исследования.
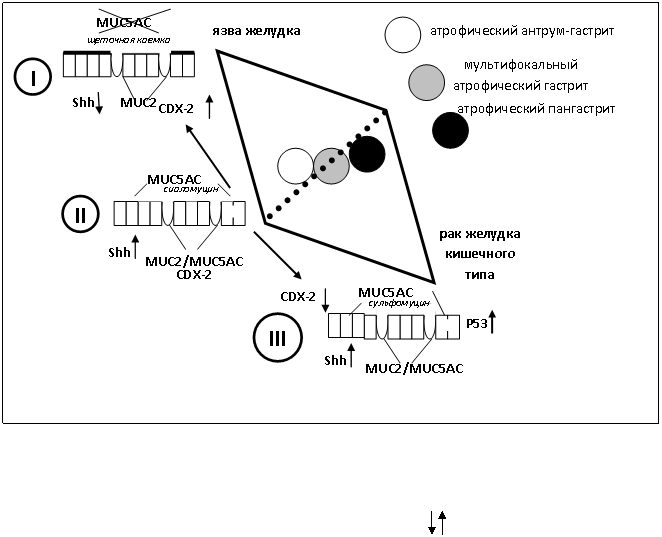
Рис. 6. Ассоциация риска развития язвы желудка и рака желудка кишечного типа с морфологическими формами хронического атрофического гастрита; отражены молекулярно-биологические события, обеспечивающие морфогенез метапластической атрофии.
Условные обозначения: I-III – тип кишечной метаплазии. – снижение или повышение экспрессии.
Определение уровня атрофии слизистой оболочки с помощью визуально-аналоговой шкалы как интегральная оценка риска развития рака желудка кишечного типа и ее воспроизводимость
На рисунке 7 кратко представлен морфогенез атрофии слизистой оболочки желудка, включающий основные механизмы: абсолютная атрофия и гиперпролиферативная метапластическая атрофия. Вероятно, при хроническом гастрите параллельно имеет место последовательная смена его фенотипа и изученных нами морфогенетических вариантов атрофии, что ассоциировано на определенных этапах с риском развития язвы или рака желудка кишечного типа.
Основы такого подхода с ассоциацией между морфологическими изменениями слизистой оболочки желудка и прогностической оценкой «рак – язва», изложенные (1998) позволяют определить пациентов с хроническим гастритом, входящих в контингент риска развития рака желудка кишечного типа или хронической язвы желудка.
Изученные в нашем исследовании особенности морфогенеза хронического атрофического гастрита с раздельным рассмотрением форм-фенотипов хронического гастрита и соответствующих им механизмов развития атрофии слизистой оболочки желудка дополняют существующие представления. А идентификация стадии хронического гастрита, оцениваемой по разработанной визуально-аналоговой шкале, фактически представляет собой практический «инструмент» более четкого выделения групп риска (III-IV стадия) и обеспечения персонификации вторичной профилактики и патоморфологического мониторинга риска развития рака желудка кишечного типа.
 |
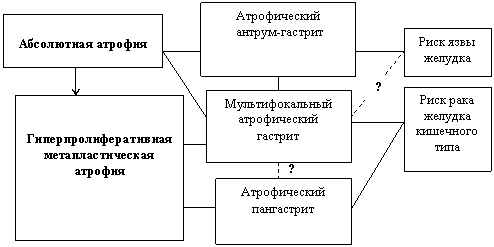 |
Рис. 7. Гипотетическая схема, отражающая хронологическую последовательность смены фенотипических вариантов и стадии хронического гастрита с обозначением ведущих механизмов атрофии и ассоциаций с риском развития хронической язвы желудка и рака желудка кишечного типа.
В оценке разработанной визуально-аналоговой шкалы (рис. 2) мы рассчитывали воспроизводимость метода (согласие: метод/наблюдатель), с постановкой вопроса: получают ли несколько наблюдателей-экспертов одинаковые результаты, применяя один метод? При этом наша оценка системы OLGA и предлагаемой визуально-аналоговой шкалы на материале биопсий, подготовленных для пересмотра российскими патологами-экспертами* при расчете взвешенной каппы Коэна характеризовалась значением коффициента k=0,71, что соответствует хорошей степени согласованности. Полагаем, что это позволяет использовать созданную шкалу, как минимум, в качестве альтернативы достаточно громоздкой системе OLGA, а также позволяет сопоставлять данные, полученные при использовании системы OLGA, и разработанной нами шкалы.
За основу подхода по созданию пересмотра мы положили условия, сходные с принципами работы группы Atrophy Club. Однако, имелись важные отличия. В качестве первичного материала анализа экспертами Atrophy Club оценивалась не градация атрофии, а сам факт ее наличия с бинарным значением анализируемого показателя (есть атрофия/нет атрофии) в микропрепаратах: 48 препаратов с серийными срезами гастробиоптатов из антрального отдела, тела и угла желудка с окраской гематоксилином и эозином и ШИК-реакцией в сочетании с альциановым синим при рН=2,5. В нашей работе на первом (заочном) этапе оценивалась именно градация атрофии в микрофотографиях, а на втором (очном) проводили оценку интегрального показателя стадии хронического гастрита по 14 сериям препаратов – клиническим случаям при наличие 4-5 биоптатов от каждого пациента (65 препаратов) при альтернативном, а не совместном использовании аналогичный окрасок гистологических срезов.
________________________________________________________________
*– работа экспертов проходила в период проведения III съезда Российского общества патологоанатомов (26–30 мая 2009 года, Самара). Имеются рекомендации съезда использовать предложенную нами визуально-аналоговой шкалу в качестве «инструмента» рабочей классификации хронического гастрита, что нашло отражение в резолюции съезда (пункт 6).
Сравнивать значения критерия согласия – k, при разных исследованиях даже при существовании минимальных отличий трудно, поскольку значение коэффициента сильно зависит от числа исследователей-экспертов, и, особенно, от числа категорий – чем больше значений показателя, тем ниже может быть критерий согласия (Landis J. R., Koch G. G., 1977; Feinstein A. R, Cicchetti D. V., 1990; Morris J. A., 1994; van der Wulp H. et al., 2009).
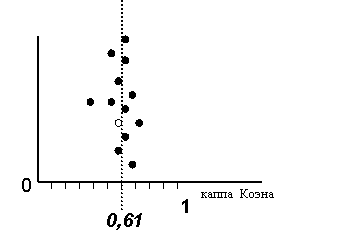
Итоговый показатель работы Международной группы Atrophy Club с оценкой градации атрофии составил k=0,73 (gge et al., 2002), что вполне сопоставимо с результатами заочного (k=0,61 – хорошая степень согласованности) и очного (k=0,5 – умеренная степень согласованности) этапов работы отечественных экспертов (рис. 8, 9).
Меньшие значения критерия согласия, полученные в нашей работе, являются вполне закономерными, поскольку при работе экспертов российской группы использовалась оценка воспроизводимости именно стадии гастрита как интегрального показателя, то есть имело место большее количество категорий, чем у экспертов Atrophy Club. Примечательно, что разброс индивидуальных значений k (диагностическая вариабельность) был в наших и зарубежных исследованиях сопоставимым.
На очном этапе работы былы устранены «выбросы» – два значения с индивидуальными показателями экспертов k=0,131 и k=0,275 (при их парном сопоставлении k=0,07). Подобные отличия индивидуальных показателей экспертов обычно отражают плохую согласованность исследователей при методических нарушениях в их работе (эксперт не следует общим техническим рекомендациям) и поэтому должны быть исключены из анализа (Tooth L. R. et al., 2004; Sim J. et al., 2005).
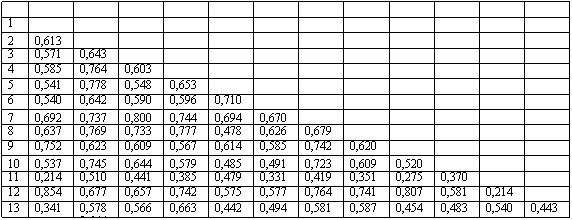 |
 Рис. 8. Значения индивидуальных показателей каппа-статистики при парном сопоставлении результатов работы экспертов на заочном этапе Российского пересмотра Международной классификации хронического гастрита с использованной разработанной визуально-аналоговой шкалы градации атрофии. На графике отражен разброс суммарных усредненных значений (медиана) каждого эксперта и конечный результат – значение капы Коэна.
Рис. 8. Значения индивидуальных показателей каппа-статистики при парном сопоставлении результатов работы экспертов на заочном этапе Российского пересмотра Международной классификации хронического гастрита с использованной разработанной визуально-аналоговой шкалы градации атрофии. На графике отражен разброс суммарных усредненных значений (медиана) каждого эксперта и конечный результат – значение капы Коэна.
|
1 патолог (0,440) | ||||
|
2 патолог (0,612) |
0,652 | |||
|
3 патолог (0,500) |
0,387 |
0,370 | ||
|
4 патолог (0,460) |
0,419 |
0,615 |
0,500 | |
|
5 патолог (0,501) |
0,440 |
0,609 |
0,571 |
0,364 |
Рис. 9. Значения индивидуальных показателей каппа-статистики при парном сопоставлении результатов работы экспертов на очном этапе Российского пересмотра Международной классификации хронического гастрита с использованной разработанной визуально-аналоговой шкалы градации атрофии. На графике отражен разброс суммарных усредненных значений (медиана) каждого эксперта и конечный результат – значение капы Коэна.
Таким образом, установленные особенности клеточного обновления эпителия слизистой оболочки желудка, отражающие морфогенез атрофии при различных фенотипических вариантах хронического гастрита, позволяют обосновать выявленную ассоциацию гиперпролиферативной метапластической атрофии в условиях атрофического мультифокального и, преимущественно, пангастрита (стадия III-IV) с раком желудка кишечного типа. Достигнутый уровень согласия при оценке атрофических изменений слизистой оболочки желудка с помощью предложенной нами визуально-аналоговой шкалы обеспечивает достаточный уровень воспроизведения результата и позволяет считать приемлимым широкое использование Российского варианта пересмотра Международной классификации хронического гастрита в патологоанатомической практике в качестве удобного «инструмента» обеспечения патоморфологического мониторинга риска развития рака желудка кишечного типа.
Выводы
1. При атрофическом антрум-гастрите замещение специализированного эпителия реализуется как полная кишечная метаплазия при отсутствии достоверных различий в пролиферативной активности между метаплазированным и желудочным эпителием. При атрофическом мультифокальном гастрите появляются очаги пролиферирующего метапластического эпителия – гиперпролиферативная метапластическая атрофия. При атрофическом пангастрите гиперпролиферативная метапластическая атрофия сочетается с нарастающей экспрессией Р53.
2. Атрофический антрум-гастрит характеризуется преобладанием абсолютного уменьшения объема желез – абсолютная атрофия. При мультифокальном атрофическом гастрите абсолютная атрофия – убыль специализированных желез и клеток сочетается с гиперпролиферативной метапластической атрофией. При атрофическом пангастрите гиперпролиферативная метапластическая атрофия доминирует.
3. Экспрессия кишечного фактора транскрипции CDX-2 является маркером формирования гастроинтестинального фенотипа – неполной кишечной метаплазии с продукцией кишечного MUC2 и желудочного MUC5AC муцинов бокаловидными клетками. Максимальная экспрессия CDX-2 цилиндрическими каемчатыми и бокаловидными клетками имеет место при полной кишечной метаплазии в сочетании с утратой продукции MUC5AC и снижением экспрессии Shh цилиндрическими клетками, продукцией MUC2 бокаловидными клетками.
4. Неполная кишечная метаплазия III типа прямо коррелирует с распространенностью атрофических изменений слизистой оболочки желудка. В условиях недостаточного объема биопсийного материала наличие данного типа метаплазии в биоптате (биоптатах) может служить «суррогатным» маркером распространенной атрофии слизистой оболочки желудка.
5. Хронической язве желудка соответствуют фенотипы либо атрофического антрум-гастрита (особенно при низких пилорических язвах), либо реже – мультифокального атрофического гастрита с доминированием атрофии в антральном отделе желудка при высоком уровне апоптоза железистого эпителия и снижением уровня продукции протекторного муцина MUC5AC при обострении язвы.
6. С раком желудка кишечного типа преимущественно ассоциирована гиперпролиферативная метапластическая атрофия в условиях атрофического пангастрита и редко – мультифокального атрофического гастрита (стадия III-IV хронического гастрита). Характерно увеличение распространенности неполной кишечной метаплазии, возрастание экспрессии Р53 и снижение продукции протекторных желудочных муцинов MUC5AC и MUC6.
7. Использование разработанной визуально-аналоговой шкалы оценки атрофии слизистой оболочки желудка (стадии 0-IV хронического гастрита) обеспечивает достаточно высокий уровень воспроизведения результата в практике патологоанатомического исследования.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Особенности атрофии слизистой оболочки желудка при H. pylori-ассоциированном гастрите у молодых пациентов с дисплазией соединительной ткани / , , и др. // Педиатрия№2. – Приложение. - С.72–74.
2. Мозговой Helicobacter pylori: возможность обратного развития атрофии слизистой оболочки желудка и персистенция воспалительного инфильтрата / , // Экспериментальная и клиническая гастроэнтерология. – 2004. – Вып. 1 (Внеочередной). – С. 101–114.
3. Кишечная метаплазия слизистой оболочки желудка: классификация, методика детекции и сложности гистопатологической интерпретации с позиций современной практической гистохимии / , , // Экспериментальная и клиническая гастроэнтерология. – 2004. – Вып. 1 (Внеочередной). – С. 114–126.
4. Качество жизни и клинические варианты течения хронического гастрита в постэрадикационный период / , , и др. // Экспериментальная и клиническая гастроэнтерология. – 2004. – Вып. 1 (Внеочередной). – С. 134–137.
5. Ливзан -хеликобактерный гастрит: неологизм или клиническая реальность? / , , // Экспериментальная и клиническая гастроэнтерология– № 6. – С. 48–61.
6. Ливзан и безопасность тройной терапии Helicobacter pylori-ассоциированной язвенной болезнью / , , // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. – 2004. – № 4. – С. 25–29.
7. Обратное развитие морфологических признаков при основных вариантах хронического гастрита в условии эрадикации Helicobacter pylori / , , и др. // Арх. патол. – 2005. – Вып. 3. – С. 17–21.
8. Заводиленко клеточного обновления в очагах кишечной метаплазии эпителия желудка при атрофии и эрозивно-язвенных дефектах / , , // Омский научный вестник. – 2006. – Специальный выпуск. – №3(37), Ч. II. – С.42–47.
9. Лининг пролонгированная оценка обратного развития морфологических изменений слизистой оболочки желудка в результате эрадикации Helicobacter pylori / , , // Омский научный вестник. – 2006. – Специальный выпуск. – №3(37), Ч. II. – С.48–55.
10. Ливзан хронического гастрита, ассоциированного с Helicobacter pylori, в постэрадикационном периоде / , , // Экспериментальная и клиническая гастроэнтерология. – 2007. – Вып. 5. – С. 116–123.
11. Ливзан период хронического гастрита, ассоциированного с инфекцией Helicobacter pylori / , , // Consilium Medicum. – 2008. – Т. 10. - №8. - С.15–20.
12. Мозговой метаплазия слизистой оболочки желудка: от природы феномена к прогнозу / // Бюллетень Сибирского отделения Российской академии медицинских наук. – 2009. – № 3. – С. 5–9.
13. Яковлева протективных факторов слизистой оболочки желудка в морфогенезе хронических язв, осложненных кровотечением / , , // Уральский медицинский журнал. – 2009. – №. 4(58). – С. 31–34.
14. Мозговой определения типа кишечной метаплазии слизистой оболочки желудка с помощью комбинированных гистохимических методов / // Арх. патол. – 2009. - № 4. – С. 46–47.
15. Аруин классификация хронического гастрита: что следует принять и что вызывает сомнения / , , // Арх. патол. – 2009. – № 4. – С. 11–18.
16. Пролиферативная и муцинпродуцирующая активность в участках кишечной метаплазии при хроническом атрофическом гастрите и язве желудка / и др. // Вестник РАМН. – 2010. – №7. – С. 15–19.
17. Мозговой интегрального показателя атрофии слизистой оболочки при хроническом гастрите в прогнозе риска развития рака желудка / , , // Омский научный вестник. – 2010. – №1 (94). – 80–83.
18. Мозговой пересмотр Международной классификации хронического гастрита: оценка нового диагностического подхода методами каппа-статистики / , , и др. // Омский научный вестник. – 2010. – №1 (94). – 84–88.
19. Новиков риска развития рака желудка кишечного типа у носителей полиморфных аллелей генов цитокинов/ , , // Медицина в Кузбассе. – 2010. – №4. – С. 21–24.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |


