2. Какой объем занимают 6,02*1023 атомов азота при н. у.?
3. Сколько атомов азота в 2,8 л оксида азота (III) (н. у.)?
4. Сколько литров водорода (20оС и 100 кПа) выделится при взаимодействии 165 г Fe с 1 кг 30%-ого р-ра HCl? Сколько граммов HCl не войдет при этом в реакцию?
5. Из 1,568г железной руды получили осадок фосформолибдата состава Р2О5*24МоО3 массой 0,427г. Каково содержание фосфора в руде в процентах?
6. 5 мл водорода сожгли с 10 мл воздуха. После сгорания объемов газов составил 8,7 мл. Какова объемная доля кислорода в воздухе, взятом для горения? Какова его мольная доля в воздухе?
7. Вещество содержит 75,76% мышьяка и кислород. Плотность паров по воздуху этого вещества 13,65. Какова формула этого соединения?
Литература:
Глинка и упражнения по общей химии. – Л.: Химия, 1988.
Глинка химия. Л.: Химия, 1973.
Мень к контрольным и лабораторным работам по общей и неорганической химии.- Мурманск, 2004.
Практические занятия №3
Тема: Эквивалент. Закон эквивалентов.
План:
1. Химический эквивалент элемента в соединениях;
2. Химические эквиваленты сложных веществ; основные расчетные формулы;
3. Вычисления на основе закона эквивалентных отношений;
1) количество вещества эквивалентов (nэкв. (А));
2) молярная масса эквивалентов вещества: Э(А);
3) объем эквивалентов вещества: Vэкв. (А);
4) закон эквивалентных отношений: m(А)/m (B)=Э(А)/Э(В)
Вопросы для обсуждения:
1) как определяется молярная масса эквивалентов:
- элемента в соединении АаВв;
- оксида А2Ов;
- кислоты НаВ;
- основания А(ОН)в;
- соли АаВв;
2) как связаны между собой молярная и нормальная концентрации?
Расчетные задачи:
1) Одинаков ли эквивалент хрома в соединениях СrCl3 и Сr(SO4)3. Ответ подтвердите расчетами.
2) На восстановление 1,8 г оксида металла израсходовали 833 мл Н2 (н. у.). найти эквивалентные массы металла и оксида.
3) Содержание мышьяка в двух разных оксидах его равно 65,2% и 75,7% соответственно. Каковы величины эквивалентных масс мышьяка в этих оксидах? Составить формулы оксидов.
Задания для самостоятельной работы:
1) вычислите молярную массу эквивалентов Н3РО4 при реакциях обмена, в результате которых образуются:
а) Na3PO4
б) Nа2НРО4
в) NаН2РО4
2) один из металлов группы II А Периодической системы элементов массой 2,25 г при взаимодействии с соляной кислотой вытесняет 6,01 л водорода при 20оС и 1,013*105 Па. Назовите металл.
3) гидрид металла содержит 4,76% водорода. Рассчитайте молярную массу эквивалента металла и назовите металл.
Практические занятия №4 (2 ч.)
Тема: Строение атома. Химическая связь.
План:
1. Электронная конфигурация элемента.
2. Конфигурации атомов в возбужденном состоянии.
3. Валентные возможности атомов одного и того же элемента. Использование таблицы электроотрицательностей атомов.
Вопросы для обсуждения:
1. Дайте характеристику квантовых чисел состояния электрона.
2.Что означает запись 2 р2?
3. Опишите формулу орбитали с квантовыми числами: n=3; l=0; m=0. Могут ли быть орбитали другой формы при данном n?
4. Как происходит sp-, sp2-, sp3 – гибридизация? Приведите примеры.
5. Что такое «сигма» и «пи» - связь? Как они возникают?
6. Какая из конфигураций электронных оболочек возможна: 2s2, 2p5, 3f3, 2d3, 3d11, 2p8?
7. Какие типы кристаллических решеток вам известны?
8. Какие факторы влияют на прочность химической связи?
9. Какое влияние оказывают водородные связи на температуру кипения жидкостей?
Задания для самостоятельной работы:
1. Атомы каких из приведенных элементов являются изобарами:
402
а. 20 Ca и 20Ca; b. 18 Ar и 19K; c. 48Cd и 50Sn; d. 54Xe и 56Ba?
2. Какой подуровень в атомах - 3d или 3p и 6s или 5d - заполняется раньше:
3. Какова конфигурация валентных электронов в атоме технеция.
4. Сколько свободных 3d-орбиталей в атоме хрома.
5. Какие из электронных конфигураций соответствуют возбужденным состояниям:
a. ...2s2; b. ...3s2 3d1; c. ... 4s2 3d2; d. ... 1s2 2s2 p6 3p1?
6. Сколько электронов находится на 4d - подуровне атома гафния?
7. Атомы каких элементов - актиноидов имеют наибольшее число неспаренных f-электронов:
a. Pu; b. Am; c. Cm; d. Bk?
8. Какой из переходов электрона в атоме водорода требует поглощения фотона с минимальной энергией:
a. 1s → 2p; b. 1s → 4d; c. 2s → 4s; d. 2p → 3s?
9. Какие значения всех квантовых чисел (n, ml, m, ms) возможны для валентного электрона атома калия:
a. 4, 1, -1 , - 1/2; b. 4, 1 , +1 , +1/2; c. 4, 0, 0, + 1/2; d. 5, 0, +1, +1/2?
10. Какое из приведенных химических соединений имеет более прочную химическую связь: а) HI или НВr; б) Н2О или Н2S; в) NH3 или PH3?
Литература:
Глинка и упражнения по общей химии. – Л.: Химия, 1988. Глинка химия. Л.: Химия, 1973. Мень к контрольным и лабораторным работам по общей и неорганической химии.- Мурманск, 2004.Практическое занятие № 5 (2 ч.)
Тема: Основы химической термодинамики.
Кинетика химических реакций.
Термодинамика
План:
1. Основные понятия химической термодинамики.
2. Закон Гесса и его следствия.
3. Критерии самопроизвольного протекания процессов.
4. Термодинамика процессов растворения газов, жидкостей и кристаллических веществ в воде.
Вопросы для коллективного обсуждения:
1. Чему равен тепловой эффект химической реакции?
2. Какие уравнения реакций называют термохимическими?
3. Что называют стандартной энтальпией образования вещества?
4. Сформулируйте закон Гесса.
5. Сформулируйте следствия из закона Гесса.
6. Каким соотношением связаны энтальпия, энтропия и энергия Гиббса?
7. При каких условиях химические реакции протекают самопроизвольно?
Расчетные задачи:
1. На основании справочных данных рассчитайте стандартные изменения энтальпии в каждой из следующих химических реакций (предварительно подберите коэффициенты):
а) ZnS (T)+ O2(г) = ZnO(T) +SO2(г)
б) AgNO3(T) =Ag(T) + NО2(Г)+ O2(г)
2. По термохимическому уравнению рассчитайте стандартную энтальпию образования продуктов:
4NO2(Г) + О2(г) + 2Н2О(Ж) = 4HNO3(Ж) , ∆Н ° 298 = -256 кДж.
3. Определите возможность протекания реакции
P2O5(т)+H2O(ж)→ O2(г)+PH3(г)
при стандартных условиях.
Задания для самостоятельной работы:
1. На основании справочных данных рассчитайте стандартные изменения энтальпии в каждой из следующих химических реакций (предварительно подберите коэффициенты):
а) (NH4)2CrО4(T) = Cr2O3(T) +N2 +Н2О(Ж) + NH3(Г)
б) SO2(г) + H2S(г) = S(T) + Н2О(Ж)
2. По термохимическому уравнению рассчитайте стандартную энтальпию образования продуктов:
2А12О3(Т)+ 6SO2(Г) + 3O2(Г) = 2AI2(SO4)3(Т), ∆Н ° 298 = -1750 кДж;
3. Путем расчета определите уравнение реакции, по которому возможно разложение пероксида водорода при стандартной температуре:
а) Н2О2(Гг)= Н2(Г) + O2(Г)
б) Н2О2(Г) = Н2О(Ж) + 0,5 O2(Г)
Литература:
Глинка и упражнения по общей химии. – Л.: Химия, 1988.
Глинка химия. Л.: Химия, 1973.
Мень к контрольным и лабораторным работам по общей и неорганической химии.- Мурманск, 2004.
Практическое занятие № 6 (2 ч.)
Тема: Кинетика химических реакций.
План:
Основные понятия химической кинетики. Скорость химической реакции. Константа скорости реакции. Химическое равновесие. Принцип Ле-Шателье.Вопросы для коллективного обсуждения:
Что такое скорость химической реакции и от каких факторов она зависит? Что называют константой скорости реакции и каков физический смысл этой величины? Какие факторы влияют на нее? Какова зависимость скорости реакции от температуры? Что называется температурным коэффициентом скорости реакции? Какие значения он может иметь? Что называют константой химического равновесия? От каких факторов она зависит? Какие факторы влияют на состояние химического равновесия? Сформулируйте принцип Ле-Шателье. Как изменится скорость реакции 2NO + О2 → 2NO2, протекающей в закрытом сосуде, если давление увеличить в 4 раза? Как возрастет скорость реакции при повышении температуры от 50 до 100 °С, если температурный коэффициент равен 2? В какую сторону сместится химическое равновесие при изменении температуры и давления в следующих случаях: а) 2Н2О ↔ 2Н2 + О2, ∆Н° > 0 б) О2 + 2СО ↔ 2СО2, ∆Н ° < 0 Как влияет на равновесие систем повышение давления? температуры? а) 2SO3 ↔ 2SO2 + О2, ∆Н ° > 0 б) N2 + О2 ↔ 2NO, ∆Н ° > 0 Напишите выражение константы равновесия системы, предварительно расставив коэффициенты:NH3 + О2 ↔ NO + H2O(пар)
Каким образом можно сместить равновесие этой системы вправо?Задания для самостоятельной работы:
1. Во сколько раз уменьшится скорость реакции при понижении температуры от 120 до 80 °С, если температурный коэффициент равен 3?
2. Взаимодействие между оксидом углерода (И) и хлором протекает по уравнению СО + С12 →СОС12. Концентрация оксида углерода (II) - 0,3 моль/дм3, хлора - 0,2 моль/дм3. Как изменится скорость прямой реакции, если увеличить концентрацию оксида углерода (II) до 1,2 моль/дм3, а концентрацию хлора - до 0,6 моль/дм3?
3. В какую сторону сместится химическое равновесие при изменении температуры и давления в следующих случаях:
4. в) С + Н2О ↔СО + Н2, ∆Н ° > 0
5. г) N2 + ЗН2 ↔ 2NH3, ∆Н ° < 0
6. Напишите выражение константы равновесия системы 4Н2О(пар) + 3Fe(T) ↔ Fe3O4(T) + 4Н2(г), ∆Н ° < 0
7. Как следует изменить температуру, концентрацию и давление компонентов в равновесной системе 4НС1 + О2 ↔ 2С12+ 2Н2О, ∆Н Н° < 0, чтобы повысить выход хлора?
8. Укажите общий порядок реакции 2NO + Н2 = N2O + Н2О и порядок реакции по каждому веществу. Напишите кинетическое уравнение реакции.
9. Во сколько раз возрастет скорость реакции при повышении температуры от 37 до 47 °С, если энергия активации равна 74,5 кДж/моль?
Литература:
Глинка и упражнения по общей химии. – Л.: Химия, 1988.
Глинка химия. Л.: Химия, 1973.
Мень к контрольным и лабораторным работам по общей и неорганической химии.- Мурманск, 2004.
Практическое занятие №7 (2 ч.)
Тема: Количественный состав растворов.
План:
1. Способы выражения состава раствора:
Массовая доля растворенного вещества; молярная доля растворенного вещества и растворителя; молярная концентрация растворенного вещества (молярность); молярная концентрация эквивалентов вещества (нормальность); объемная доля в газовых растворах
2. Растворимость веществ.
Вопросы для обсуждения:
1) типы растворов, их компоненты;
2) гидраты и сольваты (кристаллогидраты)
3) способы выражения содержания растворенного вещества в растворе: массовая доля, молярная доля, молярная концентрация, объем и плотность растворов (расчетные формулы);
4) определение растворимости вещества;
5) зависимость растворимости газа от давления.
Расчетные задачи:
1) Сколько граммов соли и воды содержится в 800г раствора 12% NaNO3?
2) Сколько граммов Na2SO4*2H2O следует растворить в 250г воды для получения раствора, содержащего 5% безводной соли?
3) Сколько граммов 10%-ого раствора Н2SO4 потребуется для обменного взаимодействия с 100 мл 13,7%-го раствора Na2CO3 (плотность=1,145г/см3)?
4) Сколько миллиметров 96%-ной серной кислоты необходимо взять для приготовления 2 л 0,5 М раствора?
5) Вычислите растворимость Ba(NO3)2 в воде при 20 °С, если в 545 г раствора нитрата бария при этой температуре содержится 45 г соли.
6)Вычислите массовую долю K2SO4 и его коэффициент растворимости, если при 0 °С 50 г раствора содержат 3,44 г сульфата калия.
7) При охлаждении насыщенного при 90 °С раствора до 25 °С выкристаллизовалось 200 г соли. Какую массу воды и соли надо взять, если растворимость соли при 90 и 25 °С соответственно составляет 42,7 и 6,9 г?
Задания для самостоятельной работы:
Вычислите массу гидроксида натрия, необходимую для приготовления 2 л 20%-ного раствора NaOH. Какой объем воды необходимо прибавить к 200 мл 68%-ного раствора серной кислоты, чтобы получить 10%-ный раствор кислоты? Определите молярную концентрацию раствора серной кислоты, который получится, если к 100 мл 96%-ной серной кислоты прибавить 400 мл воды. Кислота в автомобильном аккумуляторе (раствор серной кислоты) имеет плотность 1,2 г/см3. Какова массовая доля H2SO4 в этом растворе? Сколько миллилитров 96%-ной серной кислоты нужно взять для приготовления 1 л аккумуляторной кислоты? Каково содержание (в массовых долях) NaOH в его растворе концентрацией 2 моль/л? Коэффициент растворимости СаС12 в воде при 100 °С равен 159 г на 100 г Н2 О. Какая масса хлорида кальция при этой температуре содержится в 1,35 кг раствора? Определите массовую долю СоС12 и растворимость хлорида кобальта, если 500 г его раствора при 20 °С содержат 173 г соли. Растворимость CuSO4 при 20 и 100 °С равна соответственно 20,2 и 77 г. Какая масса сульфата меди выпадет в осадок, если охладить 825 г раствора от 100 до 20 °С? Определите массу карбоната калия, выпавшего в осадок из 770 г насыщенного при 100 °С раствора и охлажденного до 0 °С, если в 100 г растворителя при 100 °С содержится 155 г соли, а при 0 °С 111 г К2СО3. Какой объем надо взять, чтобы растворить 250 г хлора при 10 °С и давлении 1,5-105Па? Растворимость хлора при 10 °С и давлении 1, Па составляет 3,Н8 м3 на 1 м3 воды.Литература:
Глинка и упражнения по общей химии. – Л.: Химия, 1988.
Глинка химия. Л.: Химия, 1973.
Мень к контрольным и лабораторным работам по общей и неорганической химии.- Мурманск, 2004.
Практическое занятие № 8 (2 ч.)
Тема: Ионные реакции в растворах.
План:
1. Уравнения ионных реакций обмена:
1) молекулярные;
2) полные ионные;
3) сокращенные ионные.
2. Случаи необратимых реакций обмена с образованием:
- малорастворимых веществ
- малодиссоциирующих веществ
- газообразных веществ или летучих соединений.
Вопросы для обсуждения:
1. а) сильные и слабые электролиты;
б) степень и константа диссоциации;
в) ионные реакции и направление их протекания;
г)условия протекания реакций в растворах электролитов.
2. Упражнения в написании уравнений ионных реакций обмена:
1) Са(NO3)2 + K2CO3 →
2) HNO3 + Ba(OH)2 →
3) Ba(NO2)2 + K2SO4→
4) K2CO3 +HCl→
5) Na2CO3 + H2SO4→
6) NaOH +Fe(NO3)2→
7) Pb(NO3)2 + K2SO4→
8) Na2SiO3 +Ba(OH)2→
9) FeCl3 +CsOH→
10) FeSO4 +Na3PO4 →
11) Pb(NO3)2 + K2SO4→
12) Na2SiO3 +Ba(OH)2→
13) FeCl3 +CsOH→
14) FeSO4 +Na3PO4 →
Задания для самостоятельной работы:
1. Составьте уравнения реакций в молекулярном и ионном виде:
а) Р2О5+ Са(ОН)2 → з) FeCI3 + NaOH→
б) ZnO + H3PO4 → н) СаО + СО2 →
в) Sn(OH)2 + NaOH → к) SО3 + Са(ОН)2 →
г) Sn(OH)2 + НС1 → л) Pb(NO3)2 + KCI →
д) NaHCO3 + HC1 → м) SO2 + Н2О →
Практическое занятие № 9 (2 ч.)
Тема: Окислительно-восстановительные реакции. Методы электронного и электронно-ионного баланса.
План:
1. Типы окислительно- восстановительных реакций (ОВР):
- межмолекулярная;
- внутримолекулярная;
- реакция диспропорционирования
2. Роль среды в ОВР: разбор примеров ОВР и подборе коэффициентов уравнений методами электронного и электронно-ионного баланса:
1. Аg + HNO3, конц. →
Аg + HNO3, разб. →
Mg + HNO3, конц. →
Mg + HNO3, разб. →
Mg + HNO3, очень разб. →
2. NaOH +S = Na2S+Na2SO3
BaCrO4 =BaO +Cr2O3 +O2
Na2SO3 + KMnO4 +KOH = Na2SO4 + K2MnO4 +H2O
FeSO4 + KMnO4+H2SO4 = Fe2(SO4)3 +MnSO4 + K2SO4 + H2O
Na2SO3 + KMnO4 +H2O = Na2SO4 + MnO2 + KOH
H2S + K2Cr2O7 + H2SO4 = K2SO4 +Cr2(SO4)3 + H2O
Вопросы для обсуждения:
1. Стандартные окислительно-восстановительные потенциалы.
2. Направление протекания окислительно-восстановительных реакций.
3. Окислительно-восстановительные реакции в мониторинге и защите окружающей среды.
Задания для самостоятельной работы:
Написать уравнения окислительно-восстановительных реакций, протекающих в растворах, и подобрать необходимые коэффициенты методом ионно-электронного баланса.
1) MnO4- +H+ +NaCl → Cl2 + Mn2+ +H2O +…
2) Cr(OH)4)- + Br2 + OH - → CrO42- +Br - +H2O+ …
3) Cr3+ + S2O82- + H2O → Cr2O72- + SO42- +H+ + …
4) NaOH +S → Na2S +Na2SO3 + ....
5) AgCl + Mn2+ +OH - → Ag+ MnO(OH)2 + Cl - + H2O
6) SnCl2 +H2O2 +H+ +Cl - → SnCl4 + H2O+....
Литература:
Глинка и упражнения по общей химии. – Л.: Химия, 1988.
Глинка химия. Л.: Химия, 1973.
Мень к контрольным и лабораторным работам по общей и неорганической химии.- Мурманск, 2004.
1.7.2 Тематика и планы лабораторных работ по изученному материалу.
Лабораторная работа № 1-2(4 ч.)
ТЕМА: ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Цель работы — изучить некоторые химические свойства оксидов, гидроксидов, кислот, солей и условия необратимости реакции между растворами двух веществ.
ТБ в химической лаборатории.
Приемы работы с химических оборудование и реактивами.
Опыт 1. Взаимодействие основных оксидов с водой.
Опыт 2. Взаимодействие кислотных оксидов с водой.
Опыт 3. Взаимодействие солей с основаниями. Получение нерастворимых в воде гидроксидов металлов и определение их характера.
Опыт 4. Взаимодействие кислот с солями.
Опыт 5. Получение средних и кислых солей.
Опыт 6. Получение гидроксида меди (II) и основной соли меди.
Опыт 7. Взаимодействие солей друг с другом.
Контрольные вопросы
1. Какие вещества называются оксидами? Приведите примеры основных, кислотных и амфотерных оксидов.
2. Как образуются гидроксиды? Какие вещества называются основаниями? кислотами?
3. На примере оксидов и гидроксидов элементов третьего периода объясните изменения их характера при увеличении порядкового номера элемента.
4. Как определяют кислотность основания? Как определяют основность кислоты?
5. Какие вещества называются солями? Назовите различные способы получения солей и составьте соответствующие уравнения.
6. В чем сходство диссоциации оснований? кислот? Докажите, что оно имеется.
7. Как образуются нерастворимые в воде основания? Составьте соответствующие уравнения.
8. Какие гидроксиды называются амфотерными? Как доказать их амфотерность?
9. Назовите условие необратимости реакции между растворами двух солей.
10. Составьте уравнения реакций:
а) Р2О5+ Са(ОН)2 → з) FeCI3 + NaOH→
б) ZnO + H3PO4 → н)СаО + СО2 →
в) Sn(OH)2 + NaOH → к) SО3 + Са(ОН)2 →
г) Sn(OH)2 + НС1 → л) Pb(NO3)2 + KCI →
д) NaHCO3 + HC1 → м) SO2 + Н2О →
е) NaHCO3 + NaOH → н) MnO + Н2О→
ж) Са(НСО3)2+ NaOH → о) Mg(OH)2 + СО2 →
11. При помощи каких реакций можно осуществить следующие переходы от одного вещества к другому?
а) Zn → ZnS → ZnO → (ZnOH)2SO4 → ZnO
б) Cu(OH)2 → CuCl2 → ZnCl2→ ZnOHCl→ ZnSO4
в) CO2 → MgCO3 → Mg(HCO3)2 → MgCO3 → MgO
г) С →CО2 → H2CO3 → BaCO3 → BaCl2
д) MgO → MgCl2→ Mg(OH)2 → MgOHNО3 → Mg(NO3)2
Лабораторная работа № 3 (2ч.)
ТЕМА: Определение теплоты нейтрализации
Цели работы — изучить лабораторные способы определения теплового эффекта химической реакции на примере реакции нейтрализации.
Оборудование и материалы:
1. Калориметрическая ячейка (см. рис.1).
2. Термометр с ценой дел. 0,01°.
3. Мешалка.
4. Весы аналитические.
5. Мерный цилиндр на 100 мл.
Реактивы:
1. NaOH, 1 н р-р;
2. НСl, 1 н р - р; H2SO4; HNO3 ( кислота выбирается по заданию преподавателя).
3. КС1, кристаллич.
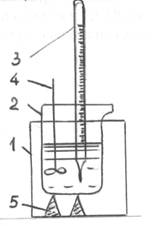
1 - стакан
2 – ячейка (300 мл)
3 - термометр
4 - мешалка
5 – деревянная подставка
Ход определения:
1. Определение постоянной калориметра.
Постоянная калориметра характеризует теплоемкость системы данной конструкции с учетом размеров, массы и материала используемой установки.
Для определения постоянной ячейки в нее заливают 200 мл воды и выдерживают ее до установления температуры окружающей среды. Готовят навеску хлорида калия около 0,05 моль и всыпают соль в воду при перемешивании, следя за изменениями температуры. Определяют максимальную установившуюся температуру с точностью до 0,01°. Расчет постоянной калориметра производят по формуле:

К - постоянная калориметра;
Q - теплота растворения KCl для соответствующей концентрации, кДж/моль (берут из справочника);
vKCl - навеска KCl, моль.
tMAX - максимальная температура раствора после растворения соли;
tНАЧ - температура воды в начале опыта.
2. Определение теплоты нейтрализации.
В стакан калориметра заливают 100 мл NaOH, опускают термометр и мешалку. После установления постоянной температуры при перемешивании вливают 100 мл 1н НС1 и следят за подъемом температуры до максимальной. После того как температура начнет снижаться записывают значение.
Расчет проводят по уравнению:
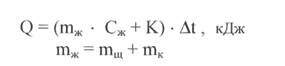
mЖ - масса жидкости в стакане, г
mЩ, mК - массы взятых щелочи и кислоты соответственно, г
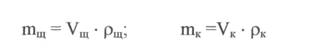
ρЩ, ρК - плотности растворов щелочи и кислоты соответственно (берут из справочника)
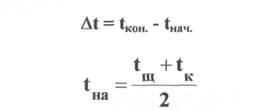
tЩ, tK - температура щелочи и кислоты перед сливанием растворов (из опыта).
Сж - теплоемкость жидкости после сливания, принимаемая равной 4,18 • 10-3 кДж/г - град. К - постоянная ячейки, определенная в п.1., кДж/град.
Задание:
1. Рассчитать теплоту нейтрализации в кДж/моль.
2. Оформить отчет о работе.
3. Сделать расчет ошибки определения:
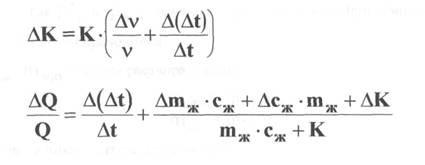
Лабораторная работа № 4 (2ч.)
ТЕМА: КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ.
ХИМИЧЕСКОЕ РАВНОВЕСИЕ
Цели работы — изучить скорость химической реакции и ее зависимость от концентрации, температуры, введения катализатора; выяснить влияние концентрации веществ на сдвиг химического равновесия.
Оборудование и реактивы: набор пробирок вместимостью 20 см3 с пробками, химический стакан вместимостью 250 см3, термометр, мерные цилиндры вместимостью 10 см3, водяная баня, секундомер; растворы: 1 н Na2S2O3, 2 н H2SO4, 0,1 н КМпО4, 0,1 н KNO3, цинк в гранулах, 0,001 н и концентрированные растворы FeCl3 и KCNS, насыщенный раствор КСl.
Опыт 1. Влияние концентрации реагирующих веществ на скорость реакции
Зависимость скорости реакции от концентрации реагирующих веществ изучают на примере взаимодействия раствора тиосульфата натрия с раствором серной кислоты.
Таблица 1
Номер пробирки | Объем V, см3 | Общий объем V, см3 | Относительная концентрация Na2S2O3 | Время начала помутнения т, с | Относительная скорость реакции 1/τ, с-1 | ||
Na2S2O3 | Н2О | H2SO4 | |||||
1 | 9 | 0 | 3 | 12 | 1 | ||
2 | 6 | 3 | 3 | 12 | 0,67 | ||
3 | 3 | 6 | 3 | 12 | 0,33 |
На миллиметровой бумаге постройте график зависимости 1/ τ - Cотн(Na2S2O3). Сделайте вывод о зависимости скорости реакции от концентрации Na2S2O3.
Каким должен быть график при идеальном выполнении закона действующих масс?
Опыт 2. Влияние температуры на скорость реакции
Зависимость скорости реакции от температуры изучают на примере взаимодействия тиосульфата натрия с серной кислотой.
Используя правило Вант-Гоффа, рассчитайте значение температурного коэффициента для данной реакции.
Таблица 2
Номер пробирки | Объем V, см3 | Общий объем V, см3 | Температура t/C | Время начала помутнения, τ, с | Относительная скорость реакции1/τ, с-1 | |
Na2S2O3 | H2SO4 | |||||
1 | 5 | 5 | 10 | |||
2 | 5 | 5 | 10 | |||
3 | 5 | 5 | 10 |
Опыт 3. Влияние катализатора на скорость реакции

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



