ЛБ №2 – до 10 баллов.
ЛБ №3 – до 10 баллов.
ЛБ №4 – до 10 баллов.
ЛБ №5 – до 10 баллов.
ЛБ №6 – до 10 баллов.
ЛБ №6 – до 10 баллов.
ЛБ №7 – до 10 баллов.
ЛБ №9 – до 10 баллов.
ЛБ №9 – до 10 баллов.
ЛБ №10 – до 10 баллов.
Вводный тест – 25 баллов.
Тестирование по теме «Дисперсные системы» – 25 баллов.
Зачетное тестирование – 20 баллов.
Итого: 520 баллов.
Примеры рейтинговых заданий представлены в разделе «Примерные зачетные тестовые задания».
Задания для самостоятельной работы выполняется студентом с использованием лекций и учебных пособий и оформляется в письменном виде. Задание должно быть сдано студентом в строго определенные сроки в соответствии с учебным календарным планом. Целью самостоятельной работы студента является подготовка тестированию по соответствующим темам и экзамену.
Для оценки 5 сумма баллов за все модули должна быть не менее 480, для оценки 4 – не менее 400 баллов и для оценки 3 – не менее 280 баллов. Если оценка студента не устраивает или он набрал менее 280 баллов, студент сдает экзамен по дисциплине.
Выполнение практической части обязательно.
РАЗДЕЛ 2. Методические указания по изучению дисциплины
Мень к контрольным и лабораторным работам по общей и неорганической химии.- Мурманск: МГПУ, 200с.
Организация работы и ведение лабораторного журнала
1. Прежде чем приступить к выполнению лабораторной работы, изучите необходимый материал по учебнику, лекционным записям и методическим указаниям к ней.
2. До начала опыта предварительно подробно ознакомьтесь по методическим указаниям с условиями выполнения данного опыта и продумайте последовательность операции.
3. Выполняя опыт, соблюдайте все меры предосторожности, количественные соотношения веществ, проводите необходимые наблюдения.
4. Все лабораторные работы выполняйте индивидуально, за исключением тех, которые по указанию преподавателя проводятся группами. Опыты производите в чистой посуде.
5. Не загромождайте свое рабочее место: не кладите на стол портфели, книги, свертки и пр.
6. Не уносите приборы, аппараты, реактивы общего пользования на свое рабочее место. Примите за правило: каждый предмет или реактив необходимо возвращать на место сразу после его использования.
7. Соблюдайте тишину в лаборатории. По окончании работы вымойте химическую посуду, тщательно уберите рабочее место, отключите воду и электричество.
8. Запись выполненных работ и обязательных опытов производите в лабораторном журнале, в котором должны быть представлены все необходимые наблюдения, схема установки, уравнения реакций, вычисления, выводы.
Все наблюдения записывайте в лабораторный журнал непосредственно после проведения каждого опыта. При этом особое внимание следует обращать на эффект реакции: изменение окраски, выпадение и растворение осадка, появление характерного запаха и т. д.
Недопустимо пользоваться «случайными» листочками бумаги: это может привести к ненужной переписке и, кроме того, потере результатов экспериментов.
В отчете о лабораторной работе должны быть указаны:
1) дата выполнения работы;
2) название лабораторной работы;
3) номер и наименование опыта;
4) рисунок или схема прибора (если пользовались прибором);
5) последовательность выполнения работы (условия проведения и краткое описание опыта);
6) наблюдаемые явления;
7) уравнения всех реакций, происходящих в опыте;
8) таблица с результатами наблюдений;
9) расчеты (если работа носит количественный характер);
10) графики;
11) ответы на поставленные вопросы;
12) выводы.
К графическому представлению экспериментальных данных предъявляются следующие требования. График размером около половины тетрадного листа выполняют карандашом на миллиметровой бумаге и вклеивают в лабораторный журнал. Координатные оси располагают на расстоянии 1—1,5 см от края листа и не заканчивают стрелками. Масштаб выбирают таким образом, чтобы график занимал все поле между осями координат. При соединении экспериментальных точек следует учитывать не только относительное их расположение, но и теоретические представления о виде (типе) зависимости.
Правила техники безопасности при работе химической лаборатории
Работа в химической лаборатории требует особого внимания и обязательного выполнения необходимых требований. Это связано с тем, что в лаборатории находятся электрические приборы, едкие, ядовитые и огнеопасные вещества. Поэтому при работе в лаборатории студенты должны строго соблюдать следующие правила техники безопасности:
1. При выполнении всех работ в химической лаборатории следует соблюдать осторожность.
2. В целях безопасности работать с малыми количествами реактивов.
3. Следует предохранять руки от пореза стеклом, ожогов горячими предметами и концентрированными кислотами и щелочами.
4. Нельзя брать вещества руками и пробовать их на вкус. Нюхать вещества следует, держа отверстие пробирки с веществом на некотором расстоянии от лица, ниже уровня носа и направляя струю газа или пара движением руки к себе.
5. Нагревать жидкость в пробирке следует постепенно, направляя отверстие пробирки в сторону от своего и соседнего рабочего места, так как вследствие частичного перегрева может произойти выбрасывание жидкости.
6. Нельзя наклоняться над пробиркой с кипящей жидкостью, а также над сосудом, в котором смешивают какие-либо вещества, особенно жидкости. Наблюдать за ходом реакции в стеклянном сосуде следует через его стенки.
7. При растворении кислот необходимо наливать кислоту в воду (как в случае с серной кислотой), а не наоборот.
8. Все опыты с неприятно пахнущими и ядовитыми веществами следует проводить только в вытяжном шкафу.
9. Весьма вредны пары ртути, поэтому пролитую ртуть нужно тщательно собрать и обязательно сообщить об этом преподавателю. Поверхность, на которой была ртуть, необходимо тщательно смочить раствором хлорида железа (III) с массовой долей 20 %.
10. Работу с эфиром, толуолом, спиртом и другими легковоспламеняющимися веществами следует проводить вдали от огня.
11. Израсходованные или взятые в избытке реактивы нельзя выливать обратно в склянки или раковины, их следует переливать в специально отведенные стеклянные емкости.
12. Нельзя путать пробки от склянок, а также пипетки для взятия реактивов.
13. Горячие пробирки и посуду необходимо ставить только на специальные подставки.
14. После работы в лаборатории обязательно вымойте руки.
15. При попадании реактива (особенно щелочи или кислоты) в глаза, на кожу или одежду, прежде всего, смойте его большим количеством воды, а затем промойте пораженные участки нейтрализующим средством.
16. При термических ожогах пораженное место смочите раствором таннина в спирте или раствором перманганата калия с массовой долей 2 %.
17. При химических ожогах сильной струей воды удалите с кожи вещество, вызвавшее ожог, сообщите преподавателю или лаборанту о несчастном случае.
РАЗДЕЛ 3. Содержательный компонент теоретического материала.
Лекция 1. Основные химические понятия и законы.
Введение. Задачи, стоящие перед химической наукой; отличительные особенности изучения химии в вузе. Место химии в ряду наук о природе, ее связь с другими естественнонаучными достижениями. Развитие "пограничных" наук.
1.1. Международная система единиц физических величин и ее применение в неорганической химии. Основные единицы системы СИ. Масса, объем и плотность вещества, давление, концентрация, энергетические величины.
1.2. Атомно-молекулярное учение. Современная система атомных масс. Изотопы и изобары. Атомная масса и массовое число изотопа. Изотопный состав элемента. Простые и сложные вещества. Молекулярная масса. Индивидуальные вещества и их смеси. Химическая классификация чистоты веществ.
1.3. Стехиометрия химических реакций. Стехиометрические законы. Стехиометрические уравнения. Моль - единица количества вещества. Эквивалент. Закон эквивалентов. Способы выражения концентрации растворов.
1.4. Современная номенклатура неорганических веществ. Химические элементы. Простые вещества. Ионы; различные классы соединений. Кислоты и их соли, оксиды. Комплексные соединения.
Лекция 2. Основы строения вещества.
2.1. Строение атома. Понятие о квантовой механике.
2.2. Характеристика состояния электронов системой квантовых чисел, их физический смысл. Атомные орбитали для s-, p-, d - состояний электронов.
2.3. Принцип Паули. Максимальное число электронов в электронных слоях и оболочках. Правило Хунда.
2.4. Последовательность энергетических уровней и подуровней электронов в многоэлектронных атомах. Энергия ионизации, сродство к электрону.
2.5. Периодический закон и строение атомов элементов. Современная формулировка периодического закона. Структура периодической системы.
2.6. Заполнение электронных слоев и оболочек атомов. Периодическое изменение свойств элементов (вертикальная, горизонтальная и диагональная периодичности). Атомные и ионные радиусы, их зависимость от электронного строения и степени окисления.
2.7. Периодический закон как основа неорганической химии, его философское значение.
Лекция 3.Химическая связь.
3.1. Ковалентная связь. Метод валентных связей.
3.2. Электроотрицательность. Свойства ковалентной связи; направленность и насыщаемость. Полярная ковалентная связь. Механизм образования ковалентной связи (обменный, донорно-акцепторный). Характеристика ковалентной связи: длина, прочность, валентные углы.
3.3. Понятие о нахождении средней энергии связи в сложных молекулах. Эффективные заряды атомов в молекулах. Дипольные моменты и строение молекул.
3.4. Основные положения метода валентных связей. Валентность элемента.
3.5. Ионная связь. Ионная связь как предельный случай ковалентной связи. Ненаправленность и ненасыщаемость ионной связи. Электростатическое взаимодействие ионов. Кривая потенциальной энергии для ионной молекулы. Понятие о расчете энергии ионной связи. Поляризация ионов. Зависимость поляризации ионов от типа электронной структуры, заряда и радиуса иона. Влияние поляризации ионов на свойства вещества, температуру плавления, термическую устойчивость.
3.6. Межмолекулярное взаимодействие. Природа межмолекулярных сил. Энергия межмолекулярного взаимодействия. Взаимодействие между полярными и неполярными молекулами: ориентационное индуктивное, дисперсионное (силы ван-дер-Ваальса).
3.7. Водородная связь. Межмолекулярная и внутримолекулярная, симметричная и асимметричная водородная связь. Энергия и длина связи. Влияние водородной связи на свойства вещества (температуру плавления, кипения, степень диссоциации в водном растворе и др.).
3.8. Строение вещества в конденсированном состоянии. Твердое, жидкое, газообразное, плазменное состояния; их особенности. Типы кристаллических решеток (атомная, молекулярная, ионная, металлическая). Природа связи между частицами в различных типах кристаллических решеток. Нестехиометрические соединения. Дальтониды и бертоллиды.
Лекция 4-5. Химическая термодинамика.
1. Элементы химической термодинамики. Функции состояния. Понятие о химической термодинамике.
2.Внутренняя энергия и энтальпия, их физический смысл.
3.Термохимия зкзо - и эндотермические реакции. Термохимические уравнения.
4. Понятие о стандартном состоянии. Стандартные энтальпии образования веществ.
5. Закон Гесса и его следствия. Применение закона Гесса для вычисления энтальпий химических реакций, энергий связей в молекулах, энтальпий атомизации, энтальпий сгорания, энтальпий растворения и др.
6 Понятие об энтропии. Абсолютная энтропия и строение вещества. Изменение энтропии в различных процессах. Использование справочных данных для расчета характеристик различных процессов.
7. Химическое равновесие. Истинное и кажущееся равновесия, их признаки. Константа химического равновесия (Кр, Кс, Ка).
8. Энергия Гиббса, ее связь с энтропией и энтальпией. Изменение энергии Гиббса как характеристика равновесного состояния. Связь стандартного изменения энергии Гиббса с константой равновесия.
9. Равновесие в гомогенных и гетерогенных системах. Использование справочных данных для расчета стандартного изменения энергии Гиббса и константы химического равновесия. Связь изменения энергии Гиббса со стандартным изменением этой величины.
10. Критерий самопроизвольности процессов. Смещение химического равновесия. Принцип Ле-Шателье-Брауна. Влияние температуры, давления и концентрации реагентов на химическое равновесие.
Лекция 6. Химическая кинетика.
6.1. Скорость химической реакции. Закон действующих масс. Константа скорости химической реакции. Порядок и молекулярность химических реакций.
6.2. Факторы, влияющие на скорость химической реакции. Зависимость химической реакции от температуры.
6.3.Энергия активации. Уравнение Аррениуса.
6.4. Гомогенный и гетерогенный катализ.
6.5. Гомогенные и гетерогенные равновесия. Константа равновесия на примерах образования азота ( II ) в двигателях внутреннего сгорания и очистки природного газа от серы до сжигания (безотходные технологии переработки сырья).
6.6. Правило Ле – Шателье. Фазовые равновесия. Правило фаз Гиббса. Диаграммы состояния воды.
Лекция 7-8. Истинные растворы.
1 Общие сведения о растворах. Твёрдые и жидкие растворы.
2. Водные и неводные растворители.
3. Энергетика процессов растворения.
4.Зависимость растворения от температуры на примерах растворения CO2, О2 в воде. Зависимость растворения от природы и свойств растворителя на примерах растворения ртути;
5. Растворы неэлектролитов. Процессы, сопровождающие образование жидких истинных растворов. Краткая характеристика межмолекулярных взаимодействий в растворах.
6. Закон Рауля. Идеальные и реальные растворы. Активность. Коэффициент активности как мера отклонения свойств компонента от поведения в идеальном растворе.
7. Кипение и отвердевание растворов. Эбулиоскопия и криоскопия.
8. Осмос и осмотическое давление. Закон Вант – Гоффа;
Лекция 9. Гидролиз солей.
9.1 Ионное произведение воды. Водородный показатель.
9.2 Буферные растворы. Карбонатная буферная система Мирового океана. Буферные системы в почвах.
9.3 Гидролиз водных растворов солей.
9.4 Константа и степень гидролиза на примерах использования солей железа и алюминия для очистки сточных вод от взвешенных частиц.
9.5 Труднорастворимые электролиты. Произведение растворимости.
7.6 Условия осаждения и растворения осадка – на примерах реакций связывания углерода и фосфора в природе.
Лекция 10. Растворы электролитов.
10.1. Растворы электролитов. Типы электролитов.
10.2. Ассоциированные и неассоциированные электролиты. Теория электролитической диссоциации Аррениуса. Сольватация ионов и молекул.
10.3. Определение степени диссоциации слабого электролита в растворе на основе измерений электропроводности.
10.4. Константа диссоциации; закон разбавления Оствальда. Ступенчатая диссоциация слабых электролитов. Влияние одноименных ионов на равновесие диссоциации слабого электролита в растворе.
10.5. Равновесие в системе, состоящей из насыщенного раствора электролита и его кристаллов. Кривая растворимости.
10.6.Произведение растворимости; условия осаждения и растворения малорастворимого электролита.
Лекция 11-12. Дисперсные системы.
1. Основные особенности коллоидного состояния материи, классификация коллоидных систем, понятие о дисперсности. Основные положения термодинамики поверхностных явлений. Признаки объектов коллоидной химии.
2. Получение коллоидных систем: конденсация и диспергирование, химические способы получения.
3.Классификация дисперсных систем.
4. Коллоидные растворы. Строение мицеллы.
5.Молекулярно-кинетические и оптические свойства коллоидных систем. Броуновское движение, диффузия, распределение коллоидных частиц в гравитационном поле, седиментация. Осмотические свойства. Закономерности светорассеяния и светопоглощения, явление Тиндаля.
6. Поверхностные явления в дисперсных системах. Избыточная поверхностная энергия и поверхностное натяжение на границе раздела фаз, уравнение Гиббса.
7. Виды сорбции. Адсорбция и связь ее с поверхностным натяжением, поверхностно-активные вещества. Адсорбция из газовой фазы, изотерма Ленгмюра, строение адсорбционного слоя на границе раствор–газ. Адсорбция из растворов, обменная адсорбция, избирательная адсорбция, смачивание, флотация.
8.Устойчивость коллоидных систем. Агрегативная и седиментационная устойчивость. Факторы стабилизации дисперсных систем.
9. Коагуляция коллоидных систем. Факторы, вызывающие коагуляцию, коагуляция электролитами. Теории коагуляции: адсорбционная и электростатическая.
10. Микрогетерогенные системы. Эмульсии. Пены. Аэрозоли, Дымы и туманы.
11. Гели и студни. Явления синерезиса. Примеры образования плотной дымки, окутывающей промышленные города; реакций, описывающих процессы при возникновении химического и фотохимического смога. (Аэрозоли и загрязнение ОС: аэрозольный эффект, химический и фотохимический смоги.)
Лекция 13-14. Окислительно-восстановительные свойства веществ.
1. Окислительно-восстановительные реакции.
2. Важнейшие окислители и восстановители.
3. Окислительно-восстановительные свойства элементов и их соединений и периодический закон.
4. Классификация реакций окисления-восстановления. Составление уравнений реакций окисления-восстановления.
5. Окислительно-восстановительный эквивалент.
6. Понятие об электродных потенциалах. Стандартные электродные потенциалы, э. д.с. окислительно-восстановительной реакции. Электродный потенциал. Ряд напряжений металлов. Уравнение Нерста.
7. Электролиз. Вычисление стандартного изменения энергии Гиббса окислительно-восстановительных реакции на основе данных э. д.с.
8.Гальванические элементы. Электролиз расплавов и водных растворов и солей.
9. Инертные и активные электроды. Примеры использования олова, цинка и магния для защиты железа от коррозии.
Лекция 15. Комплексные соединения.
15.1. Химия комплексных соединений. Общие сведения о комплексных соединениях.
15.2 Комплексообразователь, лиганды, координационное число, внутренняя и внешняя сфера комплексного соединения.
15.3 Классификация комплексов.
15.4 Влияние комплексообразования на растворение. Важнейшие комплексообразователи и лиганды.
15.5 Номенклатура комплексных соединений.
15.6 Изомерия комплексов. Константа нестойкости комплексного иона.
15.7 Примеры реакций образования и распада окси - и карбоксигемоглобина. Воздействие СО на человека и животного. Токсичность. ЛД 50, ПДК.
РАЗДЕЛ 4. Словарь терминов (Глоссарий).
Химия — наука о веществах, их строении, свойствах и превращениях.
Химическая реакция — превращение одних веществ в другие вещества.
Атом — электронейтральная частица, в центре которой находится положительно заряженное ядро, а остальное пространство занято облаками отрицательно заряженных электронов. Атом является наименьшей частицей химического элемента, носителем его химических свойств.
Химический элемент — совокупность атомов с определенным зарядом ядра Z. Заряд ядра равен порядковому номеру элемента в периодической системе химических элементов ва.
Относительная атомная масса (Аr) — число, которое показывает, во сколько раз масса атома данного элемента больше 1/12 части массы атома изотопа углерода 12С.
Относительная молекулярная масса (Мг) — это число, которое показывает, во сколько раз масса молекулы (формульной единицы) данного вещества больше 1/12 части массы атома изотопа углерода 12С.
Моль — единица количества вещества. Моль — количество вещества, содержащее
~ 6,02 • 1023 молекул (если вещество состоит из молекул) или = 6,02 • 1023 атомов (если вещество состоит из атомов).
Число Авогадро (NA) — постоянная, показывающая число молекул (атомов) в одном моле любого вещества:
NA = 6,02 • 1023 моль-1
Молярная масса вещества (М) — масса одного моля вещества. Молярная масса вещества в г/моль численно равна относительной молекулярной массе.
Закон Авогадро: в равных объемах различных газов при одинаковых условиях (температуре и давлении) содержится одинаковое число молекул.
Молярный объем газа (Ум) — объем одного моля газа, который при нормальных условиях (273 К и 101,3 кПа) равен 22,4 л (VM° =22,4 л/моль).
Относительная плотность газа X по газу Y — отношение плотности газа X к плотности газа Y, которое равно отношению молекулярных или молярных масс соответствующих газов.
Массовая доля химического элемента X в сложном веществе — отношение суммарной массы атомов элемента X к массе молекулы сложного вещества.
Массовая доля данного вещества (компонента) в смеси веществ — отношение массы компонента к массе смеси.
Объемная доля газа X в смеси газов — отношение объема газа X к объему смеси газов.
Простейшая (эмпирическая) формула вещества — формула, которая показывает простейшие целочисленные соотношения чисел атомов разных элементов в данном веществе (например, простейшей формулой глюкозы С6Н12О6 является СН2О).
Молекулярная (истинная) формула вещества — формула, показывающая реальное число атомов в молекуле вещества (или в его формульной единице, если речь идет о ионных соединениях).
Закон сохранения массы веществ: общая масса всех веществ, вступивших в химическую реакцию, равна общей массе всех продуктов реакции.
Химическое уравнение (уравнение реакции) — письменное выражение химической реакции, в котором указываются формулы исходных веществ и продуктов реакции, а также коэффициенты перед формулами, которые подбираются так, чтобы число атомов каждого элемента в левой и в правой частях уравнения
было одинаковым.
Коэффициенты в уравнении реакции — числа, которые показывают мольные соотношения участвующих в реакции веществ (например, для реакции 2А1 + ЗС12 = 2А1С13 соотношение чисел молей п(А1) : п(С12) : А1С13) = 2:3:2).
Выход продукта реакции (массовая доля выхода) — отношение практически полученной массы (числа молей) вещества к массе (числу молей), теоретически рассчитанной по уравнению реакции.
Элементарные частицы — общее название протонов, нейтронов и электронов, т. е. частиц, из которых состоят атомы.
Нуклоны — общее название протонов и нейтронов, т. е. 'частиц, из которых состоят ядра атомов.
Массовое число атома (А) — сумма числа протонов и нейтронов в данном атоме.
Изотопы — атомы одного элемента, имеющие разные массовые числа.
Атомная орбиталь — часть атомного пространства, в которой вероятность нахождения электрона составляет примерно 90%. В центре каждой орбитали находится ядро атома. Каждый электрон в атоме занимает определенную орбиталь.
Энергетический уровень атома — совокупность орбиталей, близких по размеру и энергии и характеризующихся одинаковым значением главного квантового числа л. Для первого уровня п = 1, для второго — 2, для третьего — 3 и т. д. Число орбиталей на каждом уровне равно п (1 орбиталь на первом уровне, 4 - на втором, 9 - на третьем и т. д.).
Электронный слой атома — совокупность электронов, находящихся на одном энергетическом уровне.
Энергетический подуровень атома — совокупность орбиталей, находящихся на одном энергетическом уровне и имеющих одинаковую геометрическую форму. Число подуровней на энергетическом уровне равно его главному квантовому числу.
s-Подуровень — подуровень, состоящий из одной шарообразной s-орбитали. На каждом энергетическом уровне имеется один
s-подуровень.
р-Подуровень — подуровень, состоящий из трех гантелеоб-разных р-орбиталей, расположенных вдоль осей пространственной системы координат. На каждом энергетическом уровне, кроме первого, имеется по одному р-подуровню.
d-Подуровень — подуровень, состоящий из пяти d-орбиталей. Все уровни, кроме первого и второго, содержат d-подуровень.
f-Подуровень — подуровень, состоящий из семи f-орбиталей. Все уровни, кроме первого, второго и третьего, содержат f-поду-
ровень.
Спин электрона — характеристика электрона, связанная с его вращением вокруг своей оси. Электрон может вращаться по часовой стрелке (спин + 1/2) или против часовой стрелки (спин -1/2). Согласно принципу Паули, на одной орбитали может находиться либо один электрон со спином +1/2 или -1/2 (такой электрон, называется неспаренным), либо максимально два электрона с противоположными (антипараллельными) спинами (такие электроны называются спаренными).
Принцип наименьшей энергии — принцип, в соответствии с которым электроны заполняют энергетические подуровни в порядке увеличения их энергии. Порядок заполнения подуровней: Is — 2s — 2р — 3s — Зр — 4s — 3d —4р — 5s — 4d — 5р —6s - — 4f — 5d — 6p — 7s — 5f — 6d. Другие подуровни в атомах известных элементов не заполняются.
Правило Гунда определяет порядок заполнения орбиталей, находящихся на одном подуровне. Согласно этому правилу, электроны заполняют орбитали одного подуровня таким образом, чтобы число неспаренных электронов было максимальным, причем эти электроны должны иметь параллельные спины.
Основное (невозбужденное) состояние атома — состояние, соответствующее принципу наименьшей энергии и правилу Гунда.
Периодический закон : свойства элементов и образуемых ими соединений находятся в периодической зависимости от заряда ядра атома, или порядкового номера элемента. Периодичность изменения свойств элементов обусловлена тем, что при увеличении порядкового номера последовательно увеличивается общее число электронов в атомах элементов, а число электронов на внешнем электронном слое периодически повторяется.
Период в периодической системе — последовательность расположенных в порядке возрастания заряда ядра элементов, в атомах которых электроны заполняют одинаковое число энергетических уровней. Это число равно номеру периода.
Главная подгруппа (подгруппа А) в периодической системе — вертикальный ряд элементов, атомы которых имеют одинаковое число электронов на внешнем слое. Это число равно номеру группы.
s-Элементы — элементы, в атомах которых последним заполняется электронами s-подуровень внешнего электронного слоя. s-Элементами являются первые два элемента каждого периода.
р-Элементы — элементы, в атомах которых последним заполняется электронами р-подуровень внешнего электронного слоя. р-Элементами являются последние шесть элементов 2—6 периодов.
d-Элементы (переходные элементы) — элементы, в атомах которых последним заполняется электронами d-подуровень пред-внешнего электронного слоя. d-Элементами являются элементы всех побочных подгрупп (подгрупп В).
Электронный октет — конфигурация внешнего слоя атомов благородных газов, включающая 8 электронов (ns2np6).
Металличность элемента — способность его атомов отдавать электроны.
Неметалличность элемента — способность его атомов присоединять электроны.
Электроотрицательность элемента — количественный критерий металличности и неметалличности, характеризующий способность атома данного элемента притягивать к себе электроны, участвующие в образовании химической связи с другим атомом.
Химическая связь — силы, которые обусловливают связывание атомов.
Ковалентная связь — химическая связь, обусловленная образованием общих электронных пар, т. е. перекрыванием электронных облаков (орбиталей).
Валентность элемента — число ковалентных связей, образуемых атомом данного элемента с другими атомами в данной молекуле.
Одинарная (простая) связь — ковалентная связь, образованная одной общей электронной парой.
Кратные связи — связи, образованные двумя или тремя общими электронными парами (соответственно, двойная и тройная связи).
Неполярная связь — ковалентная связь между атомами с одинаковой электроотрицательностью; характеризуется симметричным распределением электронной плотности между ядрами атомов. Как правило, реализуется в молекулах простых веществ (Н2, N2, Gla и др.).
Полярная связь — ковалентная связь между атомами с разной электроотрицательностью; при образовании этой связи электронная плотность смещается к более электроотрицательному атому.
Диполь — система из двух разноименных зарядов, находящихся на определенном расстоянии друг от друга.
Возбужденное состояние атома — это состояние с более высокой энергией, чем основное состояние; возникает в результате перехода электронов с одного подуровня на другой подуровень, имеющий большую энергию.
Гибридизация атомных орбиталей — это смешение атомных орбиталей (электронных облаков) различного типа (например, s-и р-орбиталей), в результате которого образуются одинаковые по форме и энергии гибридные орбитали (например: sp, sp2, sp3op-битали).
Донорно-акцепторная (координационная) связь — ковалентная связь, образующаяся в результате перекрывания орбитали с неподеленной парой электронов атома-донора и свободной орбитали атома-акцептора.
Ионная связь — связь, обусловленная электростатическим притяжением между положительно заряженными ионами (катионами) и отрицательно заряженными ионами (анионами). Простейшие примеры ионных соединений — соединения, образуемые атомами типичных металлов и типичных неметаллов (NaCt, KF, СаО и др.).
Металлическая связь — связь между всеми катионами металлов и всеми свободными электронами в кристаллической решетке простых веществ-металлов.
Степень окисления элемента — это реальный (в случае ионных соединений) или условный (в случае ковалентных соединений) заряд атома данного элемента в данном соединении.
Гидратация в растворах — взаимодействие частиц растворяемого вещества с молекулами воды, не связанное с разрушением этих молекул.
Гидратированные ионы — ионы, связанные с молекулами воды.
Электролитическая диссоциация (ионизация) — процесс распада ионных соединений или соединений с ковалентной полярной связью на ионы; происходит в водных растворах и в расплавах.
Электролиты — вещества, которые в водных растворах и в расплавах диссоциируют на ионы.
Степень электролитической диссоциации — отношение числа молекул, распавшихся на ионы, к общему числу растворенных молекул.
Сильные электролиты — вещества, которые в водных растворах полностью распадаются на ионы (степень диссоциации равна 1).
Слабые электролиты — вещества, которые в водных растворах лишь частично распадаются на ионы (степень диссоциации меньше 1).
Аллотропия — явление образования нескольких простых веществ атомами одного и того же химического элемента.
Оксиды — соединения двух элементов, один из которых кио лород в степени окисления -2 (СаО, СО2, Р2О5 ).
Пероксиды — соединения водорода и некоторых металлов с кислородом в степени окисления -1 (Н2О2, Na2O2, CaO2 и др.).
Гидроксиды (гидраты оксидов) — продукты прямого или косвенного соединения оксидов с водой. Делятся на три типа: основания, кислоты и амфотерные гидроксиды.
Основания (основные гидроксиды) — электролиты, которые при диссоциации образуют катионы металлов и только один вид анионов — гидроксид-ионы ОН - (NaOH, Ca(OH)2, Bi(OH)3 и др.).
Основные оксиды — оксиды, гидраты которых являются основаниями (Na2O, CaO, Bi2O3 и др.).
Кислоты — электролиты, которые при диссоциации образуют только катионы водорода Н+ и анионы кислотных остатков (H2SO4, HNO3, HC1O4 и др.).
Кислотные оксиды — оксиды, гидраты которых являются кислотами (кислотными гидроксидами) (SO3, NOO5, С12О7 и др.).
Амфотерные гидроксиды — электролиты, способные диссоциировать как по типу оснований, так и по типу кислот (Zn(OH)2, А1(ОН)3 и др.).
Амфотерные оксиды — оксиды, гидраты которых являются амфотерными гидроксидами (ZnO, A12O3 и др.).
Солеобразующие оксиды — общее название основных, кислотных и амфотерных оксидов, которые образуют соли при взаимодействии с кислотами или с основаниями.
Несолеобразующие (безразличные, индифферентные) оксиды — оксиды, которые не образуют ни гидратов, ни солей (N2O, NO, CO, SiO).
Кислотность основания — число гидроксидных групп в молекуле (формульной единице) основания.
Щелочи — растворимые в воде основания. Наиболее известными щелочами являются гидроксиды щелочных и щелочноземельных металлов (NaOH, Ca(OH)2 и др.).
Основность кислоты — число атомов водорода в молекуле кислоты, которые могут отщепляться в виде ионов Н+.
Кислородсодержащие кислоты — гидраты кислотных оксидов (H2SO4, HNO3, H3PO4 и др.).
Бескислородные кислоты — водные растворы газообразных нодородных соединений некоторых неметаллов (НС1, HBr, H2S и
др.).
Реакция нейтрализации — взаимодействие между кислотой и основанием, в результате которого образуются соль и вода (например: НС1 + NaOH=NaCl + Н2О). Реакции нейтрализации относятся к типу реакций обмена.
Реакции обмена — реакции, в ходе которых исходные сложные вещества обмениваются своими составными частями и образуют новые сложные вещества; происходят без изменения степеней окисления элементов.
Нормальные (средние) соли — продукты полного замещения атомом водорода в молекулах кислот атомами металла или продукты полного замещения гидроксидных групп в молекулах оснований кислотными остатками (NaCl, FeBr3, A12(SO4)3 и др.).
Кислые соли — продукты неполного замещения атомов водорода в молекулах многоосновных кислот атомами металла (NaHCO3, CaHPO4, Са(Н2РО4)2 и др.).
Основные соли — продукты неполного замещения гидроксидных групп в молекулах многокислотных оснований кислотными остатками (CuOHCl, A1(OH)2NO3 и др.).
Смешанные соли — соли, состоящие из катионов одного металла и анионов двух различных кислотных остатков (PbFCl, Са(С1О)С1 и др.).
Двойные соли — соли, состоящие из катионов двух различных металлов (аммония) и анионов одной кислоты (KA1(SO4)2, NH4Fe(SO4)2 и др.).
Комплексные соли — соли, состоящие из катионов металла и комплексных анионов (K4[Fe(CN)6] , Na2[PtCl6] и др.) или из комплексных катионов и анионов кислотных остатков.
РАЗДЕЛ 5. Практикум по решению задач (практических ситуаций) по темам лекций.
5.1 Алгоритмы решения задач
Алгоритм 1. Метод суммарного уравнения параллельных реакций
1. Написать, что дано и что необходимо найти.
2. Написать схемы параллельных реакций, расставить коэффициенты.
3. Написать суммарное уравнение:
– только химические формулы задействованных веществ с соответствующими коэффициентами;
– коэффициенты перед одинаковыми химическими формулами суммируются.
Пример1. Некоторое количество углеводорода состава CnH2n–2 дает с избытком хлора 21,0 г тетрахлорида. То же количество углеводорода с избытком брома дает 38,8 г тетрабромида. Напишите молекулярную формулу всех его возможных изомеров.
а) п. 1. Дано:
CnH2n–2,
M(CnH2n–2Cl4) = 21,0 г,
M(CnH2n–2Br4) = 38,8 г. Найти: химическая формула – ?
б) п. 2. CnH2n–2 + 2Сl2 = CnH2n–2Сl4,
CnH2n–2 + 2Br2 = CnH2n–2Br4.
в) п. 3. 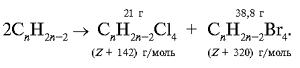
Обозначим M(CnH2n–2) = Z.
Решаем полученную пропорцию: 21/(Z + 142) = 38,8/(Z + 320), Z = 68.
Найдем индекс n: M(CnH2n–2) = 12n + 2n – 2,
12n + 2n – 2 = 68, n = 5. Ответ. С5Н8.
Алгоритм 2. Насыщенные растворы
1. Записать, что дано и что необходимо найти.2. Составить первую пропорцию, используя определение коэффициента растворимости Краств3. Составить вторую пропорцию, исходя из первой и данных задачи:

Решить пропорцию относительно х. Записать ответ (при решении обратных задач составляется такая же схема)Для газов растворимость понижается при нагревании. Растворимость (коэффициент растворимости Kраств) – количество вещества (в г), которое может раствориться в 100 г растворителя при определенной температуре, образуя насыщенный раствор.
Пример 1. Коэффициент растворимости соли при температуре 50 °С равен 40 г, при температуре 10 °С составляет 15 г. Определите массу осадка, полученного при охлаждении насыщенного при температуре 50 °С раствора массой 70 г до температуры 10 °С.
а) п. 1. Дано:
Kраств(соли) при t = 50 °С – 40 г,
Kраств(соли) при t = 10 °С – 15 г,
m(насыщ. р-ра) при t = 50 °С – 70 г. Найти: m (осадка) при 10 °С – ?
б) п. 2.
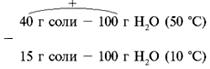
в) п. 3.
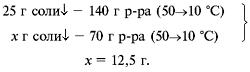
Ответ. m(осадка) при охлаждении равна 12,5 г.
Пример 2. При н. у. в воде массой 100 г растворяется хлороводород объемом 50,5 л. При температуре 50 °С и нормальном давлении коэффициент растворимости хлороводорода равен 59,6 г. Насыщенный при температуре 0 °С раствор HCl массой 40 г нагрели до температуры 50 °С. Определите массу полученного раствора.
а) п. 1. Дано:
V(HCl) = 50,5 л (н. у.),
Kраств(HCl) = 59,6 г (50 °С, 1 атм),
m(насыщ. р-ра) = 40 г (0 °С). Найти: m(р-ра HCl) – ?
б) п. 2.
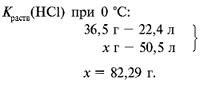
в) п. 3.
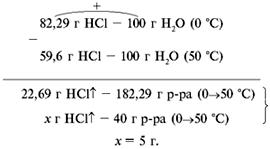
5 г HCl улетучится при нагревании. Ответ. m(полученного р-ра HCl) = 40 – 5 = 35 г.
Пример 3. В воде массой 100 г растворяется при температуре 30 °С бромид аммония массой 81,8 г. При охлаждении насыщенного при температуре 30 °С раствора NH4Br массой 300 г до температуры 0 °С выпадает в осадок соль массой 36,8 г. Определите, какая масса бромида аммония может быть растворена в воде массой 100 г при t = 0 °С.
а) п. 1. Дано:
Kраств = 81,8 г (30 °С),
m(насыщ. р-ра) = 300 г (30 °С),
m(осадка) = 36,8 г (0 °С). Найти: K'раств(0 °С) – ?
б) п. 2.
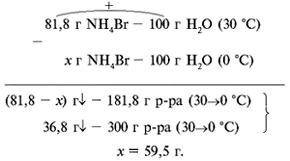
Ответ. K'раств(0 °С) = 59,5 г.
Алгоритм 3.
Расстановка коэффициентов методом полуреакций
(электронно-ионный баланс)
1. В уравнении окислительно-восстановительной реакции определить элементы, которые меняют степень окисления.
2. Составить электронно-ионный баланс с учетом среды:
– малодиссоциирующие вещества, недиссоциирующие вещества на ионы не расписывают;
– в кислой среде в реакции могут участвовать Н+ и Н2О;
– в щелочной среде – ОН– и Н2О;
– в нейтральной среде – Н2О, Н+ и ОН–.
3. Записать сокращенное ионное уравнение согласно электронно-ионному балансу:
– суммировать процессы окисления и восстановления с учетом равенства электронов в этих процессах;
– сократить справа и слева в химическом уравнении одинаковые ионы, молекулы.
4. Записать уравнение в молекулярной форме по ионному уравнению, дописать формулы веществ, которые в электронно-ионном балансе не были задействованы.
5. Проверить коэффициенты в молекулярном уравнении.
Пример 4. Расставить коэффициенты методом электронно-ионного баланса: H2S + K2Cr2O7 + H2SO4 = S Cr2(SO4)3 + H2O + K2SO4.
а) п. 1.
![]()
б) п. 2.
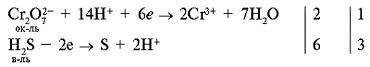
в) п. 3.
![]()
г) п. 4, п. 5. Ответ. 3H2S + K2Cr2O7 + 4H2SO4 = 3S + Cr2(SO4)3 + 7H2O + K2SO4.
http://*****/
РАЗДЕЛ 6. Изменения в рабочей программе, которые произошли после
утверждения программы.
Характер изменений в программе | Номер и дата протокола заседания кафедры, на котором было принято данное решение | Подпись заведующего кафедрой, утверждающего внесенное изменение | Подпись декана факультета (проректора по учебной работе), утверждающего данное изменение |
РАЗДЕЛ 7. Учебные занятия по дисциплине ведут:
Ф. И.О., ученое звание и степень преподавателя | Учебный год | Факультет | Специальность |
|
Ст. преподаватель | 2005/2006 | Естественно-географический | 032400- Биология-География |
|
Ст. преподаватель | 2006/2007 | Естественно-географический | 050102- Биология |
|
Ст. преподаватель | 2007/2008 | Естественно-географический | 050102- Биология-География 050102- Биология |
|
Ст. преподаватель | 2008/2009 | Естественно-географический | 050102- Биология |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



