Влияние катализатора на скорость реакции изучают на примере реакции восстановления перманганата калия.
Таблица 3
Номер пробирки | Количество смеси KMnO4+H2SO4, см3 | Количество гранул Zn, шт. | Объем KNO3, см3 | Время обесцвечивания, τ, с |
1 | 5,5 | 1 | 0,5 | |
2 | 5,5 | 1 | - | |
3 | 5,5 | - | - |
В присутствии катализатора (KNO3) реакции протекают следующим образом:
1. КМО3(катализатор) + Zn + H2SO4= KNO2+ H2O + ZnSO4, или
KNO3 + 2H0(Zn, H2SO4 разб) = KNO2 + H2O
2. 2KMnO4 + 5KNO2 + 3H2SO4 = 2MnSO4 + K2SO4 + 3H2O + 5KNO3 (катализатор)
Для подтверждения реакционной способности KNO2 прилейте в третью пробирку 0,5 см3 1 н раствора KNO2. Наблюдайте обесцвечивание раствора. Сделайте вывод о влиянии катализатора на скорость реакции.
Опыт 4. Влияние концентрации реагирующих веществ на химическое равновесие
Влияние концентрации реагирующих веществ на состояние химического равновесия изучают на примере взаимодействия хлорида железа (III) с роданидом калия
Лабораторная работа № 5 (2ч.)
ТЕМА: ПРИГОТОВЛЕНИЕ РАСТВОРОВ
Цели работы — приготовление растворов кислот и солей различной концентрации.
Приборы и реактивы: весы, ареометр для жидкостей тяжелее воды, ступка с пестиком, мерная колба емкостью 250мл, мерные цилиндры 50 и 250мл, цилиндр высокий узкий, стаканы 100мл (2 шт.) и 300мл (1шт.), воронка, стеклянная палочка, ложки (2шт), банки для сливания растворов; хлорид бария (тв.), карбонат натрия (кристалл.), растворы: серная кислота (пл. 1,84), соляная кислота (пл. 1,19), гидроксид натрия (40%).
Опыт 1. Приготовление растворов процентной концентрации.
Задание. Приготовить 200г 5-%- ного раствора карбоната натрия из кристаллической соды Na2CO3 . 10 Н2О и воды.
Вычислить, какое количество Na2СОз . 10 Н2О требуется для приготовления 200г 5-%-ного раствора в расчете на безводную соль Nа2СОз.
Отвесить это количество измельченной соды в предварительно взвешенном стаканчике на технохимических весах с точностью до 0,01г.
Рассчитать, какой объем воды необходим для растворения взятой навески. Отмерить мерным цилиндром этот объем воды.
Вылить воду в стакан и растворить в ней отвешенную соль.
* Вылить раствор в сухой высокий узкий цилиндр и опустить в него ареометр так, чтобы он не касался стенок сосуда. Отметить то деление шкалы, которое совпадает с уровнем жидкости в цилиндре, произведя расчет по шкале сверху вниз. ( Ареометр промыть водой, осторожно вытереть досуха и сдать лаборанту).
Раствор вылить в приготовленную склянку.
Задание. Рассчитать молярность приготовленного раствора, используя найденную плотность.
Опыт 2. Приготовление молярных растворов.
Задание. Приготовить 250мл 1М раствора соляной (серной) кислоты из раствора, имеющегося в лаборатории.
Определить ареометром плотность раствора кислоты.
По найденной плотности, определить процентную концентрацию данного раствора, вычислить навеску, а затем объем этого раствора, необходимый для приготовления заданного раствора.
Налить в мерную колбу 250мл около половины её объема воды и влить в неё ( в случае серной кислоты - тонкой струей, осторожно!) через воронку вычисленный объём раствора кислоты, отмеренный цилиндром. Осторожно перемешать полученный раствор и охладить его до комнатной температуры. Долить колбу водой до метки, закрыть пробкой и хорошо перемешать.
* Вылить полученный раствор в сухой высокий цилиндр, определить ареометром его плотность и затем вылить в приготовленную склянку.
Задание. Вычислить процентную и молярную концентрации, сравнить вычисленную молярность с заданной, установить точность выполнения опыта.
Лабораторная работа № 6 (2 ч.)
ТЕМА: РЕАКЦИИ В РАСТВОРАХ ЭЛЕКТРОЛИТОВ
Цели работы — изучить особенности протекания химических процессов в растворах электролитов.
Приборы и реактивы: штатив с пробирками, шпатель; растворы: сульфат натрия Na2SO4, сульфат калия K2SO4, сульфат цинка ZnSО4, хлорид бария ВаСl2, гидроксид натрия NaOH, соляная кислота НС1, карбонат натрия Na2 СО3, карбонат калия К2СО3, хлорид цинка
ZnСl2, мрамор СаСОз, фенолфталеин, образцы растворов в пронумерованных пробирках, индикаторная бумага.
Опыт 1. Реакции, идущие с образованием нерастворимых и труднорастворимых веществ.
Опыт 2. Реакции, идущие с образованием слабого электролита.
Опыт 3. Реакции, протекающие с образованием малодиссоциирующих веществ.
Опыт 4. Реакции, идущие с образованием летучего соединения.
Задание. Заполните таблицу. Объясните наблюдаемые явления. Напишите уравнения реакций молекулярном и ионном виде.
№ | Название опыта | Наблюдения | Уравнения реакций |
Выводы: |
Контрольные вопросы
1. Какие вещества называют электролитами? Чем отличаются их водные растворы от растворов неэлектролитов?
2. Какими условиями определяется возможность электролитической диссоциации вещества? Какая величина характеризует ионизирующую способность растворителя? Покажите механизм распада частиц растворенного вещества на ионы.
3. Какие величины являются количественной характеристикой процесса электролитической диссоциации? Дайте их определения. Какую из них называют постоянной величиной и почему?
4. На какие группы условно разделяются электролиты по степени диссоциации? Приведите примеры представителей этих групп.
5. Как и почему на степень диссоциации слабого электролита влияют введение в его раствор одноименного иона и разбавление раствора?
6. Как способность электролитов к диссоциации зависит от вида химической связи?
7. Концентрация каких ионов в растворах солей KHSO3 и КН2РО4 больше и каких меньше?
8. Какие гидроксиды называются амфотерными?
9. Составьте ионно-молекулярные уравнения следующих реакций:
a) AI2(SO4)3 + Pb(NO3)2 → г) HCN + NaOH →
6) ZnS + HCl → д) Сu (ОН)2 +Na2S→
в) Fe(OH)3+ HNO3 → e) Cu(OH)2 + H2S →
10. Составьте молекулярные уравнения к следующим ионно-молекулярным уравнениям:
а) Рb2+ + 2I-→ г) HCN + ОН-→
б) Са2+ + СО3 2-→ д) Сu2+ + 2ОН-→
в) NH4OH + Н+ → е) CN - + Н+ →
Лабораторная работа № 7
(2ч.)
ТЕМА: ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Цели работы — изучить окислительно-восстановительную способность металлов и их ионов.
Опыт 1. Окислительно-восстановительная способность металлов и их ионов.
Опыт 2. Окислительные свойства иона Fe3+ .
Опыт 3. Восстановительные свойства иона Fe2+ .
Опыт 4. Окисление ионов Сг3+ пероксидом водорода.
Опыт 5. Окисление ионов Fe2+ ионами МnО4- .
Задание: составить для всех реакций окислительные и восстановительные полуреакции; рассчитать ЭДС, ∆G° и константу равновесия реакций, используя стандартные электродные.
Контрольные вопросы
1. Типы окислительно- восстановительных реакций (ОВР).
2. Стандартные окислительно-восстановительные потенциалы.
3. Направление протекания окислительно-восстановительных реакций.
4. Роль среды в ОВР.
5. Подберите коэффициенты в уравнениях химических методами электронного и электронно-ионного баланса:
а) Аg + HNO3, конц. →
Аg + HNO3, разб. →
Mg + HNO3, конц. →
Mg + HNO3, разб. →
Mg + HNO3, очень разб. →
б) NaOH +S = Na2S+Na2SO3
BaCrO4 =BaO +Cr2O3 +O2
Na2SO3 + KMnO4 +KOH = Na2SO4 + K2MnO4 +H2O
FeSO4 + KMnO4+H2SO4 = Fe2(SO4)3 +MnSO4 + K2SO4 + H2O
Na2SO3 + KMnO4 +H2O = Na2SO4 + MnO2 + KOH
H2S + K2Cr2O7 + H2SO4 = K2SO4 +Cr2(SO4)3 + H2O
Лабораторная работа № 8 (2ч.)
Тема: Свойства растворов сильных и слабых электролитов.
Цели работы — сравнить химическую активность кислот; изучить влияние одноименных ионов на направление диссоциации слабых электролитов; изучить свойства амфотерных электролитов; осуществить ионообменные реакции образования труднорастворимых и малодиссоциирующих веществ.
Опыт 1. Сравнение химической активности кислот.
а) Взаимодействие соляной и уксусной кислот с мрамором.
б) Взаимодействие соляной и уксусной кислоты с цинком.
Опыт 2. Смещение равновесия диссоциации слабого электролита.
а) Влияние соли слабой кислоты на степень диссоциации кислоты.
б) Влияние соли слабого основания на степень диссоциации этого основания.
Опыт 3. Влияние соли слабой кислоты на степень диссоциации сильных кислот.
Опыт 4. Амфотерные электролиты.
Контрольные вопросы
1. Какие вещества называют электролитами? Чем отличаются их водные растворы от растворов неэлектролитов?
2. Какими условиями определяется возможность электролитической диссоциации вещества? Какая величина характеризует ионизирующую способность растворителя? Покажите механизм распада частиц растворенного вещества на ионы.
3. Какие величины являются количественной характеристикой процесса электролитической диссоциации? Дайте их определения. Какую из них называют постоянной величиной и почему?
4. На какие группы условно разделяются электролиты по степени диссоциации? Приведите примеры представителей этих групп.
5. Как и почему на степень диссоциации слабого электролита влияют введение в его раствор одноименного иона и разбавление раствора?
6. Как способность электролитов к диссоциации зависит от вида химической связи?
7. По какому признаку согласно теории электролитической диссоциации вещества классифицируются на кислоты, основания и соли? Почему гидросоли и гидроксосоли можно назвать промежуточными соединениями?
8. Что называется ступенчатой диссоциацией? Чем определяется число ступеней для многоосновных кислот и многокислотных оснований? Как и почему изменяются значения α и Кд, от первой ступени к последней? Напишите уравнение ступенчатой диссоциации мышьяковой кислоты H3AsО4.
9. Как вычислить степень диссоциации бинарного электролита, если известны константа диссоциации и молярная концентрация раствора?
10. Концентрация каких ионов в растворах солей KHSO3 и КН2РО4 больше и каких меньше?
11. Какой из растворов при одинаковой молярной концентрации содержит больше ионов СН3СОО-: СН3СООН или CH3COONa?
12. Какие гидроксиды называются амфотерными?
13. Составьте ионно-молекулярные уравнения следующих реакций:
a) AI2(SO4)3 + Pb(NO3)2 → г) HCN + NaOH →
6) ZnS + HCl → д) Сu (ОН)2 +Na2S→
в) Fe(OH)3+ HNO3 → e) Cu(OH)2 + H2S →
14. Составьте молекулярные уравнения к следующим ионно-молекулярным уравнениям:
а) Рb2+ + 2I-→ г) HCN + ОН-→
б) Са2+ + СО3 2-→ д) Сu2+ + 2ОН-→
в) NH4OH + Н+ → е) CN - + Н+ →
Лабораторная работа № 9 (2ч.)
Тема: Гидролиз солей.
Цели работы — изучить гидролиз солей разного типа; определить реакцию среды при помощи индикаторов; изучить влияние температуры и относительной силы электролита на степень гидролиза.
Опыт 1. Определение рН при помощи универсального индикатора
В четыре пробирки налейте по 5-8 капель 0,1 М растворов: в одну — соляной кислоты НCl, в другую — уксусной кислоты СН3СООН, в третью — аммиака NH4OH, в четвертую — дистиллированной воды. В каждую пробирку добавьте по 1 капле универсального индикатора РКС и по таблице цветности универсального индикатора сравните полученную окраску с окраской эталонных растворов.
Таблица цветности универсального индикатора
Интервал | рН | Цвет индикатора | Интервал | рН | Цвет индикатора |
1,0 | Малиновый | 6,0 | Зеленовато-желтый | ||
2,0 | Розово-оранжевый | 7,0 | Желто-зеленый | ||
3,0 | Оранжевый | 8,0 | Зеленый | ||
4,0 | Желто-оранжевый | 9,0 | Сине-зеленый | ||
5,0 | Желтый | 10,0 | Серовато-синий |
Результаты опыта запишите в виде таблицы:
Испытуемый раствор | Цвет раствора | рН |
Опыт 2. Реакция среды растворов солей при гидролизе.
Результаты испытаний представьте в виде таблицы:
№ | Формула и название соли | Окраска индикатора | Реакция среды раствора | Уравнения реакций |
Опыт 3. Обратимый (неполный) гидролиз солей
Опыт 4. Факторы, влияющие на степень гидролиза
а) Влияние относительной силы электролита.
б) Влияние температуры.
Опыт 5. Необратимый (полный) гидролиз солей
Контрольные вопросы
Что называется водородным показателем? Как изменяется величина водородного показателя в кислой среде? в щелочной среде? Почему окраска индикатора изменяется при изменении реакции среды? Что называется гидролизом солей? Какие соли подвергаются гидролизу? Как можно усилить гидролиз? замедлить гидролиз? Что показывает степень гидролиза? От каких факторов зависит степень гидролиза? В какой области находится рН водных растворов солей А1С13, Na3PO4, NaHCO3, K2S? Какую реакцию среды будут иметь следующие растворы солей: Na2S, Zn(NO3)2, KNO3, CuSO4, Cr2(SO4)3? Для солей, подвергающихся гидролизу, составьте молекулярные и ионные уравнения реакций.Лабораторная работа № 10 (2ч.)
Тема: Комплексные соединения.
Цели работы — получить комплексные соединения, изучить их свойства и методы разрушения; научиться различать комплексные и двойные соли.
Опыт 1. Образование аммиакатов меди
Опыт 2. Образование аммиакатов серебра
Опыт 3. Получение соединения, содержащего в молекуле комплексные катион и анион
Опыт 4. Комплексные соединения в реакциях обмена. Взаимодействие гексацианоферрата (III) калия K3[Fe(CN)6] с сульфатом меди (II)
Опыт 5. Разрушение комплексных ионов
Опыт 6. Диссоциация двойной соли
Опыт 7. Диссоциация гексацианоферрата (III) калия
Контрольные вопросы
1. Какие соединения называются комплексными?
2. Что такое комплексообразователь? лиганды?
3. Что такое внутренняя сфера? внешняя сфера?
4. Каким ионам свойственна роль комплексообразователя?
5. Какие молекулы и ионы являются лигандами (аддендами)?
6. Имеется ли различие между двойными и комплексными солями?
7. Какие комплексные соединения называются однородными? неоднородными?
8. Определите валентность комплексообразователей, координационные числа и заряды комплексных ионов в соединениях:
[Cd(NH3)4](OH)2; К3[Со(NО2)2]; Cu2[Fe(CN)6].
9. Из каких солей можно получить K3 [Fe(CN)6]? Напишите уравнение реакции.
10. Напишите формулу комплексного соединения, состоящего из ионов К+, Cd2+, CN-. Координационное число кадмия равно 4.
11. Координационное число кобальта Со3+ (как комплексообразователя) равно 6. Укажите состав комплексных ионов в солях CoCl3•6NH3, CoCl3•5NH3 и CoCl3•4NH3. Напишите уравнения их диссоциации в водных растворах.
12. Координационное число двухвалентной меди равно 4. Составьте формулы аммиачного и цианистого комплексов двухвалентной меди, укажите их валентности и приведите примеры солей, в состав которых входили бы эти комплексные ионы.
1.7.3 Перечень примерных контрольных вопросов и заданий
для самостоятельной работы.
Задание 1.
1. Атомы каких из приведенных элементов являются изобарами:
402
а. 20 Ca и 20Ca; b. 18 Ar и 19K; c. 48Cd и 50Sn; d. 54Xe и 56Ba?
2. Укажите математическое выражение принципа неопределенности :
а. l = ![]() b. DE = hn; c.
b. DE = hn; c.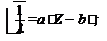 d. D x D v ³
d. D x D v ³ ![]()
3. Какие частицы являются изоэлектронными :
a. Ca2+ ; b. Si4+; c. Ar ; d. Cl - ?
4. Какой подуровень в атомах - 3d или 3p и 6s или 5d - заполняется раньше:
a. 3d и 6; b. 3p и 6s; c. 3d и 5d; d. 3p и 5d?
5. Какова конфигурация валентных электронов в атоме технеция:
a. ...5s2 p5; b. ...4d6 5s1; c. ...4d5 5s2; d....4d25s2 p3?
6. Сколько свободных 3d-орбиталей в атоме хрома:
7. Какие из электронных конфигураций соответствуют возбужденным состояниям:
a. ...2s2; b. ...3s2 3d1; c. ... 4s2 3d2; d. ... 1s2 2s2 p6 3p1?
8. Сколько электронов находится на 4d - подуровне атома гафния
9. Атомы каких элементов - актиноидов имеют наибольшее число неспаренных f-электронов:
a. Pu; b. Am; c. Cm; d. Bk?
10. Какой из переходов электрона в атоме водорода требует поглощения фотона с минимальной энергией:
a. 1s ---> 2p; b. 1s ----> 4d; c. 2s ---> 4s; d. 2p ---> 3s?
2. Какое уравнение характеризует корпускулярно-волновую природу электрона:
a. DE = h n; b. HY = E Y; c. l = h /mv; d. E = -13.6/ n2?
3. Укажите, какие из указанных частиц являются изоэлектронными:
a. Al3+; b. P3-; c. S; d. Cl-?
4. Какие значения всех квантовых чисел (n, ml, m, ms) возможны для валентного электрона атома калия:
a. 4, 1, -1 , - 1/2; b. 4, 1 , +1 , +1/2; c. 4, 0, 0, + 1/2; d. 5, 0, +1, +1/2?
5. Вычислите энергию (Дж), необходимую для перехода электрона атома водорода из состояния, характеризующегося n= 1, в состояние с n3 :
a. 1.5; b. 0.2.10-18; c. 1.9; d. 12 .
Задание 2.
а) Определить степени окисления хрома, фосфора, марганца, иода в следующих солях кальция: CrO4 , CaCr2 O7 , Ca 2P2 O7 , Ca (MnO4)2 , Ca MnO3 , CaMnO4 , CaH3 JO6.
CrO4 , CaCr2 O7 , Ca 2P2 O7 , Ca (MnO4)2 , Ca MnO3 , CaMnO4 , CaH3 JO6.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



