Лабораторная работа № 9
ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ И ЭЛЕКТРОЛИЗ
Цель работы: Ознакомление с устройством гальванических элементов и электролизом растворов электролитов.
Опыт 1. Работа гальванического элемента Якоби-Даниэля.
В один химический стакан налить не менее ½ объема 1 М раствор сульфата меди, в другой не менее ½ объема 1 М раствор сульфата цинка. Собрать гальванический элемент и измерить его ЭДС вольтметром. Сделать рисунок гальванического элемента, написать его электрохимическую схему и реакции, протекающие на электродах (в ионном виде). Рассчитать ЭДС данного гальванического элемента.
Опыт 2. Концентрационный гальванический элемент.
Записать электрохимическую схему концентрационного гальванического элемента на основе двух металлических электродов (электроды определяет преподаватель). Составить уравнения реакций, протекающих на электродах (в ионном виде). Рассчитать теоретическое значение ЭДС данного гальванического элемента.
Опыт 3. Электролиз раствора хлорида меди (II).
Налейте в U-образную трубку 0,5 М раствор хлорида меди (II) примерно до половины обьема. Вставьте в оба колена трубки графитовые электроды. Присоедините электроды к источнику постоянного тока и пропускайте ток около 5 минут. Выключите ток и рассмотрите катод, убедитесь в том, что на нем выделилась медь. Составьте схему электролиза и уравнения реакций, протекающих на электродах.
Опыт 4. Электролиз раствора сульфата натрия.
Налейте в U-образную трубку 0,5 М раствор сульфата натрия. Измерьте с помощью универсальной индикаторной бумаги реакцию раствора (если цвет бумаги не меняется, раствор имеет нейтральную реакцию, рН = 7). Погрузите в трубки графитовые электроды. Включите ток и пропускайте его около 5 минут. Наблюдайте выделение пузырьков газа на электродах. Выньте один электрод из трубки и прикоснитесь к нижнему концу электрода полоской индикаторной бумаги. Если она окрашивается в красноватый цвет – реакция раствора кислая (рН<7), если в зеленоватый – щелочная (рН>7). Отметьте реакцию раствора у анода и катода. Составьте схему электролиза и уравнения реакций, протекающих на электродах.
Опыт 5. Электролиз раствора серной кислоты с медным анодом.
Налейте в U-образную трубку 1 М раствор серной кислоты. Вставьте в оба колена трубки электроды, один графитовый, другой медный. Графитовый электрод соедините с катодом, а медный – с анодом источника тока. Включите ток. Во время электролиза наблюдайте за процессом, протекающим на катоде. Обратите внимание на то, что в начале опыта на катоде выделяются пузырьки газа, затем по мере окрашивания раствора в голубой цвет скорость выделения газа уменьшается и одновременно катод начинает покрываться слоем меди. Дайте объяснение этим явлениям и составьте уравнения реакций, протекающих на аноде и катоде.
СБОРНИК КОНТРОЛЬНЫХ ЗАДАНИЙ
. Контрольная работа 1. Способы выражения концентрации растворов. Расчёты концентраций растворов.
Вариант 1
1. К 1000 г 80%-ной уксусной кислоты прибавлено 3л воды. Найти процентную концентрацию раствора.
2. Сколько граммов нитрата алюминия содержится в 3 л 2 Н раствора этой соли?
3. Рассчитать нормальность раствора 20%-ной серной кислоты плотностью 1,14 г/мл.
4. Сколько граммов фосфорной кислоты надо взять для приготовления 500 мл 0,02 Н раствора?
5. На реакцию с хлоридом калия, содержащимся в 10 мл раствора, израсходовано 45 мл 0,02 Н раствора нитрата серебра. Сколько хлорида калия содержится в 1 литре раствора?
Вариант 2
1. Определить процентную концентрацию 6 Н раствора серной кислоты, если плотность раствора равна 1,18 г/мл?
2. Сколько мл 70%-го раствора нитрата калия плотностью 1,6 г/мл нужно взять, чтобы приготовить 0,5 л 0,2 Н раствора?
3. Определить титр раствора гидроксида натрия, если на титрование 20 мл его потребовалось 50 мл 0,3 Н раствора соляной кислоты?
4. Сколько граммов сульфата меди нужно взять для приготовления 400 мл 0,6 Н раствора?
5. Для полной нейтрализации 1 г некоторой двухосновной кислоты потребовалось 111,1 мл 0,2 Н раствора гидроксида натрия. Найти молекулярную массу кислоты.
Вариант 3
1. Сколько граммов 10-ти водного сульфата натрия нужно растворить в 250 г воды для получения 5%-го раствора безводной соли?
2. Определить молярность раствора фосфорной кислоты, если 6 г её содержится в 150 мл раствора.
3. Рассчитать молярность раствора азотной кислоты, концентрацией 23,3% и плотностью 1,14 г/мл.
4. Сколько мл 70%-го раствора нитрата калия, плотность которого 1,6 г/мл, нужно взять для приготовления 0,5 л 0,2 Н раствора?
5. Сколько мл воды приходится на 28 г КОН в его 1 моляльном растворе?
Вариант 4
1. Вычислить нормальность 50%-го раствора гидроксида натрия плотностью 1,54 г/мл.
2. Сколько мл 20%-го раствора азотной кислоты плотностью 1,115 г/мл, потребуется для нейтрализации раствора, содержащего 16 г гидроксида натрия?
3. Вычислить молярность 10%-го раствора азотной кислоты плотностью 1,056 г/мл.
4. Сколько мл 0,12 Н раствора соляной кислоты потребовалось для полной нейтрализации 15 мл 0,1 Н раствора гидроксида натрия?
5. Определить титр 10% раствора КОН, плотность которого 1,09 г/мл.
Вариант 5
1. В 100 г воды содержится 114,1 г хлорида кадмия. Вычислить процентную и моляльную концентрацию раствора.
2. Вычислить нормальную концентрацию раствора иодида калия, 1 мл которого содержит 0,0017 г иодида калия.
3. Рассчитайте моляльность 40%-го раствора хлорида магния.
4. Сколько граммов серной кислоты содержится в 1 мл 0,1 Н раствора?
5. Сколько граммов хлорида натрия нужно растворить в 500 г воды, чтобы получить 0,5 моляльный раствор?
Контрольная работа 2. Термодинамический расчет химической реакции.
вариант 1
Вычислите при какой температуре начнется диссоциация пентахлорида фосфора, протекающая по уравнению:
PCl5(г) = PCl3(г) + Cl2(г)
вариант 2
Вычислите изменение энергии Гиббса реакции, протекающей по уравнению:
СО(Г) + 3Н2(Г) = СН4(Г) + Н2О(Г). Возможна ли эта реакция при температуре минус 70 0С?
вариант 3
Определить ![]() G0298 реакции, протекающей по уравнению:
G0298 реакции, протекающей по уравнению:
4NH3(г) + 502(г) = 4NO(г) + 6H2O(г) .Вычисления сделать на основании ![]() Н0 и S0 соответствующих веществ. Возможна ли эта реакция при стандартных условиях?
Н0 и S0 соответствующих веществ. Возможна ли эта реакция при стандартных условиях?
вариант 4
Рассчитайте тепловой эффект (кДж) реакции взаимодействия 3 литров водорода с кислородом.
вариант 5
Рассчитайте тепловой эффект (кДж) реакции взаимодействия 10 м3 водорода с кислородом.
Контрольная работа 3. Кинетический расчет химической реакции.
ВАРИАНТ 1
1. Константа скорости реакции 2A(ж) + B(ж) <==> C(ж) равна 0,8. Начальные концентрации веществ А и В равны соответственно 2,5 и 1,5 моль/л. В результате реакции концентрация вещества В составила 0,5 моль/л. Какой стала концентрация вещества А и чему стала равна скорость данной реакции?
2. Перечислить все факторы, которыми можно увеличить выход SO3 по реакции:
2SO2(г) + O2(г) <==> 2SO3(г) + 192 кДж.
3. Скорость реакции при tо = 20 оС равна 1. Чему равна скорость этой реакции при tо = 50 C, если ![]() = 3,5 ?
= 3,5 ?
ВАРИАНТ 2
1. Равновесная концентрация вещества В составляет 5 моль/л. Какое количество вещества А вступает в реакцию, если начальная концентрация вещества В равна 8 моль/л. А + 2В <==> С.
После окончания реакции концентрация вещества А равна 2 моль/л.
2. Напишите закон действия масс для реакции: CO(г) + Cl2(г) --> COCl2(г). Как изменится скорость реакции, если объем системы уменьшить вдвое.
3. При температуре 60оС скорость реакции составляет 0,64 моль/л. с. Какова скорость реакции при 10оС, если температурный коэффициент скорости реакции равен 2 ?
ВАРИАНТ 3
1. В реакции CO(г) + H2О(г) <==> CO2(г) + H2(г) равновесие установилось при концентрациях [CO] = 0,04 моль/л, [H2О] = 0,16 м/л, [H2] = 0,08 моль/л, [CO2] = 0,08 моль/л. Вычислить Кр и исходные концентрации [CO] и [H2О].
2. Как повлияет на равновесие реакции 2H2(г)+ O2(г) <==>2H2О(г) + 483,6 кДж
а) увеличение температуры, б) повышение давления?
3. Две реакции протекают при 25оС с одинаковой скоростью. Температурный коэффициент скорости первой реакции равен 2,0 ; а второй 2,5. Найти отношение скоростей этих реакций при 95оС.
ВАРИАНТ 4
1. При состоянии равновесия системы N2 + 3H2 <==> 2NH3 концентрации участвующих в реакции веществ равны [N2] = 3 моль/л, [H2] = 9 моль/л, [NH3] = 4 моль/л. Каковы были исходные концентрации азота и водорода?
2. Как сместить равновесие в реакции N2 (г) + 3H2 (г) <==> 2NH3 (г) + 92,4 кДж в прямом направлении.
3. Скорость реакции при 0оС равна 1. Чему равна скорость этой реакции при 200°С, если ![]() = 2 ?
= 2 ?
ВАРИАНТ 5
1. Через некоторое время после начала реакции: 3 А + В <==> 2 C концентрации веществ составляли [А] = 3 моль/л, [В] = 1 моль/л,[С] = 0,8 моль/л. Каковы исходные концентрации веществ А и В?
2. Газовая смесь состоит из водорода и хлора. Реакция идет по уравнению H2 + Cl2 --> 2HCl. Как изменится скорость реакции, если увеличить давление в три раза?
3. Вычислить ![]() реакции, если константа скорости её при 1200С составляет 5,88.10-4 , а при 1700С равна 6,7.10-2.
реакции, если константа скорости её при 1200С составляет 5,88.10-4 , а при 1700С равна 6,7.10-2.
Контрольная работа 4. Расчет водородного показателя водного раствора кислоты, основания или соли.
Вариант 1
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) нитрата цинка.
2. Найти молярную концентрацию раствора гидроксида бария, если рН равен 9.
Вариант 2
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) хлорида магния.
2. Чему равен рН в 0,025 Н растворе серной кислоты.
Вариант 3
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) карбоната лития.
2. Вычислить рН раствора азотной кислоты, в 500 мл которого содержится 3,15 г азотной кислоты.
Вариант 4
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) нитрата свинца (II).
2. рН раствора гидроксида кальция равен 12. Найти концентрацию этого раствора в г/л.
Вариант 5
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) роданида натрия.
2. рН раствора гидроксида калия равен 11. Найти нормальность этого раствора.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ ПО ВЫПОЛНЕНИЮ КОНТРОЛЬНЫХ ЗАДАНИЙ
, Рябцева : Методические указания для решения задач.
ОГЛАВЛЕНИЕ
Введение
Список использованных обозначений
1. Основные классы неорганических соединений
1.1. Оксиды
1.2. Гидроксиды
1.3. Кислоты
1.4. Соли
2. Взаимодействие веществ
2.1. Химическая термодинамика
2.1.1. Основные понятия
2.1.2. Энергетика химических процессов (термохимические расчеты). Первый закон термодинамики
2.1.3. Энтропия. Химическое сродство. Второй закон термодинамики
2.1.4. Условия самопроизвольного протекания процессов. Третий закон термодинамики
2.1.5. Примеры решения задач
2.2. Химическая кинетика
2.2.1. Закон действия масс (закон Гульдберга-Вааге)
2.2.2. Влияние температуры на скорость реакции
2.2.3. Химическое равновесие. Константа равновесия
2.2.4. Смещение химического равновесия. Принцип Ле Шателье
2.2.5. Примеры решения задач
3. Растворы и реакции в водных растворах
3.1. Концентрации растворов
3.1.1. Способы задания концентрации растворов
3.1.2. Закон эквивалентов
3.1.3. Пример решения задачи
3.2. Теория растворов
3.2.1. Давление пара растворов
3.2.2. Кипение и замерзание растворов
3.2.3. Осмос. Осмотическое давление
3.2.4. Количественные характеристики растворов электролитов. Закон растворения
3.2.5. Произведение растворимости. Условие образования осадка
3.2.6. Примеры решения задач
3.3. Ионное произведение воды и водородный показатель. Гидролиз солей
3.3.1. Ионное произведение воды и водородный показатель
3.3.2. Гидролиз солей
3.3.3. Примеры решения задач
3.4. Комплексные соединения
3.4.1. Общие понятия о структуре комплексного соединения
3.4.2. Номенклатура комплексных соединений
3.4.3. Диссоциация комплексных соединений в водных растворах
3.4.4. Разрушение комплексных ионов
3.4.5. Примеры решения задач
3.5. Жёсткость природных вод
3.5.1. Общие понятия о жесткости воды
3.5.2. Способы умягчения воды
3.5.3. Примеры решения задач
4. Окислительно-восстановительные системы
4.1. Окислительно-восстановительные реакции
4.1.1. Общие понятия об окислительно-восстановительных реакциях
4.1.2. Подбор коэффициентов методом электронного баланса
4.1.3. Подбор коэффициентов методом электронно-ионного баланса
4.1.4. Пример решения задачи
4.2. Гальванические элементы и электрохимические процессы
4.2.1. Понятие электрода
4.2.2. Типы электродов. Электродный потенциал
4.2.3. Гальванические элементы
4.2.4. Электролиз расплавов и водных растворов электролитов
4.2.5. Законы Фарадея
4.2.6. Примеры решения задач
Приложения
Литература
СПИСОК ИСПОЛЬЗОВАННЫХ ОБОЗНАЧЕНИЙ
А - механическая работа;
G - изобарно-изотермический потенциал (свободная энергия Гиббса);
Ж - жёсткость воды;
γ – температурный коэффициент скорости химической реакции;
С – концентрация раствора;
СВ - молярная концентрация (молярность) раствора;
См – моляльная концентрация (моляльность раствора);
СЭ (допускается СН) – молярная концентрация эквивалентов вещества (эквивалентная концентрация, нормальная концентрация, нормальность раствора);
Н - энтальпия;
h – степень гидролиза раствора соли;
i – изотонический коэффициент раствора;
КД – константа диссоциации вещества в растворе электролита;
КР – константа равновесия;
КН - константа нестойкости комплексного иона;
k – константа скорости химической реакции;
kЭ – эбуллиоскопическая постоянная вещества растворителя;
kК – криоскопическая постоянная вещества растворителя;
МВ - молярная масса вещества;
Мэкв – молярная масса эквивалентов вещества;
mA - масса растворителя в растворе;
mB - масса растворённого в растворе вещества;
mP - масса раствора;
Р – давление;
pH – водородный показатель;
Q - теплота;
ρ - плотность раствора;
S - энтропия;
U - внутренняя энергия;
V - объем;
υ – скорость химической реакции;
ω – массовая доля растворённого вещества.
1. ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
1.1. Оксиды
Оксиды – соединения элементов с кислородом с общей формулой ![]() .
.
Элементы могут быть металлами и неметаллами. Например: СаО – оксид кальция; N2O – оксид азота (I); N2O5 – оксид азота (V). Кислород в оксидах двухвалентен. Если для элемента характерна переменная валентность, то она обозначена в скобках.
Оксиды не диссоциируют на ионы, т. к. не являются электролитами.
Оксиды подразделяются на:
- солеобразующие:
· основные,
· кислотные,
· амфотерные;
- несолеобразующие.
Основными оксидами называют те, которые с водой образуют основания (образованы металлами в низших степенях окисления) (+1; +2; редко +3):
Li2O + H2O ![]() 2LiOH
2LiOH
оксид лития гидроксид лития
Кислотными оксидами называют оксиды, которые при взаимодействии с водой образуют кислоты или соответствуют кислотам.
Кислотные оксиды образуются неметаллами:
N2O5 соответствует азотная кислота HNO3
оксид азота (V)
или металлами в высших степенях окисления (+3; +4; +5; +6; +7):
Mn2O7 соответствует марганцовая кислота HMnO4
оксид марганца (VII)
Амфотерные оксиды соответствуют некоторым металлам (Pb, Sn, Al, Zn...): PbO – оксид свинца (II); ZnO – оксид цинка.
Амфотерным оксидам соответствуют гидроксиды, обладающие основными и кислотными свойствами:
PbO → Pb(OH)2 – обладает основными и
кислотными свойствами
Несолеобразующими оксидами называют оксиды, которые не образуют и не соответствуют ни кислотам, ни гидроксидам:
СО N2O NO
оксид углерода (II) оксид азота (I) оксид азота (II)
1.2. Гидроксиды
Гидроксиды – вещества, отвечающие составу ![]() .
.
Гидроксиды – электролиты, которые в воде диссоциируют на ионы металлов и гидроксид-ионы (![]() ).
).
NaOH – гидроксид натрия;
Fe(OH)3 – гидроксид железа (III).
Именно гидроксид-ионы обуславливают общие свойства класса гидроксидов, включая окраску индикаторов.
Гидроксиды подразделяются на основные, кислородсодержащие кислоты и амфотерные.
Основные гидроксиды соответствуют основным оксидам и называются основаниями:
K2O – KOH; MgO – Mg(OH)2
Гидроксиды-основания могут быть хорошо и плохо растворимыми в воде.
Хорошо растворимые в воде гидроксиды называются щелочами.
Щелочи образуются металлами, располагающимися в главных подгруппах первой и некоторых металлов второй групп периодической таблицы и их восемь: LiOH; NaOH; KOH; RbOH; CsOH; FrOH; Ba(OH)2 и Ca(OH)2.
Щелочи являются сильными электролитами, диссоциирующими в водных растворах необратимо:
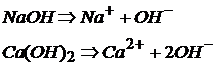
Все остальные основания являются трудно растворимыми в воде соединениями и слабыми электролитами:
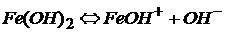
ион гидроксожелеза(II)
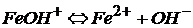
Существуют два исключения:
NH4OH – гидроксид аммония – хорошо растворимое в воде соединение, но слабый электролит (![]() – ион аммония);
– ион аммония);
Ca(OH)2 – трудно растворимое в воде соединение, но сильный электролит.
Кислородосодержащие кислоты соответствуют кислотным оксидам:
![]()
![]() Cr(OH)6 C(OH)4
Cr(OH)6 C(OH)4
CrO3 – или CO2 – или
![]()
![]() H2CrO4 ·2H2O H2CO3 · H2O
H2CrO4 ·2H2O H2CO3 · H2O
Диссоциация кислот описана ниже в разделе 1.3.
Амфотерные гидроксиды соответствуют амфотерным оксидам и обладают свойствами как оснований так и кислородосодержащих кислот:
![]() Sn(OH)2 гидроксид олова (II) – основание
Sn(OH)2 гидроксид олова (II) – основание
SnO –
![]() H2SnO2 – оловянистая кислота
H2SnO2 – оловянистая кислота
Как основание гидроксид Sn(II) диссоциирует:
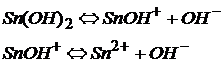
Как кислота гидроксид Sn(II) диссоциирует:
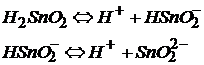
1.3. Кислоты
Кислота – сложное вещество, в молекуле которого имеется один или несколько атомов водорода, которые могут быть замещены атомами (ионами) металлов или аммонием.
Оставшаяся часть молекулы кислоты называется кислотным остатком.
По количеству частиц водорода, способных замещаться в химических реакциях, кислоты подразделяются на одно-, двух-, и многоосновные:
HNO3; HCl; HCN – одноосновные кислоты;
H2SO4; H2CO3; H2S – двухосновные кислоты.
Как электролиты кислоты могут быть сильными и слабыми.
Кислоты – сильные электролиты:
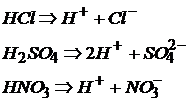
Кислоты – слабые электролиты диссоциируют ступенчато:
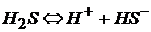
гидросульфид ион
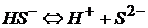
сульфид ион
По природе кислотного остатка кислоты подразделяются на бескислородные:
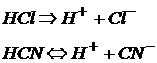
и кислородсодержащие:
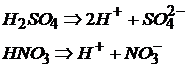
Названия кислот определяются природой кислотного остатка:
H2S – сероводородная кислота;
HCN – циановодородная кислота.
Названия кислородсодержащих кислот зависят от степени окисления центрального атома кислотного остатка.
Если центральный атом находится в высшей степени окисления, то название кислоты имеет окончание «ная»:
HNO3 – азотная.
Если центральный атом кислотного остатка находится не в наивысшей степени окисления, то название кислоты имеет окончание «истая»:
HNO2 – азотистая.
1.4. Соли
Все соли – сильные электролиты, образующиеся в результате реакции нейтрализации кислоты основанием.
Соли подразделяются на:
· средние,
· кислые,
· основные,
· двойные,
· смешанные.
Средние соли образуются, если гидроксид и кислота взаимодействуют в эквивалентном отношении. Молекула средней соли состоит из катиона металла или аммония и кислотного остатка кислоты:
MgCO3 – карбонат магния;
(NH4)2S – сульфид аммония.
Диссоциируют средние соли на ионы металла (аммония) и кислотного остатка.
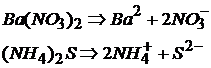
Кислые соли возможны для многоосновных кислот (H2SO4; H3PO4 …), в которых ионы Н+ частично замещены на ионы металла или аммония:
NaHCO3 – гидрокарбонат натрия.
В названии кислой соли присутствует приставка «гидро».
NH4H2PO4 – дигидрофосфат аммония.
Кислые соли диссоциируют на ионы металла (аммония) и кислотный остаток, включающий одну или несколько частиц водорода:
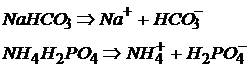
Основные соли образуются в том случае, если гидроксид является многокислотным (Fe(OH)2, Al(ОН), а кислота взята в недостатке:
Al(ОН)3 + НСl Al(ОН)2 Сl + Н2О или, что то же самое:
Аl ОН ОН ОН + НCl Al(ОН)2 Сl + Н2О.
В названии основной соли присутствует приставка «гидроксо». Присутствие нескольких ![]() ионов обозначается греческим числительным.
ионов обозначается греческим числительным.
Al(OH)2Cl – хлорид дигидроксо алюминия;
(Fe(OH)2)2SO4 – сульфат дигидроксо железа (III).
Основные соли диссоциируют на сложные катионы, состоящие из иона металла и гидроксогруппы и ионы кислотного остатка:
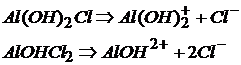
Соли, образованные двумя металлами и одной кислотой, называются двойными солями.
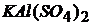 – сульфат кальция алюминия (алюмокальциевые квасцы):
– сульфат кальция алюминия (алюмокальциевые квасцы):
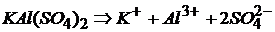 .
.
Соли, образованные одним катионом и двумя разными кислотами, называются смешанными.
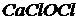 (или
(или 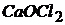 ) – кальциевая соль хлороводородной (
) – кальциевая соль хлороводородной (![]() ) и хлорноватистой (
) и хлорноватистой (![]() ) кислот:
) кислот:
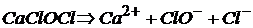 .
.
2. ВЗАИМОДЕЙСТВИЕ ВЕЩЕСТВ
2.1. Химическая термодинамика
Химическая термодинамика изучает превращение энергии при химических реакциях и способность химических систем совершать полезную работу.
2.1.1. Основные понятия
Термодинамические параметры системы – это величины, которые характеризуют состояние системы и могут быть непосредственно измерены. Основными параметрами состояния являются: давление Р, объем V, концентрация С.
Термодинамические функции системы – это переменные величины, которые зависят от параметров состояния. К термодинамическим функциям относятся: внутренняя энергия U, теплота Q, механическая работа А, энтальпия Н, энтропия S, изобарно-изотермический потенциал (свободная энергия Гиббса) G и др. Термодинамические функции бывают двух видов: функции состояния и функции процесса.
К функциям состояния относятся такие, изменения которых не зависят от пути и способа проведения процесса, а зависят только от начального и конечного состояния системы. Так, например, если функция состояния внутренняя энергия в начальном состоянии системы равна U1, а в конечном U2, то изменение ∆U = U2 – U1 не зависит от того как осуществляется процесс.
В противоположность функциям состояния изменение функций процесса зависит от того, при каких условиях и каким путем протекал процесс. К функциям процесса относится теплота Q и механическая работа А.
Состояние системы – это совокупность ее физических и химических свойств.
Термодинамический процесс – это изменение системы, связанное с изменением хотя бы одного термодинамического параметра или функции. В зависимости от способа проведения процессы могут быть термодинамически обратимыми или необратимыми.
2.1.2. Энергетика химических процессов (термохимические расчеты). Первый закон термодинамики
При любом процессе соблюдается закон сохранения материи и выполняется первое начало термодинамики, как частный случай этого закона:
Теплота, поглощаемая системой, расходуется на увеличение внутренней энергии и на совершаемую системой механическую работу.
Первый закон термодинамики применим к процессам, сопровождающимся преобразованием теплоты.
Q = ∆U + А,
где А – работа выполненная системой против действия внешних сил.
Если такая работа сводится к расширению или к сжатию, то такой силой является внешнее постоянное давление
Q = ∆U + Р∆V,
где ∆V – изменение объема системы.
Применение первого начала термодинамики к различным процессам. При изохорном процессе ∆V = 0. Уравнение первого начала термодинамики имеет вид:
Qν = ΔU
Поскольку внутренняя энергия является функцией состояния, для изохорных процессов количество теплоты также не зависит от пути перехода и определяется только начальным и конечным состоянием системы. Из уравнения следует, что в изохорном процессе вся поглощаемая теплота расходуется на увеличение внутренней энергии системы.
Прежде чем рассматривать применение первого закона термодинамики к изобарному процессу, познакомимся с широко применяемой термодинамической функцией, называемой энтальпией Н. Она определяется как сумма полной внутренней энергии системы и произведение внешнего давления на объем, который занимает система:
Н = U + РV
Для макропроцессов:
Qp = ΔH,
где Qp – количество поглощенной или выделенной системой теплоты при постоянном внешнем давлении.
Энтальпия является функцией состояния системы. Значит, в изобарном процессе количество поглощенной или выделенной теплоты не зависит от способа проведения процесса и определяется только начальным и конечным состоянием системы. Видно, что в изобарном процессе (∆Р = 0) количество теплоты измеряется изменением энтальпии.
При изотермическом процессе внутренняя энергия – величина постоянная, ∆U = 0. Тогда уравнение первого начала:
QT = А
где QT – количество поглощенной или выделенной системой теплоты при постоянной температуре.
Следовательно, при изотермическом процессе поглощенная теплота расходуется только на совершаемую системой механическую работу.
При адиабатном процессе, когда Q = 0, уравнение принимает вид:
А = ─∆U
Это означает, что в адиабатном процессе механическая работа может совершаться только за счет внутренней энергии системы.
Термохимические расчеты основаны на законе Гесса:
Тепловой эффект химической реакции не зависит от пути, по которому она протекает, а определяется только природой, состоянием и количествами исходных веществ и продуктов реакции.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



