Ni2+ + H2O → NiOH+ + H+, pH < 7,
Электродные процессы
K (–):
2H+ + 2e → H2↑
A (+): H2O – 4e → O2↑ + 4H+
Задача № 3
Напишите электродные процессы при электролизе расплава
MgCl2 ∙ 6CaCl.
Решение:
В расплаве происходит диссоциация:
MgCl2 ∙ 6CaCl Mg2+ + 6Ca2+ + 8Cl─
Е0(Меz+/Ме): –2,363B > –2,925B
Так как Е0(Мg) > Е0(Ca), то на катоде восстанавливается катион Mg2+, а потом ─ Ca2+.
Катодный процесс: Mg2+ + 2е → Mg
Ca2+ + 2e → Ca.
На аноде окисляются анионы Cl─.
Анодный процесс: 2Cl─ ─ 2e → Cl2.
Задача № 4
При электролизе раствора CuSO4 на графитовых электродах масса катода увеличилась на 10,58 г. Определите объем газа, выделившегося на аноде (н. у).
Решение:
Чтобы определить, какие вещества выделились на электродах, напишем уравнение диссоциации CuSO4 и электродные процессы:
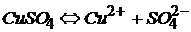 , рН < 7 из-за гидролиза
, рН < 7 из-за гидролиза
К (–): Cu2+ + 2е → Cu z(Cu) = 2
А (+): 2Н2О – 4е → О2 + 4Н+ z(О2) = 4
Следовательно, на катоде выделяется медь, на аноде – газ кислород. = 63,5/2 = 31,75 г/моль·экв.
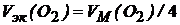 = 22,4/4 = 5,6 дм3/моль.
= 22,4/4 = 5,6 дм3/моль.
Поскольку при электролизе через катод и анод проходит одно и то же количество электричества: Q = Qа = Qк, то
.
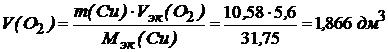 .
.
Ответ: объём образовавшегося на аноде кислорода составляет 1,866.
Приложение 1. Названия некоторых кислот и соответствующих им солей
Формула | Название кислоты (сильная –1, слабая –0) | Пример средней соли | Название солей |
HF | Фтороводородная –0 (плавиковая) | NH4F | Фториды |
HCl | Хлороводородная –1 (соляная) | NaCl | Хлориды |
HClO | Хлорноватистая –0 | NaClO | Гипохлориты |
HClO2 | Хлористая–0 | LiClO2 | Хлориты |
HClO3 | Хлорноватая –1 | KClO3 | Хлораты |
HClO4 | Хлорная –1 | NaClO4 | Перхлораты |
HBr | Бромоводородная –1 | KBr | Бромиды |
HI | Иодоводородная –1 | MgI2 | Иодиды |
HIO3 | Иодноватая –1 | KIO3 | Иодаты |
H2S | Сероводородная –0 | (NH4)2S | Сульфиды |
H2SO3 | Сернистая-0 | Na2SO3 | Сульфиты |
H2SO4 | Серная-1 | Na2SO4 | Сульфаты |
H2S2O3 | Тиосерная-0 | Na2S2O3 | Тиосульфаты |
HNO3 | Азотная-1 | KNO3 | Нитраты |
HNO2 | Азотистая-0 | NH4NO2 | Нитриты |
H3PO4 | Фосфорная-0 | Ag3PO4 | Фосфаты |
H3AsO4 | Мышьяковая-0 | Na3AsO4 | Арсенаты |
H3AsO3 | Мышьяковистая-0 | Na3AsO3 | Арсениты |
H2CrO4 | Хромовая-1 | K2CrO4 | Хроматы |
H2Cr2O7 | Двухромовая-1 | K2Cr2O7 | Дихроматы |
HMnO4 | Марганцовая-1 | KMnO4 | Перманганаты |
H2SiO3 | Кремниевая-0 | Na2SiO3 | Силикаты |
H2CO3 | Угольная-0 | CaCO3 | Карбонаты |
HCN | Циановодородная-0 (синильная) | KCN | Цианиды |
HSCN | Тиоциановая-0 (родановая) | NH4SCN | Тиоцианаты (роданиды) |
CH3COOH | Уксусная-0 | NaCH3COO | Ацетаты |
H3BO3 | Борная-0 | K3BO3 | Бораты |
H2B4O7 | Четырехборная-1 | Na2B4O7 | Тетрабораты |
HВrO3 | Бромноватая-1 | LiBrO3 | Броматы |
HCOOH | Муравьиная-0 | NaHCOO | Формиаты |
H2C2O4 | Щавелевая-0 | CaC2O4 | Оксалаты |
HCrO2 | Хромистая-0 | KСrO2 | Хромиты |
H5IO6 | Ортоиодная-0 | (NH4)5IO6 | Ортопериодаты |
HIO4 | Метаиодная-1 | NaIO4 | Метапериодаты |
H2MnO4 | Марганцовистая-1 | Na2MnO4 | Манганаты |
HOCN | Циановая-0 | Mg(OCN)2 | Цианаты |
HPO3 | Метафосфорная-1 | Ca(PO3)2 | Метафосфаты |
H4P2O7 | Двуфосфорная-1 | Na4P2O7 | Дифосфаты |
H3PO3 | Фосфористая-0 | AlPO3 | Фосфиты |
H3PO2 | Фосфорноватистая-0 | Na3PO2 | Гипофосфиты |
H2S2O8 | Пероксодвусерная-1 | BaS2O8 | Пероксодисульфаты |
H2S2O7 | Двусерная-1 | K2S2O7 | Дисульфаты (пиросульфаты) |
H2S2O5 | Двусернистая-1 | CaS2O5 | Дисульфиты |
H2S2O2 | Тиосернистая-0 | Na2S2O2 | Тиосульфиты |
H2S2O6 | Дитионовая-1 | K2S2O6 | Дитионаты |
H6TeO6 | Теллуровая-0 | Na6TeO6 | Теллураты |
HVO3 | Ванадиевая-1 | LiVO3 | Ванадаты |
H2WO4 | Вольфрамовая-1 | CaWO4 | Вольфраматы |
Приложение 2. Термодинамические характеристики некоторых веществ

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



