[Cr(CNS)4 (NH3)2] ↔ Cr3+ + 4CNS─ + 2NH3

Чем меньше значение Кн, тем устойчивее комплексный ион.
3.4.3. Разрушение комплексных ионов
Разрушить комплексный ион – это значит сместить равновесие в схеме его диссоциации в направлении прямого процесса. В зависимости от значений Кн комплексные ионы делятся на:
· нестойкие, если Кн > 10–5;
· средней стойкости, если Кн = 10–20 ÷ 10–5;
· устойчивые, если Кн < 10–20.
Устойчивые ионы химически разрушить очень сложно, нестойкие ионы разрушаются разбавлением водой, а разрушить комплексные ионы средней стойкости можно следующими способами:
1. Уводом комплексообразователя или лигандов в более устойчивый комплексный ион при условии, что константа нестойкости разрушаемого комплексного иона много больше (несколько порядков) константы нестойкости нового иона.
2. Уводом комплексообразователя или лигандов в осадок труднорастворимого соединения при условии, что произведение растворимости осадка (ПР – справочные данные) много меньше константы нестойкости разрушаемого иона.
3.4.4. Примеры решения задач
Задача № 1
Назовите комплексные соединения, укажите в них комплексообразователь, лиганды, координационное число, внешнюю сферу. Напишите уравнения диссоциации соединений и комплексных ионов.
а) K3[Co(NO2)6]
б) [Pt(NH3)4]SO4
Решение:
а) Название комплексного соединения:
Гекса – нитрито кобальтат (III) калия.
Комплексообразователь – Со3+.
Лиганды – NO2–.
Координационное число – 6.
Внешняя сфера – ионы К+.
Уравнения диссоциации:
K3[Co(NO2)6] → 3K+ + [Co(NO2)6]3–
[Co(NO2)6]3– ↔ Co3+ + 6NO2–
б) Название комплексного соединения:
Сульфат тетра – аммин платины (II).
Комплексообразователь – Pt2+.
Лиганды – NH3.
Координационное число – 4.
Внешняя сфера – SO42–.
Уравнения диссоциации:
[Pt(NH3)4]SO4 → [Pt(NH3)4]2+ + SO42–
[Pt(NH3)4]2+ ↔ Pt2+ + 4NH3.
Задача №2
Напишите формулы комплексных соединений, укажите в них комплексообразователь, лиганды, координационное число, ион внешней сферы. Напишите уравнения диссоциации комплексных соединений и комплексных ионов, выражения для констант нестойкости комплексных ионов.
а) Хлорид тетра – карбонил никеля (II).
б) Сульфат моно – гидрокарбонато индия (3).
в) Гекса – циано феррат (III) железа.
Решение:
а) [Ni(CО)4]Cl2
Комплексообразователь – Ni2+.
Лиганды – CО.
Координационное число – 4.
Ион внешней сферы – Cl–.
Уравнения диссоциации:
хТш(СО)4ъСд2 → хТш(СО)4ъ2+ + 2Сд–
[Ni(CО)4]2+ ↔ Ni2+ + 4CО.

б) [In(HCO3)]SO4
Комплексообразователь – In3+.
Лиганды – HCO3–.
Координационное число – 1.
Ион внешней сферы – SO42–.
Уравнения диссоциации:
[In(HCO3)]SO4 → [In(HCO3)]2+ + SO42–
[In(HCO3)]2+ ↔ In3+ + HCO3–

в) Fe[Fe(CN)6]
Комплексообразователь – Fe3+.
Лиганды – CN–.
Координационное число – 6.
Ион внешней сферы – Fe3+.
Уравнения диссоциации:
Fe[Fe(CN)6] → Fe3+ + [Fe(CN)6]3-
[Fe(CN)6]3– ↔ Fe3+ + 6CN-

Задача №3
Напишите уравнение реакции разрушения комплексного иона [Cu(CO3)2]2–,если его Кн = 9,77 · 10–11.
Решение:
Рассмотрим структуру данного комплексного иона
[Cu(CO3)2]2–↔ Cu2+ + 2CO32–
Cu2+ - комплексообразователь,
CO32–- лиганды.
Для того, чтобы разрушить этот комплексный ион уводом комплексообразователя или лигандов в осадок труднорастворимого соединения, находим в таблице произведений растворимости (ПР) химические соединения меди (II) и карбонаты, у которых значения ПР << Кн = 9,77 · 10–11.
Cu(OH)2 ПР = 2,2 · 10–20
CuS ПР = 6,3 · 10–36
PbCO3 ПР = 7,5 · 10–14
Рассмотрим все три случая.
Чтобы получить осадок Cu(OH)2 кроме ионов Cu2+ (комплексообразователь) необходимы ионы OH-, которые в достаточном количестве содержатся в растворе любого сильного гидроксида, например, NaOH, KOH, Ba(OH)2 и т. д.
[Cu(CO3)2]2– + 2NaOH → Cu(OH)2 ↓ + 2Na+ + 2CO32–
I Кн = 9,77 · 10–11 >> ПР = 2,2 · 10–20
Чтобы получить осадок CuS, кроме ионов Cu2+ необходимы ионы S2–, которые в достаточном количестве содержатся в любом растворимом в воде сульфиде, например, (NH4)2S; K2S; Na2S и т. д.
[Cu(CO3)2]2–+ K2S → CuS ↓ + 2K+ + 2CO32–
Кн = 9,77 · 10–11 >> ПР = 6,3 · 10–36
Чтобы получить осадок PbCO3 кроме ионов CO32– (лиганды) необходимы ионы Pb2+, которые в достаточном количестве содержатся в любой растворимой соли свинца (II), например, Pb(NO3)2, Pb(CH3COO)2 и т. д.
[Cu(CO3)2]2– + Pb(NO3)2 → PbCO3↓ + Cu2++ CO32– + 2NO3–
Кн = 9,77 · 10–11 >> ПР = 7,5 · 10–14
3.5. Жёсткость природных вод
3.5.1. Общие понятия о жёсткости воды
Вода самое распространенное на земле вещество. Вода представляет собой бесцветную, прозрачную жидкость, не имеющую ни запаха, ни вкуса. Вода имеет рН = 7,0; т. е. нейтральный характер. Плотность воды при + 4 0С равна 1 г/см3. Массовый состав воды выражается следующими числами: 11,11 % (мас.) водорода и 88,89 % (мас.) кислорода. Простейшая формула воды Н2О, мольная масса равна 18 г/моль.
Вода является всеобщим универсальным растворителем, поэтому вода никогда не бывает совершенно чистой. Вода содержит растворенные газы, микроорганизмы, растворимые примеси, частицы песка, глины и т. д.
Поэтому существует государственный стандарт (ГОСТ), согласно которому контролируется качество питьевой воды.
Контролю подлежат вкус, запах, цветность и мутность воды, определяется жесткость воды.
Контролируются концентрации в воде железа, мышьяка, азотсодержащих веществ, фторидов, меди, сульфатов, алюминия, активного хлора, свинца, цинка, серебра, бериллия, молибдена, полифосфатов, селена, стронция.
Природная вода, содержащая в растворе большое количество солей кальция и магния в виде гидрокарбонатов и сульфатов, называется жесткой водой. Точнее, жесткой называют воду с повышенным содержанием ионов Са2+ и Mg2+. Са2+ и Mg2+ образуют с мылами трудно растворимые соединения. С Синтетическими моющими средствами трудно растворимые соединения образуются в гораздо меньшей степени, но все-таки эффективность синтетических моющих средств в жесткой воде ниже, чем в мягкой. Мягкой называется вода содержащая мало ионов Са2+ и Mg2+ или совсем не содержащая их.
Жёсткость – один из технических показателей, принятых для характеристики состава и качества природных вод. Жесткость простых водоемов колеблется в широких пределах и зависит от типа окружающих почв, сезона года, времени суток.
Жёсткость воды (Ж) выражают количеством миллимоль эквивалентов ионов Ca2+ и Mg2+, содержащихся в 1 дм3 воды.
Жёсткость кальциевая:

Жёсткость магниевая:
 ,
,
где ![]() и
и ![]() – масса ионов Са2+ и Mg2+(г), соответственно;
– масса ионов Са2+ и Mg2+(г), соответственно;
 г/моль-экв;
г/моль-экв;
 г/моль-экв;
г/моль-экв;
V – объем воды (дм3).
Общая жесткость определяется суммой частных жесткостей:

Измеряется жёсткость числом миллимолей эквивалентов ионов жесткости (Са2+ и Mg2+) в 1 кг воды. В связи с тем, что плотность воды близка к единице, жесткость можно измерять в ммоль/дм3; или ммоль/дм3; или моль/м3. ![]() = 1 ммоль-экв соответствует содержанию в 1 дм3 воды 20,04 мг ионов Са2+. Аналогично
= 1 ммоль-экв соответствует содержанию в 1 дм3 воды 20,04 мг ионов Са2+. Аналогично ![]() = 1 ммоль-экв соответствует содержанию в 1 дм3 воды 12,16 мг ионов Mg2+.
= 1 ммоль-экв соответствует содержанию в 1 дм3 воды 12,16 мг ионов Mg2+.
По ГОСТ 4151-72 жёсткость не должна превышать 7 моль/м3. Если Жо < 7, то вода считается мягкой, если Жо < 4, то вода считается очень мягкой. Если Жо > 7, то вода считается жесткой, если Жо > 14, то вода считается очень жесткой.
Различают жёсткость воды карбонатную, некарбонатную и общую.
Карбонатная (временная) жёсткость ЖВ обусловлена наличием в воде гидрокарбонатов кальция и магния: Са(НСО3)2 и Mg(HCO3)2.
Некарбонатная (постоянная) жёсткость ЖП вызвана присутствием в воде других солей кальция и магния, например хлоридов и сульфатов.
3.5.2. Способы умягчения воды
Процесс устранения (снижения) жёсткости воды называется умягчением воды.
Для умягчения воды используют термический и реагентные методы.
Термический метод
Предусматривает нагревание воды до 95 – 98 ºС. При этом происходит разложение гидрокарбонатов кальция и магния:
Са(НСО3)2 = СаСО3↓ + СО2↑ + Н2О.
Магний при нагревании воды осаждается в виде гидроксида или основного карбоната (вследствие гидролиза):
Mg(HCO3)2 = MgCO3 + CO2↑ + H2O,
2MgCO3 + 2H2O = (MgOH)2CO3 + CO2↑ + H2O,
MgCO3 + 2H2O = Mg(OH)2↓ + СО2↑ + Н2О.
Таким образом, при кипячении воды жесткость, вызываемая присутствием гидрокарбонатов кальция и магния, устраняется и поэтому называется временной – ЖВ. Некарбонатная жесткость не устраняется при кипячении, поэтому ее еще называют постоянной жёсткостью – ЖП.
Реагентные методы
Связаны с удалением ионов кальция и магния в результате образования малорастворимых соединений под действием химических реагентов. В качестве таких реагентов используют Са(ОН)2 (метод известкования), смесь Са(ОН)2 + NaCO3 (содово-известковый метод), реже – другие вещества.
Гидроксид кальция устраняет карбонатную жесткость:
Са(НСО3)2 + Са(ОН)2 = 2СаСО3↓ + 2Н2О,
Mg(HCO3)2 + 2Са(ОН)2 = Mg(OH)2↓ + 2СаСО3↓ + 2Н2О.
Сода устраняет некарбонатную жесткость:
CaSO4 + Na2CO3 = CaCO3↓ + Na2SO4,
MgCl2 + Na2CO3 + H2O = Mg(OH)2↓ + 2NaCl + CO2↑.
3.5.3. Примеры решения задач
Задача № 1
В 10 литрах воды содержится 0, 54 г Са2+ и 0,32 г Mg2+. Чему равна общая жесткость воды?
Решение:


![]()

![]()
ЖО = 2,69 + 2,63 = 5,32 
Ответ: ЖО = 5,32 < 7, т. е. водя мягкая
Задача № 2
Какая масса хлорида кальция содержится в 5 литрах воды, если ее жесткость 6![]() ?
?
Решение:
Найдем массу Са2+, содержащихся в 5 дм3 воды:
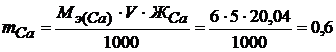 г
г
Для определения массы СаCl2 рассчитаем молярную массу и составим пропорцию:

40,08 г – 0,6 г
111,08 – х
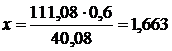 г
г
Ответ: масса СаCl2 1,663 г.
Задача № 3
К 200 л воды с ЖВ = 2,8 ммоль-экв/дм3 добавили 150 дм3 воды с ЖП = 3 ммоль-экв/дм3. Определите ЖВ, ЖП, ЖО после смешения.
Решение:
1. nЭК(врем.) = ЖВ ∙ V1/1000 = 2,8 ∙ 200/1000 = 0,56 моль-экв.
2. nЭК(пост.) = ЖП ∙ V2/1000 = 3 ∙ 150/1000 = 0,45 моль-экв.
3. После смешения V(р-ра) = V1 + V2 = 150 + 200 = 350.
4. ЖВ = 1000 ∙ nЭК(врем.)/V(р-ра) = 1000 ∙ 0,56/350 = 1,6 ммоль-экв.
5. ЖП = 1000 ∙ nЭК(пост.)/V(р-ра) = 1000 ∙ 0,45/350 = 1,3 ммоль-экв.
6. ЖО = ЖВ + ЖП = 1,6 + 1,3 = 2,9 ммоль-экв.
Ответ: в полученном образце воды жёсткость
общая ЖО = 2,9 ммоль-экв;
временная ЖВ = 1,6 ммоль-экв;
постоянная ЖП = 1,3 ммоль-экв.
Задача № 4
ЖП = 6 ммоль-экв/дм3 обусловлена содержанием СаСl2. Сколько грамм К2СО3 требуется для полного умягчения 100 дм3 воды?
Решение:
Расчет количества реагентов К2СО3, требующегося для удаления ионов жесткости, осуществляют на основе закона эквивалентов:

Отсюда

Ответ: необходимая масса К2СО3 = 40,8 г.
4. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ СИСТЕМЫ
4.1. Окислительно-восстановительные реакции
4.1.1. Общие понятия об окислительно-восстановительных реакциях
Окислительно-восстановительными называются реакции, в ходе которых атомы некоторых элементов меняют свою степень окисления.
Степень окисления – это условный заряд атома, вычисленный в предположении, что каждый атом в молекуле образует ион.
При определении степени окисления необходимо помнить, что:
1. Степень окисления простых веществ равна нулю. Например, в веществах ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() .
.
2. Постоянную степень окисления в большинстве химических соединений имеют:
+1 H, Li, Na, K, Rb, Cs, Fr
+2 Be, Mg, Ba, Ra, Sr, Zn, Ca
+3 Al
-1 F и кислород в перекисных соединениях, например, Н2О2
-2 кислород в оксидах, гидроксидах, кислотах и солях;
3. Если ион образован одним атомом, то его заряд равен степени окисления, например,
![]() SO4 → Cu2+ + SO42–
SO4 → Cu2+ + SO42–
ион меди Cu2+ образован одним атомом меди, в отличие от сульфат - иона SO42–, который образован одним атомом серы и 4 атомами кислорода, поэтому степень окисления меди в этом соединении +2;
4. Степень окисления остальных атомов находится из условия, что алгебраическая сумма степеней окисления всех атомов в молекуле равна нулю, а в ионе – заряду иона. Например:
![]()
![]()
![]()
+1 + х + (-2) · 2 = 0
x = +3
![]()
![]()
![]()
![]()
![]()
2x + (-2) · 7 = -2
x = +6
4.1.2. Подбор коэффициентов методом электронного баланса
Расставим степени окисления элементов в следующей реакции:

Реакция является окислительно-восстановительной, так как степень окисления марганца понижается от +7 в KMnO4 до +2 в MnSO4, следовательно, KMnO4 является окислителем, степень окисления азота повышается от +3 в NaNO2 до +5 в NaNO3, т. е. NaNO2 является восстановителем.
Выявленное изменение степеней окисления элементов принято изображать электронными уравнениями:
| 10 | 2; восстановление, 5; окисление,
|
Чтобы расставить коэффициенты в уравнении реакции, определяем наименьшее общее кратное число электронов в реакции, оно равно 10. Дополнительные множители 2 и 5 являются коэффициентами перед формулами окислителя и восстановителя в левой части уравнения и коэффициентами перед формулами соответствующих соединений в правой части. Схема реакции принимает следующий вид:
5NaNO2 + 2KMnO4 + H2SO4 → 5NaNO3 + 2MnSO4 + K2SO4 + H2O.
Для других соединений, участвующих в реакции, кроме водорода и кислорода, определение коэффициентов производится сопоставлением числа атомов и ионов в левой и правой частях схемы. Отмечаем, что в данной реакции число ионов калия в левой и правой частях одинаково, поэтому перед формулой K2SO4 коэффициент не ставится. Определяя число ионов ![]() , находим, что в правой части их суммарно 3, следовательно, коэффициент перед формулой серной кислоты в левой части также должен быть 3, после чего схема принимает вид:
, находим, что в правой части их суммарно 3, следовательно, коэффициент перед формулой серной кислоты в левой части также должен быть 3, после чего схема принимает вид:
5NaNO2 + 2KMnO4 + 3H2SO4 → 5NaNO3 + 2MnSO4 + K2SO4 + H2O.
Уравниваем число атомов водорода: в левой части уравнения 6 атомов водорода, тогда в правой части перед Н2О ставим коэффициент 3. Получим уравнение в окончательном виде:
5NaNO2 + 2KMnO4 + 3H2SO4 → 5NaNO3 + 2MnSO4 + K2SO4 + 3H2O.
Если уравнение в молекулярной форме составлено верно, то общее число атомов кислорода в левой и правой частях уравнения будет одинаковым.
4.1.3. Подбор коэффициентов методом электронно-ионного баланса
Рассмотрим этот метод на примере следующего превращения:
NaI + PbO2 + H2SO4 → Na2SO4 + PbSO4 + I2 + H2O
I. Для того, чтобы найти частицы, в которые входят атомы, меняющие свою степень окисления, определим степень окисления всех атомов.
I2 – простое вещество, значит степень окисления 0.
Постоянную степень окисления в большинстве соединений проявляют +1 Na, Н; -2 кислород О.
Степень окисления остальных атомов находим из условия, что сумма степеней окисления атомов в молекуле равна нулю.
![]()
![]() +
+ ![]()
![]() +
+ ![]()
![]()
![]() →
→ ![]()
![]()
![]() +
+ ![]()
![]()
![]() +
+ ![]() +
+ ![]()
![]()
Степень окисления меняют атомы иода и свинца.
Напишем данное превращение в ионном виде (в ОВР допускается представлять в ионном виде слабые электролиты – слабые кислоты, нерастворимые основания и соли).
Na+ + I– + PbO2 + 2H+ + SO42– → 2Na+ + SO42– + Pb2++ SO42–+ I2 + H2O
Na+ + I– + PbO2 + 2H+ + SO42– → 2Na+ + 2SO42– + Pb2+ + I2 + H2O
Атомы, меняющие степень окисления, входят в подчеркнутые частицы.
II. Разделить ОВР на две полуреакции. Уравнять в полуреакциях сначала частицы, затем заряды.
Разделить ОВР на две полуреакции, это значит взять частицы, в которые входят атомы, меняющие степени окисления (подчеркнутые) до и после реакции.
I- → I2
PbO2 → Pb2+
Сначала уравниваем атомы, меняющие степень окисления, поставив необходимые коэффициенты:
2I– → I2
Во второй полуреакции атомы, меняющие степень окисления (свинец) равны, но слева еще есть два атома кислорода, а слева нет.
Для уравнивания частиц кислорода в полуреакциях используем таблицу 4.1.
Таблица 4.1. – Участие среды в окислительно-восстановительных реакциях
Кислая | Нейтральная | Щелочная | |
Каждая освобождающаяся частица кислорода | Связывается с 2Н+ с образованием одной молекулы Н2О | как в щелочной среде | Связывается с одной молекулой Н2O c образованием 2ОН- |
Каждая недостающая частица кислорода | Берётся из одной молекулы Н2О, одновременно образуются 2Н+ | как в кислой среде | Берётся из 2ОН– образуется одна молекула Н2О |
1. Для определения характера среды смотрим на исходные вещества (слева) данного уравнения, если есть кислота – среда кислая, если есть основание – среда щелочная, если нет ни кислоты, ни основания – среда нейтральная.
В нашем уравнении среди исходных веществ NaI + PbO2 + H2SO4 → есть кислота (серная) H2SO4, т. е. среда кислая.
2. Если число частиц кислорода в полуреакции больше слева – это освобождающиеся частицы. Если частиц кислорода в полуреакции больше справа – это недостающие частицы кислорода. В нашей полуреакции
PbO2 → Pb2+
слева два атома кислорода, а справа нет, т. е. 2 освобождающихся частицы кислорода.
3. Таблица дана на одну частицу кислорода, поэтому в каждом конкретном случае необходимо учитывать число частиц. Так в нашем случае (кислая среда и освобождающиеся частицы кислорода) в таблице дано: каждая освобождающаяся частица кислорода в кислой среде связывается с двумя ионами водорода (2Н+) с образованием молекулы воды (Н2О). Так как в нашей полуреакции частиц кислорода две, то им необходимо 2· 2Н+ = 4Н+ и при этом образуется 2Н2О.
PbO2 + 4Н+ → Pb2+ + 2Н2О.
Для уравнивания зарядов в полуреакциях используем электроны. Заряд электрона равный – 1,6 · 10–19Кл взят за единичный, т. е. заряд ![]() = -1.
= -1.
В первой полуреакции степень окисления иода меняется от -1 до 0, а так как в ОВР участвуют две частицы, то они отдают два электрона.
2I– - 2![]() → I2
→ I2
Процесс отдачи электронов называется окислением, а частица, отдающая электроны – восстановитель.
Во второй полуреакции степень окисления свинца меняется от +4 до +2, т. е. присоединяется два электрона.
PbO2 + 4Н+ + 2![]() → Pb2+ + 2Н2О.
→ Pb2+ + 2Н2О.
Процесс присоединения электронов называется восстановление, а частица присоединяющая электроны – окислитель.
III. Уравнять число электронов в полуреакциях, подобрав дополнительные множители. Умножить каждую полуреакцию на свой дополнительный множитель и суммировать полученные полурекции в общую ОВР. Так как в данном случае число электронов в полуреакциях равное (по 2![]() ), то просто суммируем полуреакции.
), то просто суммируем полуреакции.
2I– - 2![]() → I2
→ I2
PbO2 + 4Н+ + 2![]() → Pb2+ + 2Н2О.
→ Pb2+ + 2Н2О.

2Ш– - 2![]() + ЗиЩ2 + 4Н+ + 2
+ ЗиЩ2 + 4Н+ + 2![]() → Зи2+ + 2Н2О + Ш2
→ Зи2+ + 2Н2О + Ш2
IV. После выполнения химическо-математических операций перенести полученные коэффициенты в исходное уравнение, сделать проверку, и расставить недостающие коэффициенты, если это необходимо.
В данном уравнении можно только исключить электроны, а полученные коэффициенты перенести в исходное уравнение.
2NaI + PbO2 + 2H2SO4 = Na2SO4 + PbSO4 + I2 + 2H2O
4.1.4. Пример решения задачи
Задача №1
Уравняем реакцию ионно-электронным методом.
SO2 + KMnO4 + H2O → MnO2 + K2 SO4 + H2SO4
![]()
![]() +
+ ![]()
![]()
![]() +
+ ![]()
![]() →
→ ![]()
![]() +
+ ![]()
![]()
![]() +
+ ![]()
![]()
![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |





