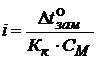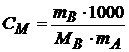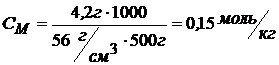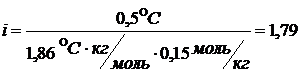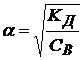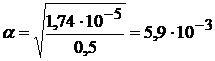ПР = .
Поскольку осадок выпадает из пересыщенных растворов, то условием образования осадка является превышение произведения молярных концентраций ионов труднорастворимого вещества в конкретном растворе над величиной ПР, т. е. 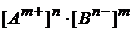 > ПР(AnBm)таб.
> ПР(AnBm)таб.
3.2.6. Примеры решения задач
Задача № 1.
Найти степень диссоциации гидроксида калия, если раствор, содержащий 4,2 г вещества и 0,5 дм3 воды, замерзает при -0,5°С.
Дано: mB = 4,2 г Vводы = 0,5 дм3 t°зам р-ра = - 0,5°С - αкаж - ? | Решение: КОН → К+ + ОН - → n = 2 – сильный электролит
∆t°зам = i · kк · СМ
∆t°зам = 0°C – (-0,5°C) = 0,5°C
MKOH = 39 + 16 + 1 = 56 г/моль
1<1,79<2
|
Ответ: кажущаяся степень диссоциации 0,79 или 79%.
Задача № 2
Определить степень диссоциации уксусной кислоты в 0,5 М растворе.
Дано: СВ = 0,5 М = 0,5 моль/дм3
α - ? | Решение: СН3СООН – слабая кислота Для слабых электролитов В приложении 3 находим значение константы диссоциации для уксусной кислоты КД = 1,74 · 10─5
|
Ответ: степень диссоциации 5,9 · 10─3.
Задача № 3
Выпадет ли осадок, если смешать 3 см3 0,000005 М раствора серной кислоты и 4 см3 0,00002 М раствора хлорида бария.
Решение:
H2SO4 + BaCl2 = BaSO4 ↓ + 2HCl
3 см3 + 4 см3 = 7 см3
Осадок выпадет в том случае, если концентрация получившегося в ходе реакции сульфата бария больше, чем в насыщенном растворе.
BaSO4 →Ba2+ + ![]()
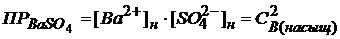 ,т. к.
,т. к. 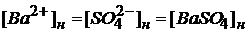
ПРтаб = 1,1 · 10─10 (значение взято в приложении 4)
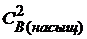 = 1,1 · 10─10
= 1,1 · 10─10
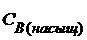 = 1,05 · 10─5 моль/дм3
= 1,05 · 10─5 моль/дм3
Найдем концентрации ионов бария и сульфат – ионов. Ионы бария содержатся в 4 см3 0,00002 М раствора хлорида бария, при добавлении 3 см3 0,000005 М раствора серной кислоты объем стал равен 7 см3 и концентрация ионов бария
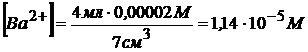
Концентрацию сульфат – ионов находим аналогично
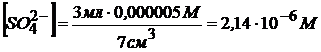
т. к. 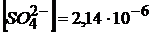 <СВ (насыщ) = 1,05 · 10─5 М осадок не выпадет.
<СВ (насыщ) = 1,05 · 10─5 М осадок не выпадет.
Ответ: осадок не выпадет
Задача № 4
В каком объеме может быть растворено 3 г иодида свинца (II).
Решение:
Чтобы найти объем насыщенного раствора PbI2, в котором содержится 3 г соли, надо знать концентрацию насыщенного раствора.
PbI2 → Pb2+ + 2I─
CB(насыщ) CB(насыщ) 2CB(насыщ)
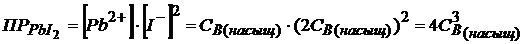
ПРтаб = 1,1 · 10─9 (значение взято в приложении 4)
4![]() = 1,1 · 10─9
= 1,1 · 10─9
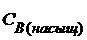 = 6,5 · 10─4 моль/дм3
= 6,5 · 10─4 моль/дм3
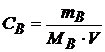 ,
,
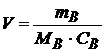
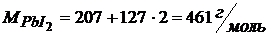
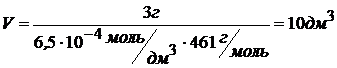
Ответ: 3 г иодида свинца можно растворить в 10 дм3 раствора.
Задача № 5
Степень диссоциации 0,1 Н раствора карбоната натрия при 0°С равна 70%. Вычислить осмотическое давление раствора.
Дано: Решение:
Na2CO3 По закону Вант-Гоффа
CЭ = 0,1 H
t º= 0ºC Росм = i · CB · R · T
αкаж = 70% = 0,7 R = 8,314 Дж/моль∙ К (универсальная газовая постоянная)
![]() T = t° + 273 = 0 + 273 = 273 K
T = t° + 273 = 0 + 273 = 273 K
Росм - ? СВ – молярная концентрация раствора, а в
условиях задачи дана нормальная концентрация, поэтому необходимо выполнить следующий расчет.
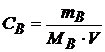 , а
, а 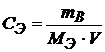 , поэтому
, поэтому
СВ · МВ = СЭ · МЭ, а 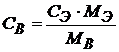
Найдем молярную и эквивалентную массу карбоната натрия
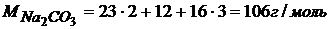
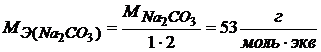 , где
, где
1 – валентность натрия; 2 – число атомов натрия в молекуле соли.
Тогда 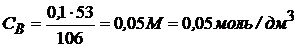
Зная степень диссоциации, можно найти изотонический коэффициент
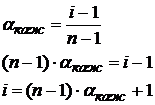
Из уравнение диссоциации соли Na2CO3 → 2Na+ + ![]() видно, что молекула образована тремя ионами (2 иона натрия и 1 карбонат - ион), поэтому
видно, что молекула образована тремя ионами (2 иона натрия и 1 карбонат - ион), поэтому
i = (3 – 1) · 0,7 + 1 =2,4
Подставляем полученные данные в формулу зависимости осмотического давления
Росм = 2,4 · 0,05 · 8,314 · 273 = 272,4 кПа
Ответ: осмотическое давление 272,4 кПа.
3.3 Ионное произведение воды и водородный показатель. Гидролиз солей
3.3.1. Ионное произведение воды и водородный показатель
Вода – самый слабый электролит, всего 1 из 10 молекул диссоциирует на ионы
Н2О ↔Н+ + ОН-
Степень диссоциации воды 1/ = 10-7
Константа диссоциации воды
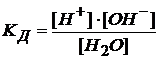 .
.
Поскольку молярная концентрация воды ![]() и константа диссоциации воды КД = 1,8 ∙ 10─16 (н. у.), то произведение этих постоянных
и константа диссоциации воды КД = 1,8 ∙ 10─16 (н. у.), то произведение этих постоянных 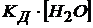 также величина постоянная и называется константой ионного произведения воды или константой воды –
также величина постоянная и называется константой ионного произведения воды или константой воды – ![]() . Таким образом
. Таким образом
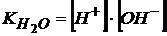 ;
;
при н. у. 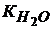 = 10─14.
= 10─14.
Для количественной оценки характера водной среды введен водородный показатель:
pH = –lg [H+].
Для нейтральной среды:
[H+] = [OH–] = 10–7, тогда pH = –lg [H+] = –lg 10–7 = 7.
Для кислой среды:
[H+] > [OH–] и pH < 7.
Для щелочной среды:
[H+] < [OH–] и pH > 7.
3.3.2. Гидролиз солей
Гидролиз солей – взаимодействие ионов соли с ионами воды, в результате которого образуется слабый электролит.
Гидролизу подвергаются:
1. Соли слабого основания и сильной кислоты
NH4Cl + HOH ↔ NH4OH + HCl
слабое основание сильная кислота
NH4+ + HOH ↔ NH4OH + H+
Растворы таких солей имеет, кислую реакцию.
Константа гидролиза соли в этом случае:
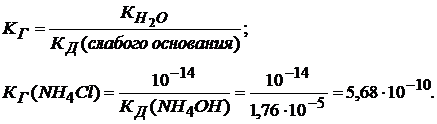
(КД – справочное значение).
Степень гидролиза:
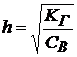 ,
,
где СВ – молярная концентрация раствора соли.
2. Соли сильного основания и слабой кислоты
KNO2 + HOH ↔ KOH + HNO2
сильное основание слабая кислота
![]() + HOH ↔ OH- + HNO2
+ HOH ↔ OH- + HNO2
Раствор таких солей имеет щелочную реакцию.
Константа гидролиза в этом случае:
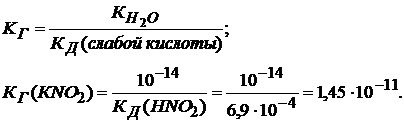
Степень гидролиза рассчитывается по формуле приведенной выше.
3. Соли слабого основания и слабой кислоты
4.
NH4F + HOH ↔ NH4OH + HF
слабое основание слабая кислота
Среда в растворах таких солей близка к нейтральной (слабокислая, если КД (кисл) > КД (осн) или слабощелочная, если КД (кисл) < КД (осн)) рН ≈ 7.
Константа гидролиза в этом случае
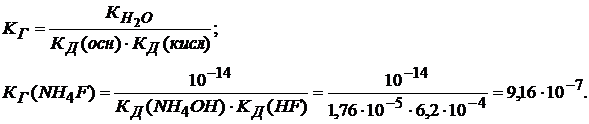
Степень гидролиза рассчитывается по формуле приведенной выше.
Соли сильного основания и сильной кислоты гидролизу не подвергаются. Растворы таких солей имеют нейтральную реакцию.
Ступенчатому гидролизу подвергаются соли, образованные многоосновными слабыми кислотами или слабыми основаниями 2х, 3х валентных металлов. Например, гидролиз Na2CO3 протекает в две ступени:
I cтупень Na2CO3 + HOH ↔ NaHCO3 + NaOH
CO32─ + HOH ↔ HCO3─ + OH─
среда щелочная, pH > 7
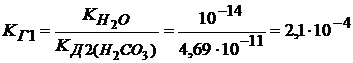
II ступень NaHCO3 + HOH ↔ H2CO3 + NaOH
HCO3- + HOH ↔ H2CO3 + OH-
среда щелочная, pH > 7
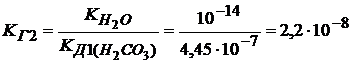
КГ1 = 2,1· 10–4 >> 2,2 · 10–8 = КГ2
Обратите внимание, что константа гидролиза по I ступени определяется константой II ступени диссоциации слабой кислоты (слабого основания) и наоборот. Поскольку для ступенчатого гидролиза КГ1 >> КГ2, то в расчетах часто второй и более высокими ступенями гидролиза пренебрегают.
3.3.3. Примеры решения задач
Задача № 1.
Найти рН 0,1 М раствора азотистой кислоты.
Решение:
HNO2 ↔ H+ + NO2–
слабая кислота
pH = –lg [H+]
Концентрация ионов водорода:
[H+] = α· CB
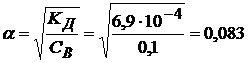 (
(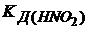 -значение взято из справочника)
-значение взято из справочника)
[H+] = 0,083 · 0,1 = 0,0083 
pH = –lg 0,0083 = 2,1
Ответ: рН = 2,1.
Задача № 2
Рассчитать рН 0,05 М раствора гидроксида аммония.
Решение:
pH = –lg [H+]
NH4OH ↔ NH4+ + OH–
слабое основание
[ОH–] = α· CB
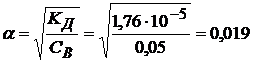 (
(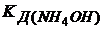 -значение взято из справочника)
-значение взято из справочника)
[ОH–] = 0,019 · 0,05 = 0,0009 ![]()
Зная, что в любом водном растворе произведение [H+] · [ОH–] = 10–14, найдем [H+].
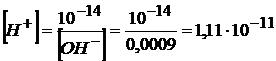
![]()
pH =–lg [H+] = –lg (1,11 · 10–11) = 10,95
Ответ: рН = 10,95.
Задача № 3.
Какая соль гидролизуется полнее: хлорит калия или нитрит калия. Написать уравнения гидролиза.
Решение:
Чтобы ответить на вопрос, какая соль гидролизуется полнее, необходимо рассчитать константы гидролиза этих солей, и та соль, у которой КГ больше, гидролизуется полнее.
Напишем уравнения гидролиза этих солей и найдем константы гидролиза:
KClO2 + HOH ↔ KOH + HClO2
сильное основание слабая кислота
![]() + HOH ↔ OH- + HClO2
+ HOH ↔ OH- + HClO2
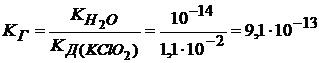
KNO2 + HOH ↔ KOH + HNO2
сильное основание слабая кислота
NO2─ + HOH ↔ OH - + HNO2
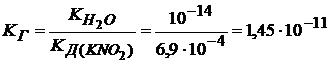
1,45 · 10–11 > 9,1 · 10–13
Ответ: нитрит калия гидролизуется полнее, т. к. ![]() .
.
Задача № 4.
Вычислить рН раствора азотной кислоты, в 300 см3 которого содержится 1,5 г кислоты.
Решение:
pH = –lg [H+]
HNO3 → H+ + NO3–
Азотная кислота – сильная, α = 1, поэтому ![]()
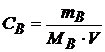 ;
;
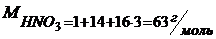
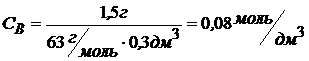
pH = -lg 0,08 = 1,1.
Ответ: рН = 1,1.
Задача № 5.
рН раствора гидроксида кальция 12. Найти молярную концентрацию раствора.
Решение:
Т. к рН = 12 можно найти концентрацию ионов водорода.
[H+] = 10–pH = 10─12 
В любом водном растворе [H+] · [OH–] = 10─14, поэтому, зная [H+], можно определить [OH–].
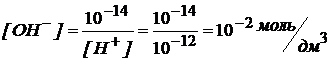
Ca(OH)2 = Ca2+ + 2OH–
Ca(OH)2 – сильное основание α = 1, поэтому можно найти концентрацию раствора Ca(OH)2 из соотношения коэффициентов в уравнении, т. е. [Ca(OH)2] в 2 раза меньше [ОН–].
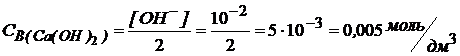 .
.
Ответ: концентрация раствора 0,005 .
.
Задача № 6.
Рассчитать константу гидролиза, степень гидролиза и рН раствора хлорида аммония концентрацией 0,1 М.
Решение:
NH4Cl – соль слабого основания и сильной кислоты ( pH < 7).
NH4Cl + HOH ↔ NH4OH + HCl
слабое основание сильная кислота
NH4+ + HOH ↔ NH4ОН + H+
Найдем 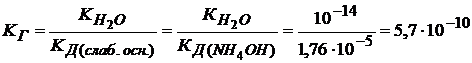
Степень гидролиза 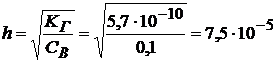
[H+] = h· CB = 7,5 · 10–5 · 0,1 = 7,5 · 10–6 
pH = –lg [H+]
pH = –lg (7,5 · 10–6) = 5,12
Ответ: h = 7,5 · 10–5; КГ = 5,7 · 10–10; рН = 5,12.
Задача № 7
Вычислить константу гидролиза, степень гидролиза и рН 0,1 М раствора сульфита калия. Учитывать только первую ступень гидролиза.
Решение:
K2SO3 – соль сильного основания KOH и слабой кислоты Н2SO3.
I ступень K2SO3 + HOH ↔ KHSO3 + KOH
![]() + HOH ↔ + OH-
+ HOH ↔ + OH-
среда в растворе этой соли щелочная, рН > 7.
Вычислим константу гидролиза по первой ступени
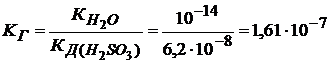
Зная концентрацию раствора (0,1 М) можно вычислить степень гидролиза.
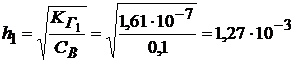 .
.
Чтобы определить рН, необходимо вычислить концентрацию ионов водорода
pH = –lg [H+]
Так как среда в растворе щелочная, то концентрация гидроксид-ионов равна произведению степени гидролиза и концентрации раствора
[ОH–] = h1· CB = 1,27 ∙ 10–3 ∙ 0,1 = 1,27 ∙ 10–4 , а в любом водном растворе [H+] · [ОH-] = 10–14следовательно,
, а в любом водном растворе [H+] · [ОH-] = 10–14следовательно,
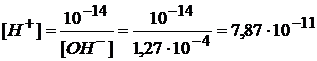
![]() .
.
Тогда pH =-lg [H+] = – lg (7,87 · 10–11) = 10,1
Ответ: h1 = 1,27 · 10–3; ![]() = 1,61 · 10–7; рН = 10,95.
= 1,61 · 10–7; рН = 10,95.
3.4. Комплексные соединения
3.4.1. Общие понятия о структуре комплексного соединения
Наиболее удачно свойства и строение комплексных соединений объясняет координационная теория, предложенная А. Вернером (1893 г.).
Основные положения этой теории:
1. В молекуле комплексного соединения один из ионов (обычно катион) занимает центральное место и называется комплексообразователем или центральным ионом.
2. Вокруг него в непосредственной близости расположено некоторое число противоположно заряженных ионов или молекул, называемых лигандами (аддендами). Они вместе с комплексообразователем образуют внутреннюю координационную сферу (комплексный ион). Суммарное число лигандов определяется координационным числом.
3. Остальные ионы находятся на более далеком расстоянии от комплексообразователя и составляют внешнюю координационную сферу (ион внешней сферы или внешний ион).
При написании химической формулы комплексного соединения комплексный ион выделяется квадратными скобками, в которых первым ставится комплексообразователь, а за ними лиганды. Частицы, находящиеся за квадратными скобками, составляют ион внешней сферы.
Наиболее часто в качестве комплексообразователя выступают:
Cu+ Ag+ Au+ (к. ч. = 2)
Cu2+, Hg2+, Cd2+, Pt2+, Pd2+, Zn2+ (к. ч. = 4)
Fe2+, Fe3+, Cr3+, Co2+, Ni2+, Al3+, Pt4+ (к. ч. = 6)
Ca2+, Sn2+ (к. ч. = 8)
В качестве лигандов в комплексном соединении могут быть некоторые молекулы и ионы, примеры названия которых перечислены ниже:
H2O - аква
NH3 - аммин
CO - карбонил
OH─ - гидроксо
Cl─ - хлоро
F─ - фторо
I─ - иодо
Br─ - бромо
CN─ - циано
CNS─ - родано
NO─2 - нитрито
NO─3 - нитрато
SO2─3 - сульфито
SO2─4 - сульфато
CO2─3 - карбонато
HCO─3 - гидрокарбонато
S2O2─3 – тиосульфато
и т. д.
Комплексообразователь и лиганды образуют комплексный ион, заряд которого равен сумме зарядов частиц, составляющих его. Заряд комплексного иона уравновешивается зарядом ионов внешней сферы.
3.4.2. Номенклатура комплексных соединений
Для указания числа лигандов используется греческие числительные:
1 – моно, 2 – ди, 3 – три, 4 – тетра, 5 - пента, 6 – гекса и т. д.
Название комплексного соединения формируется справа налево.
Для комплексных соединений с комплексным катионом: [Ag (NH3)2]Cl.
x x x x



![]()
![]() название иона внешней сферы
название иона внешней сферы
![]() количество лигандов (греч.)
количество лигандов (греч.)
![]() название лигандов
название лигандов
![]() русское название комплексообразователя в родительном падеже с указанием в скобках валентности
русское название комплексообразователя в родительном падеже с указанием в скобках валентности
[Ag (NH3)2]Cl хлорид ди – аммин серебра (I)
[Pt (NH3)4Cl2]Cl2 – хлорид ди-хлоро тетра – аммин платины (IV)
[Zn (H2O)4]SO4 – сульфат тетра – аква цинка (II)
[Cu (NH3)4](OH)2 – гидроксид тетра – аммин меди (II)
Для комплексных соединений с комплексными анионом: K4 [Fe (CN)6]
x x x x


![]()
![]()

![]() количество лигандов (греч.)
количество лигандов (греч.)
![]() название лигандов
название лигандов
латинское название комплексообразователя с добавлением окончания
![]() «ат», если есть окончание «ум», его заменить на «ат», указать валентность комплексообразователя
«ат», если есть окончание «ум», его заменить на «ат», указать валентность комплексообразователя
русское название иона внешней сферы в родительном падеже
K4 [Fe (CN)6] гекса – циано феррат (II) калия.
Примеры названий комплексообразователей с измененным окончанием:
Ag – аргентум - аргентат
Au – аурум - аурат
Pt – платина - платинат
Co – кобальт - кобальтат
Pb – плюмбум - плюмбат
Cu – купрум - купрат
Sn – станнум - станнат
Cd – кадмий – кадмиат
(NH4)2[Pt(OH)2Cl4] – тетра – хлоро, ди – гидроксо платинат (IV) аммония.
3.4.3. Диссоциация комплексных соединений в водных растворах
В водных растворах молекула комплексного соединения диссоциирует необратимо на комплексный ион и ион внешней сферы, так как между ними ионная связь:
[Ag(NH3)2]Cl → [Ag(NH3)2]+ + Cl─
NH4[Cr(CNS)4 (NH3)2] → NH4+ + [Cr(CNS)4(NH3)2]─
Диссоциация комплексного иона на комплексообразователь и лиганды ограничена (между ними донорно-акцепторная связь) и определяется константой диссоциации, называемой константой нестойкости комплексного иона (Кн). Значения констант нестойкости некоторых комплексных ионов приведены в приложении 5.
[Ag(NH3)2]+ ↔ Ag+ + 2NH3
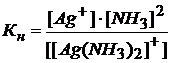

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |