СБОРНИК ОПИСАНИЙ ЛАБОРАТОРНЫХ РАБОТ
Лабораторная работа № 1
Приготовление раствора и определение его концентрации титрованием
Цель работы:
1. Приобретение навыков приготовления растворов из более концентрированного раствора.
2. Ознакомление с титрованием растворов.
Выполните расчет:
определите, сколько миллилитров раствора серной кислоты (концентрацией 12%, плотностью 1,083 г/мл) потребуется для приготовления 100 мл раствора ![]() заданной нормальности. Нормальная концентрация раствора задается преподавателем каждому студенту.
заданной нормальности. Нормальная концентрация раствора задается преподавателем каждому студенту.
Ход работы:
1. Приготовьте раствор серной кислоты. Для этого налейте в плоскодонную колбу объемом 100 мл небольшое количество (20-50 мл) дистиллированной воды. Налейте в мерительную пробирку рассчитанное количество миллилитров 12% серной кислоты и перелейте ее в колбу с водой. Закройте колбу притертой пробкой и, встряхивая колбу, перемешайте раствор. Долейте дистиллированную воду до калибровочной риски колбы (100 мл).
2. В каждую из двух конических колб налейте по 20 мл приготовленного раствора серной кислоты. Измерение объема выполняйте мерным цилиндром. Добавьте в каждую колбу капель раствора фенолфталеина.
3. Бюретку заполните 0,1 Н раствором NaOH немного выше верхней (нулевой) отметки. Нажимая на стеклянный шарик в резиновой трубочке бюретки, установите мениск раствора на нулевой отметке.
4. Титрование выполняйте следующим образом: к 20 мл раствора H2SO4 приливайте 0,1Н раствор NaOH, нажимая на стеклянный шарик в резиновом наконечнике бюретки. Добавляемую в кислоту щелочь непрерывно размешивайте круговыми движениями конической колбы. После появления первой окраски (исчезающей при перемешивании), раствор NaOH добавляйте по каплям.
Как только окраска раствора стала бледно-розовой, титрование прекратите. Возьмите отсчет по шкале бюретки объема раствора NaOH, израсходованного на титрование. Запишите результат первого титрования Vщ1 = … мл.
Долейте раствор NaOH до нулевой отметки бюретки и оттитруйте раствор H2SO4 во второй колбе. Запишите результат второго титрования Vщ2 = … мл.
Найдите среднее арифметическое значение результатов двух титрований Vщ (ср). Это объем NaOH, необходимый для титрования 20 мл приготовленного раствора кислоты.
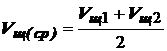
5. Рассчитайте по данным титрования значение нормальной концентрации приготовленного раствора кислоты. Расчет выполняйте по закону эквивалентов:
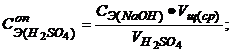
6. Рассчитайте погрешность опыта:
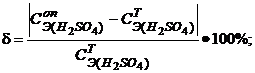
7. Вычислите титр приготовленного раствора.
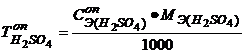
8. Все результаты сведите в таблицу. Сформулируйте вывод по результатам работы.
Содержание отчёта
Отчет должен содержать:
1. Все необходимые расчеты;
2. Таблицу приведенной ниже формы;
3. Вывод.
Таблица исходных данных и полученных результатов
| V12% H2SO4, мл |
| Объём раствора NaOH (щелочи), израсходованного на титрование |
| δ, % |
г/мл | ||
|
|
| ||||||
20 |
Лабораторная работа № 2
Зависимость скорости реакции от концентрации раствора и температуры
Опыт 1.
Цель опыта: установить зависимость скорости химической реакции от концентрации
реагирующих веществ.
Химические реактивы: сульфит натрия Na2SO3, подкисленный H2SO4; крахмал (внесен в раствор Na2SO3); иодат калия KIO3; дистиллированная вода.
Химическая посуда и оборудование: секундомер, мерительные цилиндры, химические стаканы.
Ход работы:
Скорость реакции в зависимости от концентрации исследуется на примере:
2KIO3 + 5Nа2SO3 + H2SO4 = K2SO4 + 5Na2SO4 + I2 + H2O
Приготовьте растворы иодата калия трех различных концентраций. Для этого отмерьте цилиндром 30 мл KIO3 и перелейте в стакан № 1. Затем отмерьте 20 мл KIO3, перелейте в стакан № 2 и добавьте туда же 10 мл Н2О. В третий стакан отмерьте 10 мл KIO3 и добавьте туда 20 мл Н2О. Воду отмерять тем же цилиндром, что и раствор KIO3 . Затем другим цилиндром отмерьте 30 мл Na2SO3.
Раствор Na2SO3 быстро прилейте в стакан № 1, одновременно с приливанием включите секундомер. В момент окончания реакции ( резкое изменение цвета раствора ) – выключите секундомер. Запишите в таблицу время, прошедшее с момента сливания растворов до появления синего окрашивания. Аналогично измерьте время реакции для стаканов № 2 и № 3, также быстро прилив туда по 30 мл сульфита натрия.
Заполните таблицу:
Опыт | Раствор / объем, мл | Относительная концентрация | Время реакции, с | Относительная скорость | ||
Na2SO3 | KIO3 | H2O | ||||
1 | 30 | 30 | 0 | 1,00 | ||
2 | 30 | 20 | 10 | 0,67 | ||
3 | 30 | 10 | 20 | 0,33 |
Относительную скорость (V) рассчитайте как Сотн. / t (относительная концентрация ко времени реакции).
Постройте график, откладывая по горизонтальной оси концентрации, а по вертикальной оси - относительную скорость реакции.
Сделайте вывод, основываясь на законе действия масс. Соответствует ли ваш график этому закону?
Опыт 2.
Цель опыта: установить зависимость скорости химической реакции от температуры.
Химические реактивы: тиосульфат натрия Na2S2O3, серная кислота H2SO4.
Химическая посуда и оборудование: секундомер, мерительные цилиндры, химические стаканы, пробирки, термометр.
Ход работы:
Скорость реакции в зависимости от температуры исследуется на примере:
Nа2S2O3 + H2SO4 = Na2SO4 + H2SO3 + S
Отмерьте мерительной пробиркой 3 раза по 3 мл H2SO4 и перелейте в три химические пробирки. Другой мерительной пробиркой также 3 раза по 3 мл отмерьте раствор Na2S2O3 и перелейте в 3 другие химические пробирки. Сгруппируйте пробирки в три пары (кислота – тиосульфат натрия).
Измерение 1. Возьмите первую пару пробирок и слейте оба раствора вместе. В момент сливания включите секундомер. При появлении слабой опалесценции выключите секундомер. Запишите в таблицу время реакции (“t, c”). Температура растворов равна комнатной, поэтому в графу “t0 c” запишите эту температуру по вашему термометру.
Измерение 2. Вторую пару пробирок поместите в стакан с теплой водой, предварительно опустив в одну из пробирок термометр. Как только температура одного из растворов станет на 10 0С выше температуры первого опыта, уберите термометр и быстро слейте содержимое пробирок. Время реакции запишите в таблицу.
Измерение 3. Проводится аналогично, но температуру третьей пары пробирок нужно установить на 10 0С выше температуры второго опыта.
Измере- ние | t,0C | Время, c | Относительная скорость | Температурный коэффициент |
1 | ||||
2 | ||||
3 |
Относительную скорость рассчитайте по формуле: 1/t. Определите температурный коэффициент ( ![]() ).
).
Сделайте вывод о влиянии температуры на скорость изученной реакции.
Лабораторная работа № 3
Комплексные соединения
Цель работы: ознакомиться с получением, строением и диссоциацией комплексных соединений, ознакомиться с диссоциацией и разрушением комплексных ионов.
Опыт 1. Получение ацидокомплекса серебра.
а) Мерительной пробиркой отмерить 1 мл раствора нитрата серебра и перелить в большую пробирку. К раствору нитрата серебра прилить 1 мл раствора хлорида калия.
Написать реакцию в молекулярном и ионном виде.
К осадку осторожно приливать, постоянно взбалтывая, раствор роданида калия до полного растворения осадка.
Написать реакцию образования комплексного соединения, разобрать строение этого соединения, учитывая, что координационное число серебра равно 2.
б) Написать реакции диссоциации данного комплексного соединения и комплексного иона данного соединения.
в) Выбрать вещество для разрушения данного комплексного иона, провести реакцию, медленно приливая выбранный раствор к раствору комплексного соединения, написать уравнение реакции, учитывая, что константа нестойкости данного комплексного иона равна 10-10.
Опыт 2. Получение ацидокомплекса свинца.
а) Мерительной пробиркой отмерить 1 мл нитрата свинца, перелить в большую пробирку. К раствору нитрата добавить 1 – 2 капли раствора иодида калия.
Написать реакцию в молекулярном и ионном виде.
К осадку осторожно приливать, постоянно взбалтывая, раствор гидрокарбоната натрия до полного растворения осадка.
Написать реакцию образования комплексного соединения, разобрать строение этого соединения, учитывая, что координационное число свинца
равно 4.
б) Написать реакции диссоциации данного комплексного соединения и комплексного иона данного соединения.
в) Выбрать вещество для разрушения данного комплексного иона, провести реакцию, медленно приливая выбранный раствор к раствору комплексного соединения, написать уравнение реакции, учитывая, что константа нестойкости данного комплексного иона равна 10-6.
Лабораторная работа № 4
Гидролиз солей и рН-метрия растворов
Цель работы: ознакомиться с гидролизом трех типов солей;
научиться составлять уравнения гидролиза;
познакомиться с методами определения водородного показателя (рН) водных растворов разной природы.
Опыт1. Окраска индикаторов в различных средах.
Возьмите 9 пробирок. Налейте в 3 пробирки по 1 мл. дистиллированной воды. В следующие 3 пробирки по 1 мл. 0,1 Н раствора NaOH, еще в 3 пробирки по 1 мл. 0,1 Н раствора HCl. В одну пробирку с водой, в одну с раствором щелочи и в одну с раствором кислоты добавьте по 1 – 2 капли раствора метилоранжа. Аналогично в три другие пробирки добавьте по 1 - 2 капли раствора фенолфталеина. И в оставшиеся 3 пробирки добавьте по 1 – 2 капли раствора лакмуса. Составьте таблицу окраски индикаторов в различных средах.
Опыт 2. Количественное определение рН раствора.
В пять пробирок налейте по 1 мл.: в одну 0,1 Н раствора соляной кислоты, в другую 0,1 Н раствора уксусной кислоты, в третью 0,1 Н раствора аммиака, в четвертую 0,1 Н раствора гидроксида натрия и в пятую – дистиллированной воды.
В каждую пробирку опустите ½ полоски индикаторной бумаги. Окраску индикаторной бумаги сравните с эталонной шкалой. Результаты определения рН запишите в таблицу.
Опыт 3. Гидролиз солей.
В четыре пробирки налейте по 1 мл.: в одну дистиллированной воды, в другую раствор Na2CO3, в третью – ZnCl2, в четвертую – KCl. В каждую из пробирок прилейте по 1 – 2 капли фиолетового раствора лакмуса и сравните окраску лакмуса в воде и в растворах солей.
Какие из испытуемых солей подверглись гидролизу? Составьте уравнение гидролиза.
Опыт 4. Гидролиз соли слабого основания и слабой кислоты.
К 1 мл. раствора сульфата алюминия прилейте 1 мл. раствора Na2CO3. Напишите молекулярное и ионное уравнения взаимодействия солей.
Какая из образовавшихся солей не подвергается гидролизу, а какая подвергается полному необратимому гидролизу? Составьте молекулярное уравнение полного необратимого гидролиза этой соли.
Опыт 5. Растворение металла в продукте гидролиза его соли.
Опустите кусочек цинка в пробирку с раствором хлорида цинка и нагрейте пробирку в горячей воде. Чем объяснить выделение водорода? Ответ подтвердите уравнениями реакций.
Лабораторная работа № 5
Окислительно-восстановительные реакции (ОВР)
Цель работы: приобретение навыков уравнивания окислительно - восстановительных реакций методом электронно-ионного баланса.
Ход работы: провести следующие три опыта, отметить цвет всех растворов до реакции и после. Определить коэффициенты в уравнениях ОВР методом электронно-ионного баланса.
Опыт 1.
В пробирку налить 1 мл 0,005 М раствора перманганата калия КМnO4. Затем прилиить1 мл 20 % раствора серной кислоты H2SO4 и 2 мл 0,5 Н раствора нитрита натрия NaNO2 или нитрита калия КNO2. Отметить изменения, происшедшие в результате реакции. Уравнять ОВР:
КМnO4 + H2SO4 + NaNO2 ® NaNO3 + MnSO4 + K2SO4 + Н2О
Опыт 2.
В пробирку налить 1 мл 0,005 M раствора перманганата калия KMnO4. Затем прилить 1 мл 2 H раствора соляной кислоты HCl и 2 мл 3 % раствора пероксида водорода H2O2. Отметить изменения, происшедшие в ходе реакции. Уравнять ОВР:
KMnO4 + HCl + H2O2 ® KCl + MnCl2 + H2O + O2
Опыт 3.
В большую пробирку поместить несколько кристалликов сульфата железа (II) FeSO4. Вместо сульфата железа можно использовать соль Мора. Затем прилить 2 мл 20 % раствора серной кислоты H2SO4. После полного растворения соли добавить 1 мл 0,005 М раствора перманганата калия KMnO4. Отметить изменения, происшедшие в результате реакций. Уравнять ОВР:
FeSO4 + H2SO4 + KMnO4 ® MnSO4 + Fe2(SO4)3 + K2SO4 + Н2О
Лабораторная работа № 6
Качественные реакции на катионы
Вода, используемая в быту и производстве и получившая загрязнения, которые изменили её свойства, называется сточной. Сточные воды подлежат уничтожению или отчистке. Методы очистки зависят от загрязнителей, и поэтому необходимо сначала установить, какие загрязнители присутствуют в данной сточной воде. Наиболее опасными загрязнителями являются ионы тяжелых металлов: Hg2+, Pb2+, Cd2+, Zn2+ из неметаллов – это цианид – ионы (СN-), примеси мышьяка и селена.
Обнаружение того или иного иона в растворе («открытие иона») производится с помощью качественных реакций на данный ион. Качественной называется реакция, дающая с искомым ионом или веществом какую-либо характерную реакцию (например, осадок определенного цвета).
Цель работы: Провести качественные реакции для открытия катионов металлов - загрязнителей воды.
Опыт 1. Открытие ионов ртути (2).
Хлорид олова (2) восстанавливает хлорид ртути (2) до белого осадка хлорида ртути (1) Hg2Cl2 (каломель), не растворимого в воде. При дальнейшем прибавлении SnCl2 каломель восстанавливается до черной порошковообразной металлической ртути. Реакция весьма чувствительна.
Выполнение реакции: Реакцию можно выполнить капельным методом. На фильтровальную бумагу нанести каплю исследуемой воды, добавить 1-2 капли раствора SnCl2 и каплю анилина. В присутствии ртути образуется бурое или черное пятно.
Опыт 2. . Открытие ионов кадмия (2).
Ионы Cd2+ образуют со щелочами нерастворимый осадок белого цвета Cd(OH)2. Гидроксид кадмия не растворим в избытке щелочи, но растворим в аммиаке, с которым он образуется комплексный ион [Cd(NH3)4]2+.
Выполнение реакции: В две пробирки налить по 1 см3 исследуемой воды, добавить 2Н раствор NaOH. Если в растворе есть Cd2+, то выпадает белый осадок Cd(ОН)2. На осадок в одной пробирке воздействовать раствором гидроксида натрия, на другой – 10%-ным раствором аммиака.
Написать необходимые реакции в молеулярном и кратном ионном виде.
Опыт 3. Открытие ионов свинца(2).
Качественными реактивами на ион Pb2+ является иодид – ион(I-), родизонат – ион (С6О62-), образующие с Pb2+ характерные осадки.
3.1. Открытие ионов свинца(2) с помощью иодида калия.
Выполнение реакции:
В пробирку налить 1 см3 исследуемой воды и по каплям добавить раствор иодида калия, который осаждает Pb2+ в виде иодида свинца, характерный желтый цвет.
Растворить осадок PbI2, нагрев пробирку с ним на водяной бане. При охлаждении раствора выпадает осадок в виде золотисто-желтых лепестков.
3.2. Открытие ионов свинца (2) с помощью родозонита натрия (Na2C6O6).
Выполнение реакции: Данная реакция очень чувствительна, поэтому её можно выполнить капельным методом. Каплю исследуемой воды нанести на фильтровальную бумагу, смочить образовавшегося пятно свежеприготовленным раствором 0,2%-ным водным раствором родизоната натрия. Появление пятна красного или фиолетового цвета указывает на присутствие Pb2+. Для усиления чувствительности реакции окрашенное пятно смочить буферным раствором рН которого равен 2,8.
Опыт 4. Открытие ионов цинка.
Цинк – энергичный комплексообразователь. Он образует комплексные ионы [Zn(SCH)4]2-. Осадок гидроксида цинка растворяется в водном растворе аммиака и в растворах тиоционидов с образованием указанных комплексных ионов.
Выполнение реакции: Налить в пробирку 1 см3 исследуемой воды, добавить 2Н раствор NaOH. В присутствии ионов цинка выпадает осадок.
Растворить осадок Zn(OH)2 воздействием на него:
а) 10%-го раствора NH3
б) раствора тиоцианида калия (КSCN) или тиоцианида аммония (NH4SCN).
Написать все необходимые реакции в молекулярном и кратном ионно
Лабораторная работа № 7
Качественные реакции на анионы
Цель работы: Обнаружение нитрат (![]() ) и нитрит (
) и нитрит (![]() ) ионов.
) ионов.
Опыт 1. Обнаружение нитрат – иона реакцией с дифениламином
Налейте в пробирку 1 мл дифениламина (С6Н5)2NH; 1,5 мл H2SO4 (конц.) и 1 мл анализируемого раствора (NaNO3). В присутствии ![]() появляется темно-синее окрашивание, вызываемое продуктами окисления дифениламина нитрат-ионом.
появляется темно-синее окрашивание, вызываемое продуктами окисления дифениламина нитрат-ионом.
Уравняйте реакцию:
(С6Н5)2NH + H2SO4 + NaNO3 → (С6Н5)4N2 + Na2SO4 + NO2 + H2O
Опыт 2. Обнаружение нитрат – иона реакцией с сульфатом железа (II). Поместите в пробирку 1 мл испытуемого раствора и кристаллик FeSO4 величиной с булавочную головку, после чего медленно прилейте по стенке пробирки несколько капель концентрированной серной кислоты. В месте соприкосновения двух жидкостей появляется бурое кольцо, вызванное образованием NO:
FeSO4 + HNO3 + H2SO4 → Fe2(SO4)3 + NO + H2O
Уравняйте реакцию.
При избытке соли железа образуется комплексное соединение:
FeSO4 + NO → [Fe(NO)]SO4
Опыт 3. Обнаружение нитрит – иона реакцией окисления иодидов. Фильтровальную бумагу пропитайте крахмальным раствором, затем последовательно поместите на нее по 1 капле 2 Н раствора уксусной кислоты, испытуемого раствора и 0,1 Н раствора иодида калия. В присутствии ![]() появляется синее пятно или кольцо.
появляется синее пятно или кольцо.
Реакция идет по уравнению:
KNO2 + CH3COOH + KI → CH3COOK + I2 + NO + H2O
Уравняйте реакцию. Объясните появление синего окрашивания.
Опыт 3. Обнаружение нитрит – иона реакцией с перманганатом калия. Поместите в пробирку 1 мл KMnO4, 1 мл H2SO4 (разб.) и нагрейте смесь доºС, затем прибавьте 1 мл КNO2. При этом раствор обесцвечивается, так как в кислой среде происходит окисление ![]() до
до ![]() , а
, а 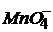 восстанавливается до Mn2+.
восстанавливается до Mn2+.
Уравняйте реакцию:
KMnO4 + H2SO4 + КNO2 → К2SO4 + MnSO4 + КNO3 + H2O
Лабораторная работа № 8
Дисперсные системы
Цель работы: Знакомство с методами получения и разрушения золей. Исследование физических свойств золей.
Опыт 1. Получение золей методом замены растворителя.
Получение золя серы. В пробирку с 5 мл дистиллированной воды добавьте 8-10 капель насыщенного спиртового раствора серы. Наблюдайте появление мутно-голубого окрашивания. Проследите за изменениями в жидкости вплоть до появления осадка. Чем его можно объяснить? Где лучше растворима сера – в спирте или в воде? Возможно ли образование коллоидного раствора, если вещество хорошо растворимо в данном растворителе? Можно ли назвать золь серы устойчивым?
Опыт 2. Получение золей химическим конденсационным методом.
2.1. Получение золя гидроксида железа. Налейте в химический стакан 25 мл дистиллированной воды и нагревайте на электрической плитке до кипения. В кипящую воду прилейте 1 мл 2% раствора FeCl3. Наблюдайте появление интенсивного окрашивания. Раствор сохраните. Этот опыт основан на гидролизе хлорида железа. Кипячение раствора способствует протеканию полного гидролиза. Напишите структуру мицеллы полученного золя гидроксида железа, считая ионы железа потенциалопределяющими.
2.2. Получение золя иодида серебра. Налейте в пробирку 2 мл раствора иодида калия и прибавьте одну каплю раствора нитрата серебра. Наблюдайте образование опалесцирующего золя. Напишите структуру мицеллы золя. Золь сохраните.
Опыт 3. Получение золей методом пептизации.
3.1. К 0,5 мл 2% раствора хлорида железа добавьте 1-2 капли 2Н раствора гидроксида натрия до образования осадка гидроксида железа.
Полученный осадок пептизируйте концентрированным раствором хлорида железа, для чего к свежему осадку добавьте концентрированный раствор FeCl3 до перехода осадка в прозрачный золь. Напишите структуру мицеллы золя и укажите тип пептизации.
3.2. Получите тот же осадок Fe(OH)3 и пептизируйте его, добавляя к осадку по каплям раствор соляной кислоты до перехода осадка в прозрачный золь. Напишите структуру мицеллы золя и укажите тип пептизации.
Опыт 4. Коагуляция золей.
4.1. Коагуляция золя железа. Налейте в пробирку 2 мл золя гидроксида железа, полученного в опыте 2.1 и подействуйте на него раствором сульфата натрия. Наблюдайте появление мути. Объясните коагулирующее действие электролитов.
4.2. Взаимная коагуляция золей. Приготовьте золь иодида серебра при избытке нитрата серебра, для чего к 2 мл раствора нитрата серебра прибавьте 1 каплю раствора иодида калия. Напишите структуру мицеллы этого золя. К полученному золю прилейте золь, полученный в опыте 2.2. Наблюдайте взаимную коагуляцию этих золей. Обьясните механизм наблюдаемого разрушения.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



