Получение глюкозамина гидрохлорида. Глюкозамина гидрохлорид был получен гидролизом хитина концентрированной соляной кислотой в соотношении 1:3 при 950С в течение 3 часов. С целью увеличения выхода конечного продукта на 5-7% нами введена дополнительная стадия, которая включает в себя добавление к гидролизату 10% (от объема гидролизата) этилового спирта, охлаждение до 50С, выдерживание реакционной смеси при этой температуре в течение 16 ч для кристаллизации соли.
Важным этапом в получении глюкозамина является его очистка от побочных продуктов гидролиза хитина. Установлено, что трехкратная обработка препарата этиловым спиртом в соотношении 2:1 при 800С в течение 10-15 минут с последующим освобождением от спирта фильтрованием позволило получить глюкозамина гидрохлорид со степенью чистоты 89%. Нами введена дополнительная стадия очистки активированным углем при соотношении глюкозамин:уголь 10:1, перемешивании и температуре 70-800С в течение 10 минут. После этого полученный бесцветный или бледно-желтый раствор подвергалсяя высушиванию на распылительной либо на лиофильной сушилке.
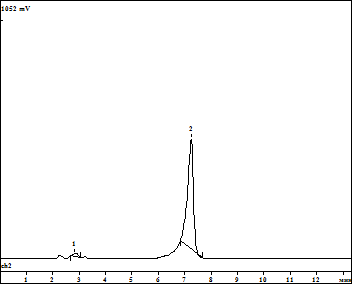
Степень чистоты полученного препарата была определена с использованием высокоэффективной обращенно-фазовой хроматографии. Как показали результаты хроматографических исследований (рисунок 1), введение этапа дополнительной очистки позволило получить препарат глюкозамина гидрохлорида со степенью чистоты 99,07 %.
| COLUMN: Shodex Asahipac NH2P-50 4E Size: 4.6x 250 mm Number: 709032 Part. size: 5.0 µm ELUENT: CH3CN : H2O = 70 :30 Flow: 0.80 мл/мин Temperature: 25.0 C Pressure: 86.0 бар No Retention Area Area Name мин mV*сек % 1 2 7.,51 99.07 _____________________________ 2 1300 |
Рисунок 1 Хроматограмма глюкозамина гидрохлорида
Схема комплексной переработки ХСО креветки. В результате проведенных исследований предложена схема технологии комплексной переработки отходов креветки для получения хитина, хитозана глюкозамина гидрохлорида и белкового гидролизата (рисунок 2). Разработанная технология апробирована и используется в промышленных условиях на предприятии .
| ||
| ||
Гомогенизация | ||
| ||
|
| |
| Инактивация фермента | |
| ||
Отстаивание | ||
| ||
| ||
| ||
Раствор гидролизата |
| |
| ||
Сушка |
| Депротеинирование (3 часа) |
|
| |
Порошок гидролизата
|
| Промывка водой до рН 7,5 |
Упаковка |
| |
| Деминерализация (2 часа) | |
| ||
| Промывка водой до рН 7,5 | |
| Хитин | |
| ||
|
| Деацетилирование (2 часа) |
| ||
| Гидролиз (3 часа) | Промывка водой до рН 7,5 |
|
| |
Охлаждение до (5±1ºС) | Хитозан | |
|
| |
Кристаллизация (16-18 ч.) | Сушка | |
|
| |
| Расфасовка | |
| ||
| Промывка | НCl |
| ||
| Растворение осадка | Фильтрат |
| ||
| Очистка раствора | |
| ||
Фильтрация | ||
| ||
Сушка | ||
| ||
| ||
Глюкозамина гидрохлорид | ||
| ||
| ||
Упаковка |
Рисунок 2 Технологическая схема комплексной переработки
отходов креветки
Доклинические исследования белкового гидролизата и глюкозамина гидрохлорида.
Исследование белкового гидролизата. Острая токсичность белкового гидролизата была определена внутрижелудочным введением белым мышам в дозах от 1000 до 6000 мг/кг. Установлено, что введение гидролизата во всех тестируемых дозах ни в одном случае не привело к гибели животных. У всех мышей отсутствовали признаки интоксикации. В связи с тем, что верхняя доза была максимально возможной для внутрижелудочного введения, значение LD50 исследуемого препарата превышало 6000 мг/кг. Согласно общепринятой классификации и общим требованиям безопасности ГОСТ 12.1.007, белковый гидролизат был отнесен к малоопасным веществам (IV-ый класс опасности по ГОСТ 12.1.007).
При изучении субхронической токсичности на белых крысах было выявлено, что при внутрижелудочном введении в дозах 1000, 2000 и 4000 мг/кг в течение 14 дней гидролизат не оказывал отрицательного влияния на функцию жизненно важных органов и систем лабораторных животных.
Нанесение белкового гидролизата на слизистую конъюнктивы глаз кроликов показало, что препарат оказывал слабое раздражающее действие (не более 1 балла).
При изучении аллергизирующего (сенсибилизирующего) действия гидролизата из отходов креветки методом реакции непрямой дегрануляции тучных клеток установлено, что при однократном подкожном введении морским свинкам в дозе 0,2 мл/кг препарат сенсибилизацию организма не вызывал. При накожном ежедневном нанесении гидролизата в течение 7 суток раздражающего действия также не установлено.
Исследование глюкозамина гидрохлорида. Путем внутрижелудочного введения препарата белым крысам в нарастающих дозах от 2000 до 12000 мг/кг изучена острая токсичность глюкозамина гидрохлорида. Установлено, что LD50 глюкозамина гидрохлорида превышало 12000 мг/кг при отсутствии у животных признаков интоксикации. Таким образом, глюкозамина гидрохлорид был отнесен к малоопасным веществам (IV-ый класс опасности по ГОСТ 12.1.007). Дальнейшие исследования препарата свидетельствовали об отсутствии отрицательного влияния на функцию жизненно важных органов и систем белых крыс при многократном внутрижелудочном введении, слабом раздражающем действии на слизистую конъюнктивы глаза кроликов и отсутствии сенсибилизирующего действия на организм морских свинок.
Эффективность применения сукцината хитозана в комплексе с пробиотическим препаратом «Проваген». Задача заключалась в оценке влияния сукцината хитозана в сочетании с пробиотическим препаратом «Проваген» на интенсивность роста и развития телят, динамику морфологических и биохимических показателей крови подопытных животных, на микрофлору содержимого желудочно-кишечного тракта.
В ходе эксперимента установлено, что введение в рацион испытуемого пробиотика и его комплекса с сукцинатом хитозана способствовало увеличению живой массы опытных животных, по сравнению с контролем, на 4,2% и 6,3%, соответственно (таблица 6).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |