Составить письменные конспекты вопросам самоподготовки.
Литература:[1, с. 191-200, 208-211,]; [2, с. 122-126]; [3, с. 31-32, 28-29]; [4, с. 126-128]; [6].
Задание 1 Провести количественное определение лекарственного вещества.
По методу количественного определения написать: уравнение реакции, лежащее в основе метода, расчет фактора эквивалентности, расчет титра и процентного содержания лекарственного вещества, провести статистическую обработку результатов анализа по обоим методам и данные представить в виде таблицы по предлагаемой форме (табл. 1), охарактеризовать методы в плане требований (табл. 2)
Таблица 1
Название метода | Навеска вещества, а | Объем титранта, V(мл) | Содержание х % | Статистические данные | ||||||
| S2 | S | S | Δ | Еотн |
| ||||
а1- а2- а3- а4- а5- | V1 – V2 – V3 – V4 – V5 - | х1- х2- х3- х4- х5- | ||||||||
а1- а2- а3- а4- а5- | V1 – V2 – V3 – V4 – V5 - | х1- х2- х3- х4- х5- |
Таблица 2
№ п/п | Требования к методам анализа | Методы | |
1-ый метод | 2-ой метод | ||
1 | Специфичность | ||
2 | Селективность (избирательность) | ||
3 | Унификация | ||
4 | Воспроизводимость (точность). Характеризует S (стандартное отклонение). | ||
5 | Правильность (достоверность)
| ||
6 | Безвредность, доступность, устойчивость реагента | ||
7 | Экономичность (дешевизна) | ||
8 | Простота методики выполнения | ||
9 | Экспрессность (быстрота) |
Варианты лабораторной работы по количественному
определению ЛВ химическими методами.
№ варианта | Лекарственное вещество | Методы определения |
1 | Раствор кальция хлорида | Комплексонометрическое, Аргентометрическое |
2 | Кислота аскорбиновая | Йодатометрическое, Алкалиметрическое |
3 | Йодатометрическое, Йодометрическое | |
4 | Алкалиметрическое, Йодометрическое | |
5 | Раствор пероксида водорода 3% | Перманганатометрическое, Йодометрическое |
6 | Магния оксид | Комплексонометрическое, Ацидиметрическое |
7 | Новокаин | Нитритометрическое, Аргентометрическое |
8 | Аргентометрическое, Алкалиметрическое | |
9 | Нитритометрическое, Алкалиметрическое |
Методики количественного определения
лекарственных веществ.
1. Раствор кальция хлорида 10% (Мr 219, 08).
10 мл препарата помещают в мерную колбу вместительностью 100 мл и доводят объем раствора водой до метки.
1.1. Комплексонометрическое определение. (ГФ X, ст. 120).
10 мл полученного раствора переносят в колбу для титрования, добавляют 15 мл воды, 5 мл аммиачного буферного раствора, 0,12 г индикаторной смеси или 7 капель раствора кислотного хром темно-синего и титруют раствором трилона Б (0,05 моль/л) до появления сине - фиолетового окрашивания.
1.2. Аргентометрическое определение.
К 5 мл разведения прибавляют 1-2 капли калия хромата и титруют раствором серебра нитрата (0,05 моль/л) до появления красноватого осадка.
2. Раствор пероксида водорода 3% (Мr 34,01).
10 мл раствора пероксида водорода помещают в мерную колбу вместимостью 100 мл и доводят объем раствора водой до метки.
2.1. Перманганатометрическое определение (ГФ X, ст. 621).
К 10 мл разведения прибавляют 5 мл кислоты серной разведенной и титруют раствором калия перманганата 0,1 моль/л, (УЧ 1/5 КМnО4) до появления слабо-розового окрашивания.
2.2. Йодометрическое определение. 10 мл разведения помещают в склянку с притертой пробкой, прибавляют 5 мл 10% раствора калия йодида, 5 мл кислоты серной разведенной и оставляют в темном месте на 10 минут. Титруют раствором натрия тиосульфата (0,1 моль/л) до обесцвечивания раствора (индикатор - крахмал).
3. Магния оксид (Мr 40,32)
Около 0,5 г препарата (точная навеска) растворяют в 40 мл раствора кислоты хлороводородной (0,1 моль/л) в мерной колбе вместимостью 250 мл и доводят объем раствора водой до метки.
3.1. Комплексонометрическое определение (ГФ X, ст. 380).
К 25 мл полученного разведения прибавляют 20 мл воды, 10 мл аммиачного буферного раствора и титруют при энергичном перемешивании раствором трилона Б (0,05 моль/л) до появления синего окрашивания (индикатор - кислотный хром черный специальный).
3.2. Ацидиметрическое определение.
К 20 мл разведения прибавляют 2-3 капли раствора метилового оранжевого и титруют раствором натрия гидроксида (0,1 моль/л) до появления желтого окрашивания.
Содержание магния оксида рассчитывают по формуле:
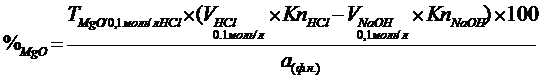
4. Кислота аскорбиновая (Мr 176,13.)
Около 0,5 препарата (т. н.) растворяют в воде в мерной колбе вместимостью 50 мл, доводят объем водой до метки и перемешивают.
4.1. Йодатометрическое определение (ГФ X, ст. 6).
К 10 мл разведения прибавляют 0,5 мл 1% раствора калия иодида, 2 мл раствора крахмала и 1 мл 2% раствора кислоты хлороводородной и титруют раствором калия йодата 0,1 моль/л (УЧ 1/6 КIO3,) до появления стойкого слабо-синего окрашивания.
4.2. Алкалиметрическое определение.
К 20 мл разведения прибавляют 5-7 капель раствора фенолфталеина и титруют раствором натрия гидроксида (0,1 моль/л) до появления розового окрашивания.
4.3. Йодометрическое определение.
К 10 мл разведения прибавляют 1-2 мл крахмала и титруют раствором йода 0,1 моль/л (УЧ 1/2 I2,) до появления синего окрашивания.
5. Новокаин (Мr. 272,8.)
5.1. Нитритометрическое определение (ГФ X, ст. 467).
Около 0,3 г препарата (точная навеска) растворяют в смеси 10 мл воды и 10 мл разведенной кислоты хлороводородной. Добавляют воды до общего объема 80 мл, 1 г калия бромида, 3 капли нейтрального красного и при постоянном перемешивании медленно титруют раствором натрия нитрита (0,1 моль/л) от малиновой окраски до голубой. Либо используют индикатор - 4 капли раствора тропеолина 00 и 2 капли метиленовой сини, титруют от красно-фиолетовой окраски до голубой.
5.2. Аргентометрическое определение.
Около 0,1 г препарата (точная навеска) растворяют в 10 мл воды, прибавляют 2-3 капли раствора бромфенолового синего и по каплям кислоту уксусную разведенную до перехода фиолетового окрашивания в зеленовато-желтое и титруют раствором серебра нитрата(0,05 моль/л) до появления фиолетового окрашивания.
5.3. Алкалиметрическое определение.
Около 0,3 г препарата (точная навеска) растворяют в 10 мл воды, прибавляют 5 мл нейтрализованной по фенолфталеину смеси спирта этилового с хлороформом (1:2), 3-5 капель раствора фенолфталеина и титруют при перемешивании раствором натрия гидроксида (0,1 моль/л) до слабо-розового окрашивания водного слоя.
Задание 2 Оформить протокол исследования, как часть «пояснительной записки» к проекту ФСП.
Пример.
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
К ПРОЕКТУ ФСП 42-1-01 В ЧАСТИ «КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КАЛИЯ ХЛОРИДА»
Определение адекватности фармакопейного (аргентометрического) и меркуриметрического методов анализа калия хлорида (КС1; Мr 74,56)
Стандартный метод
Около 1 г препарата (точная масса) растворяют в воде в мерной колбе вместимостью 50 мл и доводят объём раствора водой до метки. Аликвоту объемом 5 мл полученного раствора разбавляют водой до 40 мл и титруют раствором серебра нитрата (0,1 моль/л) до появления оранжевого окрашивания (индикатор - калия хромат).
КСl + AgN03 = AgCl![]() + КNO3
+ КNO3
Э. м. = Мr = 74,56;
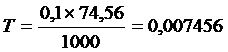 г
г
В лабораторном оформлении были представлены бюретки вместимостью 25 мл, следовательно, рационально было определять величину пробы на анализ в расчете на 20 мл титранта, т. е.: 0,007456 ![]() 20 = 0,15г. С учётом планирования 5-6 параллельных анализов массу пробы увеличивали в 10 раз. Таким образом, величина пробы на анализ составила 1,5 г. В итоге скорректированная методика отличалась от изложенной выше только величиной массы пробы на анализ (для серии однотипных измерений).
20 = 0,15г. С учётом планирования 5-6 параллельных анализов массу пробы увеличивали в 10 раз. Таким образом, величина пробы на анализ составила 1,5 г. В итоге скорректированная методика отличалась от изложенной выше только величиной массы пробы на анализ (для серии однотипных измерений).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



