15. Уясните понятие значащих цифр на примере ряда: 0,104; 1,04; 104; 1,04·10-4. Какие из приведённых цифр являются недостоверными?
16. Покажите различную степень недостоверности чисел в зависимости от формы её записи на примере: 11000; 1,10·104.
17. Чему равна недостоверность двух чисел: 0,0105 г, 10,5 мг?
18. Вычислите суммарную концентрацию ионов ОН - ряда отдельных значений: 4,00·10-2; 5,55·10-3; 1·10-6. Запишите в округлённом виде результат, ориентируясь на слагаемое с наименьшей абсолютной недостоверностью.
19. Найдите для числа «123» количество значащих цифр, абсолютную и относительную погрешности записи указанного числа.
20. Какой из следующих текстов взят из фармакопейной статьи?
а) Потеря в массе должна быть не менее 36,6%.
б) Потеря в массе была не менее 36,6%.
в) Потеря в массе будет не менее 36,6%.
г) Потеря в весе не менее 36,6%.
21. Как правильно сформулировать текст фармакопейной статьи:
а) 1,5 г препарата взбалтывали с 30 мл воды и фильтровали...
б) 1,5 г препарата надо взболтать с 30 мл воды и отфильтровать...
в) 1,5 г препарата должны взболтать с 30 мл воды и отфильтровать...
г) 1,5 г препарата взбалтывают с 30 мл воды и фильтруют...
д) 1,5 г препарата нужно будет взболтать с 30 мл воды и отфильтровать...
Эталоны ответов:
15. Каждое число имеет по 3 значащих цифры. Цифры 1 и 0, стоящие в середине, достоверны, а цифры 4 - недостоверны.
16. ±l,±lx 102 (то есть ± 100).
17. Одинаковая, т. е. ±1 (± 0,0001 г или ± 0,1 мг.)
18. 4,56·10-2 М.
ЛАБОРАТОРНОЕ ЗАНЯТИЕ № 2
Тема: Стандартизация методик количественного определения лекарственных средств физико-химическими методами.
Цель: Освоение статистической обработки экспериментальных данных и закрепление навыков работы по выбору физико-химического метода количественной оценки качества лекарств, навыков оформления протокола исследования, как части фармакопейной статьи.
Самостоятельная подготовка. Характеристики физико–химических методов по чувствительности, специфичности, точности (знать для объективной характеристики метода), аналитические сигналы и единицы измерения в инструментальных методах, основные методологические варианты использования спектроскопии для качественного анализа.
Составить письменные конспекты по вопросам самоподготовки.
Литература: [1, с. 29-46]; [2, с. 67-78]; [4, с. 262-270, 333-338]; [5, с. 12-39]; [6].
Самостоятельная работа студентов.
Задание 1 Провести фотометрическое исследование анализируемого вещества.
1. Нахождение длины волны рабочего светофильтра: провести фотометрическое исследование стандартного раствора, построить график зависимости оптической плотности А(D) от длины волны (λ), найти максимум на графике;
2. Выявление оптимальной рабочей концентрации стандартного раствора и толщины слоя фотометрируемого раствора (кюветы), полученные данные занести в таблицу 1
Таблица 1
Длина волны, нм | Концентрация, % | Толщина слоя, см | Оптическая плотность |
3. Рассчитать удельный показатель поглощения анализируемого вещества.
Задание 2 Проверить подчинение закону Бугера – Ламберта – Бера:
1. Приготовить 7-10 эталонных растворов различной концентрации (для интервала плотностей 0,2 – 0,8)
2. Измерить оптические плотности приготовленных растворов, данные представить в виде таблицы 2,
Таблица 2
Концентрация, % | Объем стандартного раствора, мл | Общий объем эталонного раствора, мл | Оптическая плотность | |||
1 | 2 | 3 | Среднее | |||
3. построить «грубый» калибровочный график.
Задание 3 Рассчитать и сделать статистическую оценку параметров линейной зависимости:
1. Рассчитать основные метрологические характеристики (коэффициент корреляции, угловой коэффициент и свободный член линейной зависимости), данные представить в виде таблицы 3
Таблица 3
№ | С | D | C2 | C·D | D2 | Dp | Dp-Dn | (Dp-Dn) |
1 | ||||||||
2 | ||||||||
Σ |
2. Рассчитать величину оптических плотностей по уравнению калибровочного графика.
3. Построить калибровочный график линейной зависимости рассчитанных величин оптических плотностей от концентрации.
Задание 4 Сформулировать методику определения и провести ее апробацию.
1. Составить схему приготовления растворов для фотометрирования предложенной ЛФ,
2. Сформулировать окончательную методику,
3. Приготовить растворы и провести их фотометрирование.
4. Рассчитать содержание фотометрируемого компонента в ЛФ,
5. Провести статистическую обработку полученных данных.
Отчет о проделанной работе представить в виде стандартных сброшюрованных листов, которые должны содержать:
а) проект НТД на количественное определение фотометрируемого компонента в лекарственной форме, который включает информацию о составе ЛФ, описание органолептических свойств, подробную текстовую методику анализа, расчетные формулы по обработке конечных данных и информации о допустимом содержании анализируемого компонента;
б) пояснительную записку с подробным обоснованием сформулированной методики фотометрического анализа, расчетами предварительных аналитических данных и конечными результатами количественного определения.
Объекты фотометрического анализа.
1. Рибофлавина 0,01% - 10,0
Кислоты аскорбиновой
Кислоты никотиновой по 0,02
2. Раствор рибофлавина 0,02% - 500,0
3. Рибофлавина 0,005
Натрия хлорида 0,9
Воды для инъекций до 100 мл.
4. Кислоты фолиевой 0,005
Глюкозы 0,25
5. Фурагина растворимого 0,1
Натрия хлорида 0,9
Воды для инъекций до 100 мл
6. Фурацилина 0,1 в табл.
7. Раствор бриллиантовой зелени 1% - 20,0
8. Раствор бриллиантовой зелени 0,5% - 50,0
9. Раствор фурагина растворимого 1% - 50,0
10. Раствор хинозола 5% - 100,0
Пример отчета о выполненной работе.
Проект ФСП 42-2-01 на метод количественного определения лекарственной формы состава:
Раствор рибофлавина 0,01 % - 10,0
Описание. Прозрачная жидкость жёлтого цвета, без запаха.
Количественное определение. 2 мл препарата помещают в пробирку и добавляют точно 8 мл воды очищенной. Тщательно перемешивают и измеряют оптическую плотность полученного раствора на фотоколориметре типа КФК (светофильтр с длиной волны 440 нм) в кювете с толщиной слоя 1 см. В качестве раствора сравнения используют воду. Содержание рибофлавина (х) в граммах вычисляют по формуле:
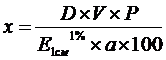
![]() ,
,
где: D - оптическая плотность полученного раствора;
V - объем фотометрируемого раствора, мл;
Р - величина одной дозы (фасовки) лекарственной формы, мл;
![]() - удельный показатель рибофлавина при светофильтре с длиной волны 440 нм;
- удельный показатель рибофлавина при светофильтре с длиной волны 440 нм;
а - величина пробы (объем, мл) препарата, взятая на анализ;
100 - фактор пересчета из процентов в граммы.
Содержание рибофлавина должно быть в пределах 0,0008 - 0,0012 г, считая на объем лекарственной формы.
Разработчик, студент _________________группы
Фамилия, имя, отчество (подпись)
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА К ПРОЕКТУ ФСП 42-2-01 НА МЕТОД КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЛЕКАРСТВЕННОЙ ФОРМЫ СОСТАВА:
Раствор рибофлавина 0,01% -10,0.
1. Исследование фотометрических характеристик.
500 |
600 |
Для проведения предварительных испытаний по выявлению аналитических фотометрических характеристик анализируемого вещества использовали 0,02% раствор рабочего стандартного образца* (РСО) рибофлавина. Указанный раствор фотометрировали на фотоколориметре типа КФК последовательно на всех светофильтрах, используя кювету толщиной слоя 1 см. Раствором сравнения служила вода очищенная.
Поскольку величина оптической плотности в случае использования светофильтра с длиной волны 440 нм превышала значение 2,0, что, как известно, отягощено большой ошибкой, то раствор РСО разбавили до 0,002% и повторно фотометрировали при данном значении длины волны. Оптическая плотность в этом случае составила величину 0,573.
По данным эксперимента (см. табл.1.1) построили график зависимости (рис.1) оптической плотности от длины световой волны (спектр). Максимум поглощения наблюдается при светофильтре с длиной волны 440 нм.

Рис. 1 Спектр поглощения рибофлавина.
*Рабочим стандартным образцом (РСО) считают раствор субстанции, из которой приготавливают лекарственные формы и отвечающую требованиям соответствующей фармакопейной статьи.
Таблица 1.1
Результаты предварительных фотометрических
испытаний раствора РСО рибофлавина
Длина волны светофильтра, нм | Концентрация, % | Оптическая плотность, A |
315 | 0,02 | 0,000 |
340 | 0,02 | 0,333 |
400 | 0,02 | 1,862 |
440 | 0,02 | 2,268 |
490 | 0,02 | 0,878 |
540 | 0,02 | 0,029 |
590 | 0,02 | 0,022 |
670 | 0,02 | 0,02 |
750 | 0,02 | 0,014 |
870 | 0,02 | 0,00 |
440 | 0,002 | 0,573 |
По данным эксперимента находили удельный показатель поглощения 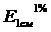 рибофлавина в данных условиях по формуле:
рибофлавина в данных условиях по формуле:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



