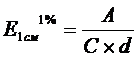 ,
,
где: А - оптическая плотность испытуемого раствора;
С - концентрация рабочего стандартного раствора, в процентах;
d - толщина слоя, см.
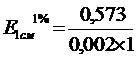
С целью проверки подчиненности закону Ламберта - Бугера -Бера приготовили серию из 7 эталонных растворов рибофлавина с интервалом концентраций 0,005 - 0,0035%. Предварительный расчет концентраций для диапазона оптических плотностей 0,2 - 1 ,0 показал, что минимальная (Сmin = 0,2/286,5) составляет 0,0007%, а максимальная (Сmax = 1,0/286,5) - 0,0035%. Для приготовленной серии эталонных растворов проводили измерения оптических плотностей в трех повторностях, результаты которых приведены в табл. 2.1
Таблица 2.1
Оптические плотности эталонных растворов
Концентрация, % | Объем стандартного раствора, мл | Общий объем, мл | Оптическая плотность, измерения | |||
1 | 2 | 3 | Среднее | |||
0,0005 | 0,25 | 10 | 0,163 | 0,165 | 0,167 | 0,165 |
0,0010 | 0,50 | 10 | 0,293 | 0,294 | 0,292 | 0,293 |
0,0015 | 0,75 | 10 | 0,425 | 0,426 | 0,426 | 0,426 |
0,0020 | 1,00 | 10 | 0,573 | 0,573 | 0,573 | 0,573 |
0,0025 | 1,25 | 10 | 0,691 | 0,693 | 0,692 | 0,692 |
0,0030 | 1,50 | 10 | 0,793 | 0,794 | 0,794 | 0,794 |
0,0035 | 1,75 | 10 | 0,946 | 0,950 | 0,948 | 0,948 |
2. Расчет параметров линейной зависимости и статистическая оценка.
Расчет метрологических характеристик линейной зависимости проводился по результатам аналитической информации, приведенной в табл. 3.1
Таблица 3.1
Параметры линейной зависимости
№ | С | D | С2 | C·D | D2 | Dp | Dp-Dn | (Dp-Dn) |
1 | 0,0005 | 0,165 | 2,5·10-7 | 8,25·10-5 | 0,0272 | 0,169 | 0,004 | 1,6·10-5 |
2 | 0,0010 | 0,293 | 10·10-7 | 29,3·10-5 | 0,0858 | 0,298 | 0,005 | 2,5·10°-5 |
3 | 0,0015 | 0,426 | 22,5·10-7 | 63,9·10-5 | 0,1815 | 0,428 | 0,002 | 0,40·10-5 |
4 | 0,0020 | 0,573 | 40·10-7 | 114,6·10-5 | 0,3283 | 0,557 | 0,016 | 25,6·10-5 |
5 | 0,0025 | 0,692 | 62,5·10-7 | 173·10-5 | 0,4789 | 0,686 | 0,006 | 3,6·10-5 |
6 | 0,0030 | 0,794 | 90·10-7 | 238·10-3 | 0,6304 | 0,815 | 0,021 | 44,1·10-5 |
7 | 0,0035 | 0,948 | 122·10-7 | 331,8·10-3 | 0,8987 | 0,944 | 0,004 | 1,6·10-5 |
Σ | 0,014 | 3,891 | 3,5·10-5 | 0,00959 | 2,6308 | - | - | 0,000794 |
Коэффициент корреляции (r), вычисленный по уравнению:
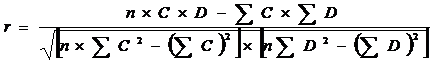
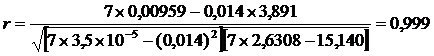
позволяет сделать заключение о жесткости изучаемой линейной зависимости между концентрациями и величинами оптических плотностей растворов рибофлавина.
Угловой коэффициент (b) и свободный член (а) линейной зависимости, вычисленные по уравнениям:
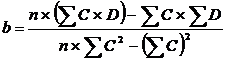
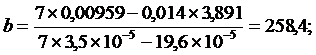
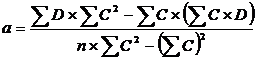
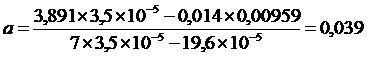
использовали для расчетов исправленных значений оптических плотностей (Dр) по формуле:
Dр =Cb + a, или: Dр =Cх 258,4 + 0,039.
Рассчитанные величины заносили в табл. 3.1 и на основании вновь полученных данных строили график (рис.2) линейной зависимости оптических плотностей (Dp) от концентраций (Сn).

Рис. 2. График линейной зависимости оптической плотности от концентрации раствора рибофлавина.
2. Формулирование и апробация методики количественного анализа лекарственной формы.
Для фотометрирования готовили растворы рибофлавина 0,002% концентрации в расчете на то, что наименьшее отклонение оптических плотностей от истинных значений обычно наблюдается в окрестностях центра графика. Для этого лекарственную форму «раствор рибофлавина 0,01%» следует разбавить в 5 раз (0,01/0,002 = 5). При использовании кюветы с толщиной слоя 1см следует приготовить не менее 10 мл фотометрируемого раствора.
Итак, рабочая методика количественного анализа рибофлавина для лекарственной формы «Раствор рибофлавина 0,01%» формулируется следующим образом: к 2 мл (пипетка ГОСТ 20922 - 74; 2 мл) лекарственной формы добавили 8 мл (пипетка ГОСТ тот же, 10 мл) воды очищенной. Перемешали. Полученный раствор фотометрировали при тех же условиях (светофильтр с длиной волны 440 нм, толщина слоя кюветы 1 см). Готовили три раствора рибофлавина для фотометрирования. Результаты испытаний приведены в табл. 4. Расчет содержания рибофлавина (х) в лекарственной форме в граммах проводили по формуле:
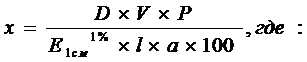
D - оптическая плотность;
![]() -удельный показатель поглощения;
-удельный показатель поглощения;
а - объем лекарственной формы, взятый на анализ;
l - толщина слоя кюветы, см;
V - объем фотометрируемого раствора, мл;
100 - пересчет в граммы. Результаты расчетов приведены в табл. 4.
Таблица 4.
Аналитические данные
количественного определения рибофлавина
№ опыта | Оптическая плотность | Содержание рибофлавина, г |
1 | 0,579 | 0,000988 |
2 | 0,578 | 0,000986 |
3 | 0,579 | 0,000988 |
Статистическая обработка результатов эксперимента
Определение среднего значения (![]() ):
):
![]()
Определение стандартного отклонения (S):
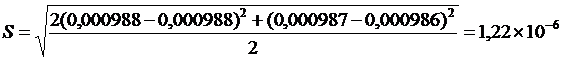
Определение доверительного интервала (![]() ) при доверительной вероятности 95%:
) при доверительной вероятности 95%:
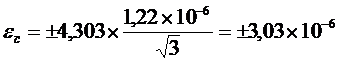
Определение ошибки метода (![]() %):
%):
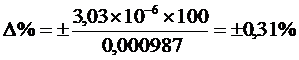
Полученная величина содержания рибофлавина укладывается в допустимые пределы отклонений (согласно инструкции по оценке качества лекарств от 16.10.97 , приказ МЗ РФ № 000), что составляет ± 20% , т. е. 0,008 - 0,012 г. Окончательная формулировка методики анализа приводится в проекте ФСП 42-2-01 в соответствии с ОСТ 91500.001-00.
Разработчик, студент ______ группы
Фамилия, имя, отчество (подпись).
Вопросы, задания, упражнения для самоконтроля.
1. Дайте сравнительную характеристику гравиметрическим, титриметрическим и фотометрическим методам анализа по следующим критериям: чувствительность, достоверность, специфичность.
2. Почему для этинилэстрадиола не предусмотрено количественное определение (ФС 36, ГФ X, с. 74)?
3. Почему фотометрические методы применяются в основном для количественного определения лекарственных форм, а не для лекарственных субстанций?
4. Какие из оптических методов анализа относятся к абсорбционным (по характеру взаимодействия с лучистой энергией):
а) люминисцентный;
б) турбидиметрический;
в) фотоколориметрический;
г) флуориметрический;
д) нефелометрический;
е) спектрофотометрический.
5. Что понимают под оптической плотностью? Зависит ли она от концентрации анализируемого вещества?
6. Что понимают под УФ - спектром вещества?
7. От чего зависит величина удельного показателя поглощения?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



