В предварительно прокаленном и взвешенном тигле или фарфоровой лодочке взвешивают 1-2 г топлива и помещают его в муфельную печь, которая предварительно нагревается до 250-300 °С. Затем температуру печи постепенно повышают до 800 °С в течение 1-2 часов и выдерживают при указанной температуре 1 час. После этого тигель (или фарфоровую лодочку) вынимают из муфельной печи, охлаждают 5 минут на воздухе и переносят в эксикатор, где он охлаждается до комнатной температуры.
После взвешивания тигля зольность рассчитывается по формуле:
Зольность (%) = (М * 100)/m,
где М - масса зольного остатка, г; m - масса топлива, г.
Для проверки правильности определения зольности тигель с зольным остатком можно еще раз. прокалить. Между двумя определениями разница не должна превышать 0,001 г.
Оформление работы: записать методику определения зольности топлива, полученные результаты записать в таблицу.
Таблица 6
Экспериментальные данные определения зольности твердого топлива
№ | Масса | Зольность, % | |
Топлива, г | Золы, г | ||
1 | |||
2 |
3. Определение количества летучих веществ в топливе
В предварительно взвешенном тигле помещают навеску измельченного воздушно-сухого твердого топлива в количестве около 1 г. Тигель закрывают крышкой и помещают в муфельную печь, нагревают до 850 °С. Выдерживают в течение 7 минут. При этом происходит удаление влаги и летучих органических веществ. Затем тигель вынимают и охлаждают, не снимая крышки, сначала на воздухе 5 минут, а затем в эксикаторе до комнатной температуры. Охлажденный тигель взвешивают и количество летучих веществ определяют по формуле:
ЛВ=[(р*100/m)-W],%,
где р - потери топлива в массе после прокаливания, г;
m - навеска топлива, г; W - влага, имеющаяся в навеске угля, %.
Количество влаги вычисляется, исходя из процентного содержания влаги, имевшейся в угле. Следовательно, прежде чем определить количество летучих веществ, нужно определить количество влаги (см. работу «Определение влажности твердого топлива»). Например, для определения количества летучих веществ было взято 1,3468 г угля, после прокаливания масса стала 1,1122 г. Количество влаги было равно 1,2%. Следовательно, в 1,3468 г. топлива влаги будет:
(1,3468 *1,2)/100 = 0,0161 г.
Количество летучих веществ равно:
ЛВ = ((0,2346-0,0161)*100)/1,3468 = 16,2 %.
Тот же результат можно получить непосредственно по формуле:
ЛВ = (100*p/m) -W, %
ЛВ= (0,2346*100/1,3468) -1,2 = 16,2 %.
Оформление работы: кратко описать методику работы и полученные цифровые данные внести в таблицу.
Таблица 7 Экспериментальные данные определения летучих веществ в твердом топливе

ЛАБОРАТОРНАЯ РАБОТА №5
ФЛОТАЦИОННОЕ ОБОГАЩЕНИЕ ЖЕЛЕЗНОЙ СУЛЬФИДНОЙ РУДЫ
Практическая часть
Цель работы: провести флотацию железного колчедана; определить выход концентрата, степень извлечения металла и степень концентрации. Оборудование и материалы
1. Сосуд для флотации - колба или цилиндр на 250 мл с пробкой.
2. Флотореагент - репейное или сосновое масло, ксантогенат или аэросил.
3. Сульфидная руда или искусственно приготовленная смесь сульфида с песком.
4. Металлическая или фарфоровая ступки.
5. Сито с отверстиями 0,1—0,05 мм.
6. Технохимические весы с разновесом.
7. Воронка Бюхнера и колба Бунзена.
8. Вакуумный насос.
9. Сушильный шкаф.
Ход работы
1. Крупные куски руды измельчают, а затем растирают в фарфоровой ступке до тончайшего порошка. Полученный порошок просеивают через мелкое сито. Частицы руды размером 0,1 мм подвергают повторному дроблению.
2. Для флотации берут 2,5-3 г руды. Руду высыпают в цилиндр на 250-300 мл, наливают 100-150 мл воды и добавляют 2 шпателька флотореагента.
3. Цилиндр закрывают пробкой и смесь энергично взбалтывают в течение 0,5-1 мин до тех пор, пока некоторая часть сульфидов не всплывает на поверхность водного слоя. Всплывшую часть сульфидов осторожно сливают в воронку Бюхнера с взвешенным заранее фильтром. Поскольку после первого взбалтывания всплывает только часть сульфидов, операцию флотации повторяют еще 2-3 раза. Необходимый вакуум на воронке Бюхнера создают водоструйным насосом или насосом Комовского.
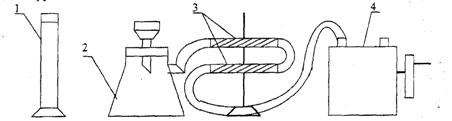
Рис. 3. Схема процесса флотационного обогащения руды
1 - сосуд для флотации;
2 - колба с воронкой для фильтрования;
3 - осушительные колонки с хлористым кальцием;
4 - насос для создания вакуума.
4. Отфильтрованные сульфиды вместе с фильтром высушивают при 80-100 °С, затем взвешивают и проводят необходимые расчеты.
Оформление работы: результаты опыта оформляют в виде таблицы.
Таблица 8 Экспериментальные и расчетные данные процесса флотации сульфидной руды

Примечание. Данные о процентном содержании сульфида в руде, необходимые для расчета, берут у преподавателя. Содержание металла в концентрате определяют расчетным путем, считая что, отфильтрованное вещество является чистым сульфидом.
ЛАБОРАТОРНАЯ РАБОТА №6
ОТКРЫТИЕ В ПОЛИМЕРАХ ФУНКЦИОНАЛЬНЫХ ГРУПП
Практическая часть
Цель работы: открыть функциональные группы, входящие в состав полимера, дать характеристику химического строения полимера. Оборудование и материалы
1. Набор полимеров в виде небольших кусочков.
2. Пробирки (термостойкие) с газоотводными трубками.
3. Пробирки-приемники.
4. Спиртовки.
5. Насыщенный раствор бихромата калия в 10% растворе серной кислоты.'
6. Насыщенный раствор хлорида железа (III).
7. Бромная вода.
8. 30% раствор едкого натра.
9. Раствор хлористоводородного бензолдиазония.
10. 10% раствор нитрата серебра, едкий натр (1:10), раствор аммиака.
11. Фелингова жидкость.
12. Насыщенный раствор хлорной извести. Ход работы
Для термического разложения полимера 8-10 г его помещают в пробирку из тугоплавкого стекла, закрывают пробкой с изогнутой газоотводной трубкой, конец которой помещают в другую пробирку (приемник), содержащую 5 мл воды. Во избежание засасывания воды газоотводную трубку держат у поверхности или погружают ее в воду не более чем на 2-3 мм. Пробирку с полимером сильно нагревают на спиртовке до полного разложения вещества, а уходящие пары улавливают в приемнике. Водный раствор продуктов разложения может содержать анилин, фенол, альдегиды, фурфурол, уксусную кислоту, стирол и метилметакрилат.
Открытие анилина
Для открытия анилина к. 1/7 полученного раствора прибавляют 1 мл бихромата калия в 10% растворе серной кислоты. Появление синей, а затем черной окраски указывает на наличие анилина. В присутствии водного раствора хлорной извести раствор окрашивается при наличии анилина в фиолетовый цвет.
Открытие фенола
Готовят водный раствор продуктов термического распада и в нем открывают обычными реакциями фенол.
1. При наличии фенола в растворе появляется фиолетовая краска при добавлении к нему раствора хлорида железа (III).
2. При добавлении избытка бромной воды выпадает осадок трибромфенола.
3. При добавлении нескольких капель щелочи и хлористоводородного бензолдиазония выпадает желтый осадок оксиазобензола.
Открытие альдегидов. Готовят водный раствор продуктов термического распада, к нему прибавляют аммиачный раствор нитрата серебра и раствор подогревают до 70-80 "С. При наличии альдегидов на стенке пробирки образуется «серебряное зеркало».
Наличие альдегидов можно также открыть с помощью фелинговой жидкости, после приливания которой к водному раствору продуктов термического разложения полимера и нагревания смеси выпадает красный осадок закиси меди.
Часть III. Технология неорганических веществ
ЛАБОРАТОРНАЯ РАБОТА №7
1. КАТАЛИТИЧЕСКОЕ ОКИСЛЕНИЕ S02 В SO3
Теоретическая часть
В производстве серной кислоты контактным, способом окисление диоксида серы по реакции:
S02 + 0,5О2 = S03 + Q (1)
проводится в присутствии катализатора – ванадиевой контактной массы.
Реакция окисления SO2 идет с уменьшением объема и выделением теплоты.
Тепловой эффект реакции Q зависит от температуры. В интервале 400-700 °С тепловой эффект (кДж/моль) с достаточной для практических расчетов точностью может быть вычислен по уравнению:
Q = 101420 – 9,26 Т. (2)
Реакция окисления S02 в S03 обратима. Константа равновесия этой реакции Кр (Па-0,5) равна:
![]() (3)
(3)
где PSO3,PSO2,PO2 – равновесные парциальные давления SO^S02,0% в Па. Константа равновесия зависит от температуры. В интервале 390-650 °С она может быть найдена по уравнению:
lgKp = 4905,5/Т-7,1483. (4)
В таблице 9 приведены значения Кр, вычисленные по этому уравнению.
Таблица 9 Константа равновесия процесса окисления диоксида серы в триоксид серы от температуры
![]()
Степень превращения диоксида серы зависит от состава газа, температуры и давления, продолжительности контакта газа с катализатором, его активности и других факторов.
Для газа заданного состава теоретически возможная, т. е. равновесная степень превращения диоксида серы (степень контактирования) Хр может быть посчитана как отношение:
XP = PSO3/(PSO2 + PO2). (5)
Подставим в это отношение значение PSO3 из уравнения для Кр и поделим

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |




