По полученным данным рассчитывают степень каустификации, а также выход едкого натра в процентах от теоретически возможного. (Примерный расчет степени каустификации приведен ниже).
Методики анализов
Содержание Na2C03 в исходном содовом растворе определяют титрованием. Для этого берут пипеткой 10 см3 анализируемого раствора в коническую колбу, добавляют 40-50 см3 дистиллированной воды и две-три капли метилового-оранжевого индикатора и титруют 1 н раствором соляной кислоты до перехода желтой окраски в розовую. Количество HCI (см3), израсходованное на титрование, эквивалентно количеству и Na2C03.
Фильтрат и промывные воды после отделения СаС03 анализируется на содержание NaOH и Na2C03 методом осаждения карбоната хлористым барием. По этому методу в одной пробе анализируемого раствора определяется общая щелочность (NaOH + Na2C03) титрованием соляной кислотой в присутствии метилового-оранжевого, а в другой пробе после осаждения Na2C03 хлористым барием определяется NaOH титрованием HCI в присутствии фенолфталеина.
Анализ фильтрата после каустификации и отделения шлама выполняют, не промывая шлама. Сначала измеряют объем фильтрата V, затем отбирают пробу 10 см3 фильтрата в коническую колбу, добавляют в колбу 50 см3 воды, две-три капли метилового-оранжевого и титруют 1 н раствором HCI до перехода желтой окраски в розовую. Количество HCI (cmj) Vi, Израсходованное на титрование пробы, эквивалентно общей щелочности. Для определения едкого натра другую пробу фильтрата (10 см3) переносят в коническую колбу, разбавляют водой до 50 см3 и прибавляют избыток хлористого бария (примерно 30 см3 10% раствора ВаС12). При этом образуется нерастворимый карбонат бария и гидроокись бария по реакциям:
Na2CO3 + BaCl2 ↔ 2NaCI + ВаСО3;
2NaOH + BaCI2 ↔ 2NaCI + Ba(OH)2.
При дальнейшем титровании пробы соляной кислотой (не отделяя осадка) определяется количество ионов ОН–, эквивалентное первоначальному содержанию едкого натра в пробе. К пробе после осаждения карбоната добавляют несколько капель фенолфталеина и тотчас же титруют 1 н раствором соляной кислоты. Количество см3 V2, израсходованное на титрование пробы, отвечает содержанию NaOH в пробе.
Анализ промывных вод ведут так же, как и в случае фильтрата, но для титрования применяют 0,1 н раствор HCI. Замеряют объем промывных вод V3, собирая их в мерную колбу, и отбирают две пробы, по 20 см3 каждая, для определения в одной общей щелочности, а в другой NaOH.
Пример расчета показателей каустификации
Пусть на титрование 10 см3 исходного содового раствора израсходовано 20 см 1 н раствора HCI. Фактор HCI (поправка m точно 1 н HCI) составляет в данном случае 0,95. Нормальность исходного раствора Na2C03 составляет:
(0,95 20)/10 = 1,9н.
Концентрация исходного раствора:
СNa2CO3=1,9 53 = 101г/л.
На титрование 10 см3 фильтрата, общий объем которого составляет 300 см, в присутствии метилового-оранжевого израсходовано 25 см3 1 н раствора HCI (m=0,95), а на титрование 10 см того же фильтрата после осаждения Na2C03 раствором ВаС12 - 21 см3 HCI.
CNaOH = (m • V2 • 40)/10 = ((0,95 2l)/10) 40 = 80г/л;
СNa2CO3 =(m(v, - У2)-53)/10 = ((0,95-(25-21))/10)-53 = 20,2г/л.
Во всем объеме полученного после каустификации фильтрата содержится:
(80 300)/1000 = 24г NaOH;
(20,2 • 300)/1000 = 6,08 г Na2C03.
Общая масса влажного осадка 150 г. Навеска осадка для промьдвки 2 г. Объем промывных вод Vi = 200 см3.
На определение общей щелочности промывных вод (проба 20 см3) израсходовано 10 см3 0,1 н раствора HCI. На определение NaOH в промывных водах (20 см3) израсходовано 6 см3 0,1 н HCI.
CNaOH =((0,1-б)/20)-40 = 1,2г/л;
CNa2C03 =((0,1(10-6))/20)-53 = 1,06г/л.
В полученных промывных водах, в пересчете на все количество осадка, содержится:
1,2 (150/2)-(200/1000) = 18г NaOH;
1,06 • (150/2)- (200/1000)= 15,9г Na2C03.
Общее количество NaOH, полученное при каустификации, составляет 24 + 18 = 42 г. Количество оставшейся соды 6,06 + 15,9 = 21,96 г или в пересчете на NaOH - 16,55 г. Степень каустификации фактическая:
X = 42/(42 +16,65) = 71,5 %.
Результаты анализов и расчетов сводят в таблицу.
Таблица 12 Экспериментальные данные процесса каустификации содового раствора
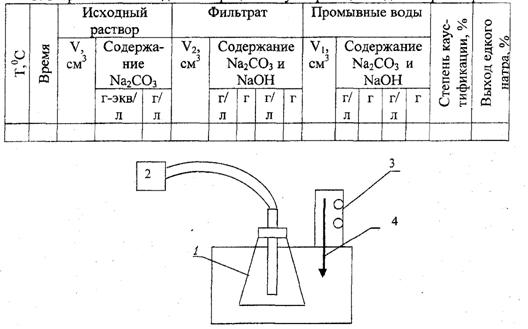
Рис. 6. Схема установки для каустификации содового раствора 1 - колба (стакан)-каустицер, 2 - воздуходувка, 3 - термостат, 4 – термометр
ЛАБОРАТОРНАЯ РАБОТА №9
ПОЛУЧЕНИЕ МЕТАЛЛИЧЕСКОГО ПОКРЫТИЯ ЭЛЕКТРОЛИТИЧЕСКИМ СПОСОБОМ
Практическая часть
Цель работы: получить медное или никелевое покрытие при заданных условиях, рассчитать выход по току и толщину покрытия. Оборудование и материалы
1. Источник постоянного тока (электролизер).
2. Амперметр.
3. Электрохимическая ячейка.
4. Магнитная мешалка.
5. Алюминиевые и медные электроды или стальные и графитовые электроды.
6. Растворы и электролиты для меднения или никелирования.
Ход работы
1. Подготовить 2-3 образца для покрытия металлом и взвесить их.
2. Рассчитать поверхность катода. Площадь пластинок штангенциркулем или, в крайнем случае, линейкой.
3. Рассчитать силу тока по заданной катодной плотности. Подготовка алюминиевых пластин для меднения заключается в проведении обезжиривания в 5% растворе NaOH при нагревании (температура раствора 60-70 °С) и последующего травления в 5% растворе H2S04 при нагревании (температура раствора 80 °С). После каждой операции необходимо образец промыть холодной дистиллированной водой.
Для никелирования наиболее пригодны прямоугольные железные пластины с общей поверхностью в 10-15 см2 с отверстиями. Пластинка предварительно зачищается крупной наждачной шкуркой, а затем - мелкой. При переходе к мелким номерам необходимо полностью сошлифовать царапины, оставшиеся от более крупных номеров шкурок. Для получения ровного блестящего никелевого покрытия пластинку после шлифовки полируют порошком окиси хрома или алюминия, который наносится на сукно, набитое на деревянный брусок. Для обезжиривания пластинку натирают гидратом окиси кальция, нанесенным на щетку. Пасту удаляют дистиллированной водой и щеткой. Пластинку в это время удерживают пинцетом. После обезжиривания пластинку ополаскивают дистиллированной водой, помещают примерно на 1 мин в 5% раствор серной кислоты, снова промывают водой. При кратковременном травлении железа серной кислотой на поверхности появляется кристаллическая структура железа, вследствие чего улучшается контакт никелевого покрытия с железом.
После подготовки образец сушат и взвешивают на аналитических весах. Далее образец закрепляют в установке для электрохимического нанесения металла (см. рис. 7).
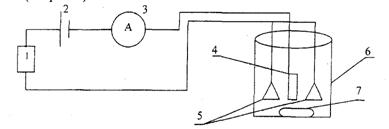
Рис. 7. Схема установки процесса электрохимического нанесения металла: 1 - сопротивление; 2 - источник питания; 3 - амперметр; 4 - катод, (-); 5 - анод, (+); 6 - электролитическая ванна; 7 - якорек (для перемешивания электролита на магнитной мешалке).
Катодная плотность тока при меднении выдерживается в пределах 1,5 -2,0 А/дм2 . Никелирование покрываемой поверхности проводится при плотности тока 0,5-1,0 А/дм2 .
При меднении анодом является медная пластина, катодом - алюминиевая; при никелировании аноды - угольные стержни, катод – стальная пластина. Покрытие образца ведется в течение 40-80 мин при комнатной температуре. По окончании процесса установку отключают, электроды промывают в проточной воде. Образец высушивают при комнатной температуре и взвешивают на аналитических весах.
По разнице массы образца до и после электроосаждения металла находят количество меди (никеля), полученное при электролизе, а затем рассчитывают выход по току по формуле:
η = G100/ItE,
где G - количество металла, действительно полученное при электролизе, г;
I - сила тока, А;
t - продолжительность электролиза, с;
Е - электрохимический эквивалент, г/Кл.
Электрохимический эквивалент вычисляют:
E = M/Fn,
где М - атомная масса металла;
F - число Фарадея;
n - число электронов, принимающих участие в электродной реакции.
Расчет толщины металлического покрытия производится по формуле:
δ = tDKηE/r
DK=I/S,
где S - толщина покрытия, мкм;
DK - катодная плотность тока, А/дм2;
t - время электролиза, с;
р - плотность меди (8,9 г/см3);
S - площадь поверхности, покрытая металлом,.
Оформление работы: по данным опыта и расчетов составляют таблицу.
Таблица 13

Состав электролита для меднения (г/л):
Сульфат меди - 180-250; серная кислота (конц.) - 30-50; соляная кислота (конц.) - 0,009 мл.
Состав электролита для никелирования (г/л):
Сернокислый никель - 150-200; сернокислый натрий - 70; сернокислый магний - 10; борная кислота - 30; хлористый натрий - 5.
Часть IY. Технология органических веществ
ЛАБОРАТОРНАЯ РАБОТА №10
ОКИСЛЕНИЕ ПАРАФИНА И ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
Теоретическая часть
Парафин окисляется при нагревании кислородом до высших спиртов, альдегидов и карбоновых кислот. Соответствующая температура, наличие катализаторов и определенное соотношение между количеством кислорода и паров парафина позволяют проводить реакцию в нужном направлении. Продукты окисления находят разнообразные применения. В частности, кислоты применяются для изготовления мыла, а спирты - синтетических моющих средств.
Практическая часть
Цель работы: получить карбоновые кислоты из парафина и определить их выход.
Оборудование и материалы
1. Колба для окисления парафина.
2. Компрессор (или кислородный баллон).
3. Термометр.
4. Парафин.
5. КМп04
6. 5% раствор едкого натра.
7. 10% раствор соляной кислоты.
8. 0,1 н раствор щелочи.
9. Фенолфталеин.
10. Технические весы.
11. Воронка.
12. Колбы на 250 мл.
13. Фильтры.
Ход работы
В колбу для окисления парафина помещают 10 г парафина и 5 г тонко растертого КМп04 и нагревают до расплавления. При этом происходит энергичное выделение газа и окисление парафина. Нагревание колбы временно прекращают. Внимание! Температура плавления парафина низкая, поэтому он плавится очень быстро. Нельзя отвлекаться от работы и покидать свое рабочее место.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |




