После окончания реакции в колбу опускают стеклянную трубку, соединенную с компрессором (или с кислородным баллоном), пропускают в течение 15-20 минут воздух (или кислород) со скоростью 1-2 пузырька в секунду. Скорость регулируется винтовым зажимом. Парафин в колбе нужно все время нагревать и поддерживать его температуру 100-120 С.
К расплавленым продуктам реакции приливают 10 мл 5% раствора щелочи, нагревают смесь до кипения, охлаждают. Верхний слой застывшего парафина осторожно отодвигают шпателем, а жидкую часть сливают через фильтр в колбу. Далее к полученному раствору солей карбоновых кислот приливают 10 мл 10% раствора, НС1 и смесь нагревают до кипения, а затем охлаждают. Выделившиеся карбоновые кислоты отфильтровывают через бумажный фильтр, который тщательно промывают водой до удаления избытка хлороводородной кислоты. Фильтр с осадком кислот помещают в колбу, приливают 20 мл воды и потенциометрически титруют 0,1 н раствором щелочи со стеклянным электродом.
Оформление работы: описать методику работы, привести уравнения химических реакций, построить кривую титрования, провести расчет количества карбоновых кислот. Расчет с целью упрощения ведут на стеариновую кислоту. Выход карбоновых кислот невелик.
ЛАБОРАТОРНАЯ РАБОТА №11
ПОЛУЧЕНИЕ УКСУСНОЙ КИСЛОТЫ СИНТЕТИЧЕСКИМ СПОСОБОМ
Цель работы: получить раствор уксусной кислоты, исходя из карбида кальция, и рассчитать выход продукта. Оборудование и материалы
1. Колба Вюрца (1) с карбидом кальция.
2. Капельная воронка (2) с насыщенным раствором NaCl.
3. Промывная склянка-счетчик пузырьков с водой (3).
4. Колба (4) с раствором HgS04 с газоотводными трубками.
5. Термометр (5).
6. Стаканчик-приемник (6) с раствором КМп04.
7. Воздуходувка (7).
8. Электроплитка (8).
9. Серная кислота концентрированная.
Примечание: цифры в круглых скобках соответствуют рисунку 8.
Ход работы
Для проведения работы собирают установку, изображенную на рисунке 8.
Ацетилен получают, приливая по каплям к карбиду кальция, количество которого не более 5 г, концентрированный раствор NaCl. О количестве получаемого ацетилена судят по количеству пузырьков в промывной склянке-счетчике пузырьков (3). Ацетилен следует пускать в колбу (4) в небольших количествах, около 1 пузырька в секунду.
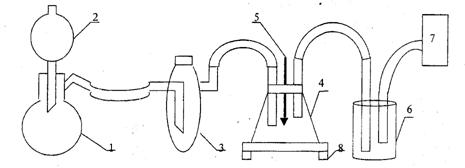
Рис. 8. Схема установки получения уксусной кислоты по реакции Кучерова
Водный раствор HgS04 заранее нагревают до 70 ºС. За температурой следят по показаниям термометра (5) и пропускают ацетилен. Ацетилен поступает в колбу (4) с насыщенным раствором HgS04, где и происходит его гидратация и образование уксусного альдегида. Для предупреждения гидролиза HgS04 в колбу (4) приливают 1-2 мл концентрированной серной кислоты. В отсутствие готового раствора HgS04 его легко можно приготовить растворением окиси ртути в серной кислоте при нагревании. Для этого нужно взять около 1 г окиси ртути и 30 мл серной кислоты, разбавленной 1:4.
Уксусный альдегид, получающийся за счет гидратации ацетилена под влиянием катализирующего действия соли ртути, испаряется и поступает в стаканчик-приемник (6) с разбавленным раствором КМп04, где происходит его окисление до уксусной кислоты.
Пары альдегида перед поступлением в стаканчик-приемник (6) следует смешать с воздухом, который нагнетается воздуходувкой (7).
Опыт продолжают в течение 10 минут до исчезновения окраски КМп04 и образования осадка двуокиси марганца. После этого прекращают ток ацетилена и воздуха и отсоединяют стаканчик-приемник (6) с раствором уксусной кислоты.
Для отделения раствора уксусной кислоты от двуокиси марганца полученный раствор отфильтровывают. Наличие уксусной кислоты определяют по реакции с хлоридом железа (III) или по образованию уксусноэтилового эфира. Для этого к полученному раствору приливают раствор хлорида железа и нагревают. Появляется окраска, напоминающая цвет крепкого чая.
Оформление работы: 1) описать методику получения уксусной кислоты в лабораторных условиях, привести полученные результаты;
2) провести титрование полученной уксусной кислоты 0,01 н раствором гидроксида натрия в присутствии фенолфталеина, рассчитать выход кислоты.
ЛАБОРАТОРНАЯ РАБОТА №12
ПОЛУЧЕНИЕ МЫЛА
Теоретическая часть
Сырьем для получения обычного мыла, используемого в быту при стирке и мытье, служат жиры животного (твердые по консистенции) или растительного (жидкие) происхождения. Жиры представляют собой сложные эфиры глицерина и высших карбоновых кислот. В состав животных жиров входят смеси предельных высших карбоновых кислот (лауриновая С11Н23СООН, пальмитиновая С15Н31СООН, стеариновая С17Н35СООН), а в состав растительных жиров - непредельные (олеиновая С]7НззСООН, гексадеценовая С15Н29СООН, линолевая С17Н29СООН).
Так как в настоящее время основным сырьем для получения мыла являются растительные жиры, их предварительно гидрируют водородом в присутствии катализатора (например, никеля) и получают твердые жиры, называемые саломасом. Получение мыла проводят в несколько стадий.
1. Гидролиз, расщепление жиров водяным паром в автоклавах при температуре 523-573 К и давлении 25*105 и 30*105 Па.
2. Очистка полученных жирных кислот.
3. Омыление кислот гидроксидом натрия или калия (или кальцинированной содой).
Схематично получение мыла можно выразить следующими реакциями:
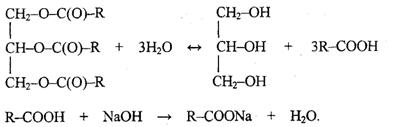
Натриевые или калиевые соли высших жирных кислот представляют собой жировое, обычное мыло. Натриевое мыло - твердое, калиевое - жидкое. Сорт мыла зависит от содержания в нем жирных кислот, которое выражается в процентах. Наша промышленность выпускает 72%, 70% и 60%-ное мыло. В высококачественное хозяйственное и туалетное мыло добавляют красители и отдушки.
Практическая часть
Цель работы: получить мыло из пищевого сырья и определить содержание жирных кислот в образце мыла.
Оборудование и материалы
1.Жир.
2. Гидроксид натрия.
3. Этанол или пропанол.
4. Хлорид натрия (1,16 - 1,18*10 г/см ).
5. Туалетное (или хозяйственное) мыло.
6. Соляная кислота.
7. Фарфоровый стакан на 100-150 мл.
8. Колбы на 100 - 250 мл.
9. Стеклянные палочки.
Ход работы
Проводят гидролиз жиров спиртовым раствором гидроксида натрия. Для этого взвешивают 6 г жира, помещают в фарфоровый стакан и нагревают до расплавления. Готовят раствор гидроксида натрия путем растворения 2,5 г NaOH в 6 мл Н20 и 15 мл этанола или пропанола-1. Спиртовый раствор NaOH приливают при перемешивании к расплавленому жиру. Полученный раствор кипятят в течение 10-15 мин, добавляют к нему 10-15 мл насыщенного раствора хлорида натрия и охлаждают в бане с водой. Образовавшийся на поверхности слой мыла извлекают из стакана, тщательно высушивают фильтровальной бумагой и переносят на предварительно взвешенный фильтр и определяют его массу. Рассчитывают выход мыла на взятый жир.
Определение содержания жирных кислот. Взвешивают 5 г туалетного или хозяйственного мыла, нарезают его тонкими полосками, помещают в другой фарфоровый стакан емкостью 100 мл, приливают 50 мл дистиллированной воды и нагревают на закрытой электроплите до полного растворения мыла. К полученному раствору добавляют 10 мл соляной кислоты (1:1) и продолжают нагревание до образования на поверхности раствора маслянистого слоя (опыт проходит лучше, если в раствор поместить стеклянную палочку). Стакан охлаждают, вынимают палочку и через образовавшееся отверстие сливают жидкость. Оставшиеся в стакане жирные кислоты переносят на предварительно взвешенную фильтровальную бумагу и высушивают. Остатки кислот снимают со стенок стакана пинцетом. Полученные жирные кислоты взвешивают, а затем по первоначальной навеске мыла вычисляют их процентное содержание в образце.
Оформление работы: кратко опишите состав мыла, реакции его получения, методику проведения опыта, рассчитайте выход мыла.
ЛАБОРАТОРНАЯ РАБОТА №13
ПОЛУЧЕНИЕ ФЕНОЛФОРМАЛЬДЕГИДНЫХ СМОЛ
Практическая часть
Цель работы: получить новолачную и резольную смолы и изучить их свойства.
Оборудование и материалы
1. Водяная и масляная бани.
2. Круглодонные колбы.
3. Термометр (100 °С, 120 °С, 160 °С).
4. Воздушный и водяной обратные холодильники.
5. Фарфоровые чашки.
6. Фенол.
7. Соляная кислота (плотность 1,19 г/см3).
8. 40% раствор формальдегида.
Новолачные смолы образуются при небольшом избытке фенола (на 7 моль фенола берется 6 моль формальдегида). В качестве катализатора применяется соляная, а иногда и щавелевая кислота. Строение полимера можно схематически изобразить формулой:
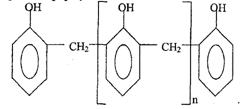
Новолачные смолы термопластичны. Общее количество бензольных колец в макромолекуле составляет 5-10.
Резольные смолы образуются при небольшом избытке формальдегида фенола (на 6 моль фенола берется 7 моль формальдегида). В качестве катализатора применяются основания, например 20-25% раствор аммиака. Резольные смолы отличаются от новолачных смол наличием групп СН2ОН, которые при нагревании участвуют в конденсации и образовании новых мостиков из -СН2 групп. Резольные смолы являются термореактивными.
Ход работы
Техника безопасности
Фенол - яд. Работать с ним нужно под тягой, в резиновых перчатках.
Взвешивать только под тягой.
В круглодонную колбу емкостью 50 мл помещают 7,5 г фенола и 5 мл 40% раствора формальдегида. Смесь взбалтывают до растворения фенола. После этого добавляют 2-3 капли концентрированной соляной кислоты, колбу закрывают пробкой со вставленным в нее обратным холодильником и нагревают на водяной бане при температуре 90-100 °С до разделения водного и смоляного слоев. После отстаивания верхний водяной слой сливают и смолу промывают теплой водой до нейтральной реакции по метилоранжу. Для высушивания смолы чашку помещают на плитку и нагревают до 180-200 °С. Для определения выхода продукта чашку со смолой взвешивают.
Для установления линейного строения полимера 1 г полученного вещества измельчают, помещают в пробирку, приливают 10 мл этилового спирта или ацетона и нагревают. Смесь взбалтывают через каждые 5-10 минут в течение 1-1,5 часа. Смолы, имеющие линейную структуру, растворяются, Для перевода новолачной смолы в полимер, имеющий 3-х-мерное строение, к измельченной смоле добавляют 10-15% (от веса смолы) уротропина и

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |




