числитель и знаменатель на произведение (PSO2 PO2-0,5), получим выражение:
xp=KP/(kp+p02-0,5). (6)
Если выразить начальные содержания S02 и О2; в газовой смеси, поступающей на окисление, через а и b в объемных процентах, то последнее уравнение примет вид:
ХP =Кp/(Кp +((100-0,5aXp)/(b-0,5aXp)P))0,5, (7)
где Р - общее давление газа, Па.
Определение равновесной степени превращения S02 (равновесного выхода S03) по этому уравнению производится методом последовательных приближений. В таблице 9 приведены значения равновесного выхода S03 при атмосферном давлении для газовых смесей различного состава, полученных при сгорании серы в воздухе. Из таблицы видно, что при температуре 400 "С окисление S02 происходит практически нацело. При высоких температурах (около 1000 °С) триоксид серы полностью диссоциирует на диоксид серы и кислорода.
Следовательно, с точки зрения полноты превращения S02 в S03 нужно было бы выбирать возможно более низкую температуру. Однако для обоснования температурного режима окисления следует учитывать и скорость реакции. При 400 °С окисление диоксида серы идет с небольшой скоростью и лишь при применении платинового катализатора. Повышение температуры увеличивает скорость реакции, но при этом уменьшается константа равновесия и, следовательно, выход SO3. Каждой степени окисления соответствует оптимальное значение температуры, при которой скорость реакции максимальна.
Для окисления S02 в SO3 в промышленных условиях применяют ванадиевые контактные массы, отличающиеся составом и способом приготовления. Однако все они содержат V205 в качестве катализатора, пиросульфат щелочного металла [K2S207] в качестве активатора и носитель, состоящий из алюмосиликатов, аморфной кремниевой кислоты и других примесей.
Для изучения влияния различных факторов на скорость окисления S02 и сравнения активности катализатора при различных температурах подсчитывают константу скорости реакции по уравнению Борескова-Иванова.
Для температуры выше 400 °С константа скорости реакции может быть найдена по уравнению Аррениуса:
Kc=K0e-E'RT, (10)
где К0 - коэффициент, характерный для катализатора и не зависящий от температуры;
Е - энергия активации, Дж/моль;
R - газовая постоянная, равная 8,31 Дж/(моль*К);
Т - температура, СК.
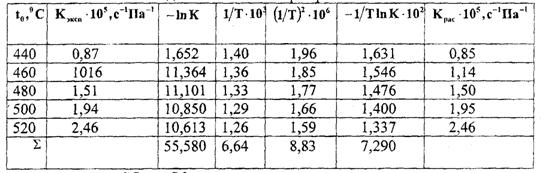
Для расчета константы скорости окисления S02 на ванадиевом катализаторе в интервале 440-550 °С можно принять Е = 59900 Дж/моль и К0 =0,222 (см. таблицу 10).
Таблица 10 Значения константы скорости реакции окисления S02 на гранулированном ванадиевом катализаторе при 440-520 °С
Окисление S02 до S03 осуществляется в контактных аппаратах, имеющих 4-5 слоев контактной массы. Для достижения высокой степени окисления S02 по мере хода реакции приходится отводить выделяющуюся теплоту.
В зависимости от метода отвода теплоты все известные аппараты можно разделить на две основные группы:
- аппараты с промежуточным теплообменом, в которых реакция окисления и теплообмен производятся раздельно, т. е. реакция в слоях катализатора протекает в адиабатических условиях, а теплота отводится между слоями;
– аппараты с непрерывным теплообменом, в которых отвод теплоты осуществляется одновременно с протеканием реакции; теплообмен происходит через теплообменную поверхность в слое катализатора.
При использовании принципа непрерывного теплообмена процесс окисления SO2 удается приблизить к оптимальным условиям и уменьшить расход катализатора. Однако конструкция таких аппаратов значительно сложнее, чем аппаратов с промежуточным теплообменом, затруднен их ремонт и особенно замена контактной массы.
Аппараты с непрерывным теплообменом имеют некоторую перспективу для применения при переработке сернистого газа повышенной концентрации (12-18% S02).
В настоящее время применяются почти исключительно контактные аппараты с промежуточным теплообменом.
Практическая часть
Цель работы: практическое изучение влияния условий окисления S02 кислородом воздуха.
Оборудование и материалы
1. Полиэтиленовый контейнер.
2. Капельная воронка.
3. Круглодонная колба.
4. Склянки Дрекселя.
5. Ротаметр.
6. Реометр.
7. Водоструйный насос.
8. Склянки-поглотители.
9. Печь.
10. Кварцевый реактор с катализатором.
11. Резиновые шланги.
12. Зажимы.
Получение диоксида серы разложением сульфита натрия серной кислотой (рис. 4)
Сульфит натрия в растворе разлагается концентрированной серной кислотой:
Na2S03 + H2S04 → Na2S04 + S02 +6H20.
Выделяющийся газ сушат и собирают в полиэтиленовый контейнер (4).
Реактивы: сульфит натрия безводный, (чистый для анализа); серная кислота, (химически чистая), концентрированная, d42o = 1,84 г/см3.
Получение. Готовят раствор сульфита натрия в дистиллированной воде из расчета 35 г сульфита натрия в 60 г воды и выливают приготовленный раствор в колбу (1). В капельную воронку (2) вводят концентрированную серную кислоту и постепенно прибавляют ее к раствору в колбе. Диоксид серы выделяется равномерным потоком и после промывки раствором серной кислоты, залитым в дрексель (3) (для поглощения S03 и высушивания), собирается в полиэтиленовый контейнер (4).
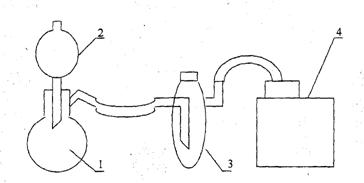
Рис. 4. Схема установки получения диоксида серы
Окисление диоксида серы (рис. 5)
1. Подсоединяют контейнер (1) с S02 к системе. Заливают в поглотительные склянки (И) и (12) одинаковое, рассчитанное количество титрованного раствора йода.
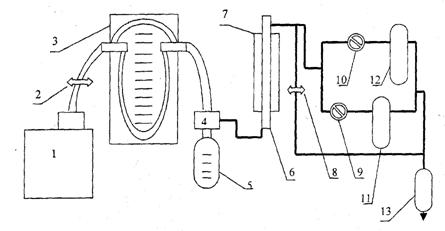
Рис. 5. Схема установки окисления S02 в S03
2. При закрытых зажиме (2), кранах (9), (10) и открытом кране (8) включают водоструйный насос (13).
3. Открыв зажим (2), устанавливают с помощью калиброванного реометра (3) расход S02 и с помощью вентиля ротаметра (5) устанавливают заданный преподавателем поток воздуха. Открывают кран (9), закрыв соответственно (8), пропускают через склянку-поглотиполученную газовую смесь (S02 + воздух из атмосферы). Раствор йода, находящийся в склянке-поглоти, должен обесцветиться, зафиксируем время, пошед
4. Закрывают кран (9), открывают кран (8). Подают напряжение на питающую обмотку печи (7), нагревая её.
5. После достижения заданной температуры 500 °С в печи (7) через 5-7 мин закрывают кран (8), открывают кран (10) и пропускают газовую смесь через ванадиевый катализатор ИК-1-6, который находится в реакторе (6). Далее газовая смесь попадает в склянку-поглотии обесцвечивает раствор иода. Время, пошедшее на обесцвечивание, фиксируется.
Концентрация газа до контактирования определяется расчетным способом, исходя из известных объемов S02 и воздуха, поданных на смешение.
Воздух для окисления S02 в S03 забирается из атмосферы за счет разряжения, создаваемого водоструйным насосом (13), поступает в смеситель (4). Сюда же приходит S02 из полиэтиленового контейнера (1). Расход воздуха и диоксида серы измеряется с помощью ротаметра (5) и реометра (3), соответственно.
Газовая смесь после смесипоступает в первую склянку-поглотис титрованным раствором йода для фиксирования времени восстановления иода диоксидом серы до окисления S02 на катализаторе. В средней части реактора (6) с внутренним диаметром 20 мм, помещенного в печь (7), расположено 20 см3 ванадиевого катализатора ИК-1-6. Нижняя часть реактора загружена фарфоровыми кольцами, на которые уложен катализатор. Температуру в зоне реакции устанавливают 500 °С. Содержание диоксида серы после окисления при контактировании с катализатором определяют путем поглощения S02 титрованным раствором йода в склянке (12).
Оформление работы
1. Определение степени контактирования. Введем обозначения:
с - объем S02 (приведенный к нормальным условиям), поступающий на
окисление за время 1 с;
с, - объем S02, поступающий через поглотительную склянку (12) за 1 с;
х - степень контактирования, доли единицы.
Учитывая, что C1 = с* (1-х) и
C1 = (VP * 10-4 * 32 * 22,4)/(t * 64), где Vp - объем 0,1 н раствора йода, залитого в склянку (12), мл, t - время, ушедшее на обесцвечивание раствора, с, найдем степень контактирования:
х = 1 – c1/c.
2. Составление материального баланса процесса окисления диоксида серы.
Количество азота до и после реакции не изменяется и равно 0.79 VB03, где VB03 - расход воздуха (приведенный к нормальным условиям), л/ч.
Количество S02 после реакции равно VS02(l-x), где VSO2 - расход S02
(при нормальных условиях), л/ч.
Количество S03 после реакции равно – VSO2 х, л/ч.
Количество кислорода после реакции - 0,21 Vвоз – 0,5 x VSO2.
Результаты расчета сводят в таблицу 11.
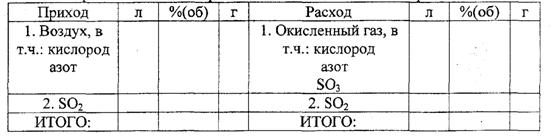
Таблица 11
Материальный баланс процесса окисления диоксида серы
ЛАБОРАТОРНАЯ РАБОТА №8
КАУСТИФИКАЦИЯ СОДОВОГО РАСТВОРА
Практическая часть
Цель работы: провести каустификацию содового раствора заданной концентрации, определить степень каустификации и выход гидроксида натрия от теоретически возможного.
Оборудование и материалы
1. Технохимические весы.
2. Термостат.
3. Стакан-каустицер.
4. Бюретки.
5. Пипетки.
6. Колбы.
7. Мерный цилиндр.
8. Компрессор.
9. Часы.
10. Термометр.
Ход работы
Для проведения опыта готовят исходный содовый раствор, концентрация которого должна составлять 5 (8,11,14,17) вес. % (задается преподавателем). Концентрация исходного раствора проверяется и точно устанавливается аналитически, путем титрования (см. ниже «методика анализов»).
В стакан-каустицер (1) емкостью 1000 см3 заливают 300-500 см исходного содового раствора и ставят его в термостат, перемешивание осуществляют, барботируя через раствор воздух. Нагревают до заданной температуры. Далее небольшими порциями добавляют к содовому раствору тонко измельченную известь, количество извести берется с избытком 5-10% от теоретического количества СаО, рассчитанного по реакции. Вместо извести можно применять известковое молоко, полученное гашением извести, концентрация известкового молока должна быть около 330 г/л Са(ОН)2. После прибавления к содовому раствору рассчитанного количества извести отмечают время начала опыта. Каустификацию ведут в зависимости от задания, в течение 30-90 мин. Температура каустификации задается в пределах 50-90 °С. Во время опыта 2-3 раза проверяют температуру раствора в каустицере, опуская туда термометр (2). Дня определения степени каустификации, взвесив фильтр, отфильтровывают шлам, предварительно остудив раствор в каустицере, промывают осадок и определяют содержание NaOH и Na2C03 отдельно в фильтрате и в промывных водах (см. ниже «методика анализов»). Поскольку осадок очень трудно отмывается от NaOH, то отфильтровывают весь шлам и дают стечь полностью фильтрату, затем измеряют объем фильтрата и определяют в нем содержание NaOH и Na2C03. Весь влажный осадок взвешивают на технических весах, затем берут навеску 1-2 г влажного осадка,' помещают на фильтр и промывают водой до получения 200-300 см3 промывных вод. Измеряют объем полученных вод и определяют в них содержание NaOH и Na2C03, пересчитывая далее их количество на массу всего осадка.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |




