Люминесцентный иммунный анализ (ЛИА)
Данный тип анализа развивается с 70-х годов, в то время была показана потенциальная возможность применения люминесценции для определения концентрации антител и антигенов. На сегодняшний день к ЛИА относят методы, в основу которых положено использование явлении люминесценции для выявления продуктов взаимодействия антиген-антитело. При этом в качестве метки может выступать любой из компонентов хеми - или биолюминесцентной реакции (ферменты, кофакторы, субстраты и т. д.).
Реакцию люминесценции следует отнести к окислительно-восстановительному типу, в ходе которой формируются нестабильные короткоживущие молекулы, находящиеся в электронно-возбужденном состоянии. В случае перехода таких соединений в основное состояние происходит испускание света с определенной длинной волны, который успешно может быть зарегистрирован при использовании фотоумножителей, приемников, а также других устройств.
Общая схема данного процесса может быть представлена с следующем виде:
АГ + АТ-Люминофор = АГ-АТ-Люминофор + hν
В качестве основного преимущества ЛИА следует отметить высокую чувствительность данного метода.
Явления, на которых основан люминисцентный анализ, можно классифицировать на хемолюминесценцию и биолюминесценцию.
Биолюминесцентный иммуноанализ по своей сути представляет из себя разновидность ИФА, поскольку использует ферментативную реакцию и включает: фермент (люциферазы бактерий или светляков), кофакторы (NAD или АТФ), субстрат (люциферин).На основании вышесказанного, возможна следующая классификация ИА: люминесцентный иммунокофакторный анализ (ЛИКА), где кофакторы (АТФ, NAD) используются в качестве метки;
люминесцентный иммуноферментный анализ (ЛИФА), где используются ферменты люциферазы либо ферменты генерирующие кофакторы (глюкозо-6-фосфат дегидрогеназа, пируваткиназа).
Характеризуя методы биолюминесцентного анализа следует отметить высокую чувствительность (до 0,5 нМ антигена) а также перспективность для конструирования высокоэффективных гомогенных и гетерогенных методов ИА (в т. ч. модификации с использованием твердой фазы). Несомненным недостатком такого анализа является высокая стоимость ферментов люцифераз, а также наличие примесей кофакторов в исследуемых биологических материалах.
Хемолюминесцентный иммуноанализ также требует присутствия в системе фермента-катализатора, субстрата и окислителя. В конечном счете, хемолюминесцентный иммуноанализ разделяют на хемолюминесцентный иммуноферментный анализ (ХИФА), хемолюминесцентный субстратный анализ (ХИСА) и хемолюминесцентный иммуноанализ с использованием переноса энергии. В первом случае меткой является фермент, катализирующий окислительно восстановительную реакцию (к примеру, микропероксидаза (фрагмент цитохрома С), пероксидаза). В практике среди данных методов широкое использование получил ХИФА с пероксидазой в качестве метки и двумя субстратами (люциферин+люминол).
Хемолюминесцентный субстратный анализ (ХИСА). Метка, вводимая в иммуноглобулин (антиген) представляет собой молекулу субстрата (эфиры акридина, изолюминол).
Хемолюминесцентный иммуноанализ с использованием переноса энергии (ЭХИА) основан на вышеописанном твердофазном иммуноанализе («сэндвич-метод») с использованием электрохемолюминесцентной метки. В качестве твердой фазы используются магнитные микробусы, с сорбированными на поверхности моноклональными антителами к анализируемому антигену, и коньюгатов иммуноглобулинов, где в качестве метки используется с хелат рутения. Анализ проводится по принципу метода иммуномагнитной сепарации, о котором будет сказано в дальнейших разделах. Инкубационная смесь содержит клинический материал, содержащий анализируемый антиген, магнитные микробусы, с иммобилизованными антителами против искомого антигена, детектирующие вторые антителами, содержащие вышеописанную метку. Отделение иммунных комплексов происходит в специальной камере, где осуществляется выделение микробус с использованием магнитного поля, после чего следует измерение люминесценции. Детектор состоит из фотометра и электрода с магнитом. После захвата микробус со связавшимися иммунными комплексами и меткой на электрод подается напряжение (1,5 В), под действием которого происходит быстрый обмен электронами между атомами рутения и субстратом (трипропиламином). Это сопровождается люминисценцией метки, которая может быть измерена фотометрически. Такие измерения можно проводить неоднократно, так как испускание фотона сопровождается регенерацией метки.
Элиспот.
Элиспот – метод анализа клеток, которые секретируют интересующие продукты (антитела, цитокины, медиаторы и т. д.). В основу данного метода положена технология тИФА по схеме «сэндвича», вместе с тем, анализируемый продукт, который выделяется клетками, фиксируется и анализируется на месте секреции. Таким способом удается измерять небольшие количества вещества до его разведения в инкубационной среде, снижается воздействие со стороны протеаз, снижается вероятность потребления клетками, связывание с соответствующими мембранными или цитоплазматическими рецепторами. После промывки культуры фиксированный продукт проявляется с помощью меченных ферментом вторых моноклональных антител к другой антигенной детерминанте анализируемого продукта. После преобразования экзогенно добавленного субстрата в местах секреции анализируемого продукта появляется соответствующее окрашивание (одна искомая клетка-продуцент соответствует одному пятну). Количество либо процент искомых клеток-продуцентов является результатом такого анализа (рисунок 21).
Элиспот применяется для установления секреции антител, цитокинов, биологически активных веществ и медиаторов воспаления для анализа физиологического состояния клеток иммунной системы (функция клеток-регуляторов, поляризация иммунного ответа Th1-Th2-Th3, цитокиновый профиль), продукции общих и специфических иммуноглобулинов различных классов, для диагностики, и учета динамики при терапии аутоиммунных заболеваний, аллергии, иммунного ответа при трансплантациях, противоопухолевого иммунного ответа и т. д. Однако, из-за относительной дороговизны и сложности таких тест-систем данный метод не нашел широкого применения к настоящему времени.
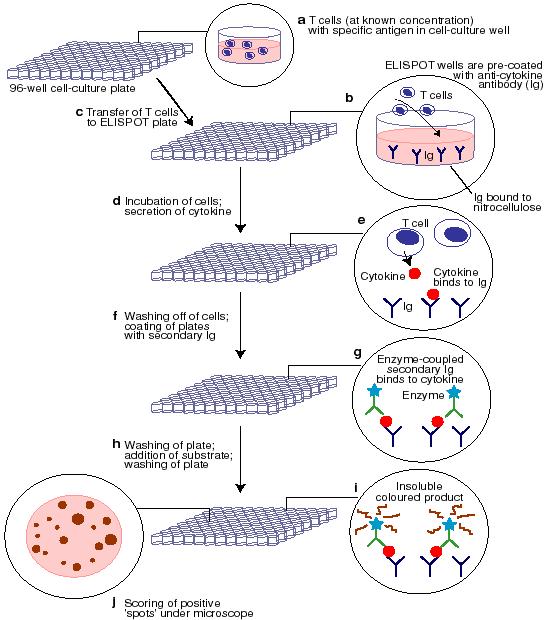
Рисунок 21 - Основные стадии анализа клеток методом элиспот на примере цитокинов, секретируемых Т клетоками.
Иммуноблот (вестернблот)
Иммуноблот – метод анализа, с помощью которого одновременно выявляют специфические иммуноглобулины к набору антигенов в плазме или другом биологическом материале. Данный метод основан натехнологии тИФА, однако в отличие от последнего является менее чувствительным, но обладает большей специфичностью.
Этапы постановки данного анализа приведены на рисунке.
Подготовительный этап обработки антигенов заключается в разрушении инфекционных частиц и обработке (SDS) додецил сульфатом натрия для преобразования всех компонентов к схожему соотношению заряд/молекулярная масса.
Получение блотов:
1. Электрофорез обработанных антигенов (пропорционально размеру).
2. Перенос разогнанных антигенов на целлюлозную мембрану.
3. Разделение мембраны на полоски, содержащие весь спектр исследуемых антигенов.
4. Обработка блота биологическим материалом больного (специфические иммуноглобулины больного взаимодействуют с соответствующими антигенами). Обработка антител антивидовыми иммуноглобулинами к антителам человека, коньюгированными с ферментом;
5. Обработка субстратом и визуализация блотов (при преобразовании субстрата в продукт в месте образования иммунного комплекса образуется пятно). Анализ результата со сравнением с положительным и отрицательным контролями.
Данный метод анализа может использоваться для решение ряда научных и прикладных задач.

Рисунок 22 - Схема проведения анализа методом иммуноблоттинга
Иммуногистохимические и иммуноцитохимические методы исследования
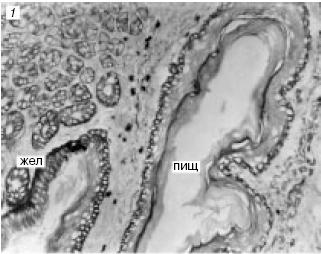
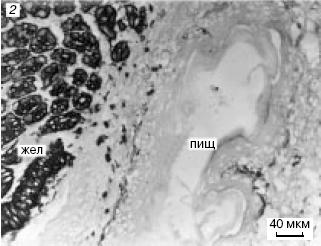
Данный комплекс методов позволяет определять заданные антигены в составе естественного тканевого или клеточного микроокружения. Такие методы основаны на технологии сходной с тИФА, и реализуютя in situ, т. е. на срезах тканей или цитопрепаратах. Формирующийся продукт нерастворим и локализуется окрашенными пятнами в месте синтеза антигена, что может быть зафиксировано с помощью световой микроскопии.
Постановка данного метода заключается в заборе материала, приготовлении соответствующих препаратов, фиксацию, обработке антигенов, окрашивании препарата любыми вышеописанными методами.
Помимо исследования опухолевых клеток, иммуногистохимия находит применение для определения аутоиммунной патологии, некоторых заболеваний, вызванных инфекционным началом, фенотипирования клеток и многих других научных целей.
|
|
Рисунок 23 - Примеры использования иммуногистохимии для определения различных типов клеток. Последовательные срезы через желудок (жел) и пищевод (пищ) мыши, окрашенные двумя моноклональными антителами: 1 - первое моноклональное антитело реагирует с эпителием пищевода и слабее с эпителием желудка; 2- второе моноклональное антитело реагирует только с эпителием желудка.
Иммунохроматографический анализ
Иммунохроматографический метод анализа основан на принципе тонкослойной хроматографии и основан на реакции между
антителом и соответствующем ему антигеном в биологических материалах. В данном методе используются специальные тест полоски, тест кассеты или панели.
Принцип действия данного метода анализа основан на том, что при опускании тест полоски в биологическую жидкость, под действием капиллярных сил раствор начинает перемещаться вдоль полоски, на таком же принципе работает метод тонкослойной хроматографии. Вместе с жидкостью перемещаются нанесенные на нижнюю поверхность тест-полоски коньюгаты специфических моноклональных антител, которые способны аффинно взаимодействовать с анализируемым антигеном.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 |