2) ![]()
3) ![]()
4) ![]()
5) ![]()
48. Дана реакция 2CO + O2 = 2CO2. Выберите правильную формулу для расчета изменения энтропии при реакции, идущей в стандартных условиях:
1) ![]()
2) ![]()
3) ![]()
4) ![]()
5) ![]()
49. Дана реакция N2 + 3H2 = 2NH3. Выберите правильную формулу для расчета энтропии при реакции, идущей в стандартных условиях.
1) ![]()
2) ![]()
3) ![]()
4) ![]()
5) ![]()
50. Из приведенных ниже формул выберите ту, которая справедлива только для идеального газа:
1) ![]()
2) ![]()
3) H = U + pV
4) ![]()
5) ![]()
51. Может ли энергия Гельмгольца вещества быть отрицательной?
1) да
2) только при низких температурах
3) только при высоких температурах
4) только для простых веществ, взятых в наиболее устойчивом состоянии
5) нет
52. Для каких процессов верна формула ∆A = ∆U - T∆S?
1) для любых
2) для обратимых
3) для изобарных
4) для изотермических
5) для изохорных
53. Может ли энергия Гиббса вещества быть отрицательной?
1) да
2) только при низких температурах
3) только при высоких температурах
4) только для простых веществ, взятых в наиболее устойчивом состоянии
5) нет
54. Выберите из приведенных ниже формул ту, которая дает изменение энтропии вещества при изобарном нагревании вещества:
1) ![]()
2) ![]()
3) ![]()
4) ![]()
5) ни одна из формул не годится
55. Энтропия 1 моля какого из приведенных ниже веществ при p = 1 атм имеет наибольшее значение?
1) вода при 0оС
2) водяной пар при 0оС
3) водяной пар при 50оС
4) лед при 0оС
5) вода при 50оС
56. Укажите правильное утверждение: «Обратимым является такой процесс, при котором…»
1) в любой момент времени система бесконечно близка к состоянию равновесия
2) температура окружающей среды практически не меняется
3) не меняется внутренняя энергия системы
4) давление в системе положительно
5) вся поглощенная системой теплота превращается в работу
57. Что такое изолированная система?
1) система, в которой при любых процессах постоянно количество вещества, внутренняя энергия и объем
2) система, в которой при любых процессах постоянно количество вещества
3) система, которая не обменивается теплом с окружающей средой
4) система, в которой при любых процессах постоянно количество вещества и внутренняя энергия
5) система, которая адиабатно изолирована от окружающей среды
58. Как ведет себя энергия Гельмгольца вещества при его расширении при постоянной температуре?
1) всегда убывает
2) всегда возрастает
3) не меняется
4) ответ зависит от типа процесса
5) меняется немонотонно
59. Как ведет себя энергия Гельмгольца вещества при его сжатии при постоянной температуре?
1) всегда убывает
2) всегда возрастает
3) не меняется
4) ответ зависит от типа процесса
5) меняется немонотонно
60. Зависимость теплового эффект химической реакции при постоянном давлении от температуры выражается уравнением Кирхгофа:
1) ![]()
2) 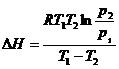
3) 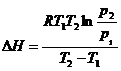
4) 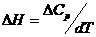
5) 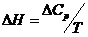
61. Энтальпия и внутренняя энергия находятся в соотношении:
1) ![]()
2) ![]()
3) 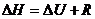
4) 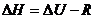
5) ![]()
62. Математическое выражение II закона термодинамики:
1) 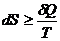
2) 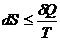
3) 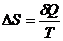
4) 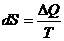
5) 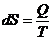
63. Термодинамическая вероятность (W) и энтропия (S) связаны уравнением:
1) ![]()
2) 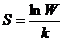
3) 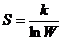
4) 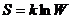
5) 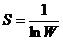
64. Фазовый переход осуществляется при
1) T = const
2) р = const
3) V = const
4) р, T = const
5) p, V = const
65. Термодинамическим потенциалом называется такая термодинамическая функция, убыль которой равна … обратимого процесса.
1) работе
2) внутренней работе
3) максимальной работе
4) полезной работе
5) теплоте
66. Самопроизвольное смешение газов при V, T = const происходит, если:
1) ![]()
2) ![]()
3) 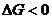
4) 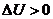
5) 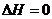
67. Самопроизвольными не являются процессы:
1) распрямление сжатой пружины
2) ржавление железа
3) зарядка аккумулятора
4) переход теплоты от горячего тела к холодному
5) смачивание водой кварцевой поверхности
68. Изменение функции состояния … от способа реализации процесса.
1) зависит
2) увеличивается
3) не зависит
4) уменьшается
5) зависит при p=const
69. В изолированной системе в самопроизвольном процессе энтропия
1) убывает
2) возрастает
3) не изменяется
4) сначала возрастает, затем убывает
5) сначала убывает, затем возрастает
70. Энтропия правильно образованного кристалла при приближении температуры к абсолютному нулю стремится к …
1) нулю
2) ![]()
3) ![]()
4) к максимальному значению
5) к минимальному значению
71. Стандартная теплота образования этилового спирта (С2Н5ОН) при Т = 298 К – это тепловой эффект реакции:
1) 2С + 1/2О2 + 3Н2 = С2Н5ОН(ж) + DН3
2) СН3СНО(г) + Н2 = С2Н5ОН(ж) + DН1
3) С2Н4 + Н2О = С2Н5ОН(ж) + DН2
4) 4С + О2 + 6Н2 = 2С2Н5ОН(ж) + DН4
5) C2H6 + O2 = C2H5OH + H2O + ∆H5
72. Стандартная теплота сгорания сахарозы равна -5646,73 кДж/моль. Это тепловой эффект реакции:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |




