68. Что такое ингибитор?
1) катализатор цепной реакции
2) вещество, добавление которого приводит к увеличению длины цепи
3) вещество, добавление которого приводит к уменьшению длины цепи
4) вещество, добавление которого приводит к возникновению активных центров
5) вещество, ускоряющее скорость цепной реакции
69. Основной закон химической кинетики:
1) скорость реакции в каждый момент времени пропорциональна концентрациям реагирующих веществ, возведенных в некоторые (целые или дробные) степени
2) скорость любой сложной реакции, состоящей из ряда последовательных стадий, определяется скоростью самой медленной стадии
3) скорость реакции пропорциональна концентрациям реагирующих веществ, возведенных в степени, равные стехиометрическим коэффициентам.
4) скорость химической реакции определяется изменением числа реагирующих молекул в единицу времени в единице объема
5) скорость сложной реакции пропорциональна концентрациям реагирующих веществ, возведенных в степени, равные стехиометрическим коэффициентам.
70. В каких координатах следует спрямлять зависимость СA=f(T), чтобы убедиться, что реакция аА+bB→cC имеет 0-й порядок, если исходные вещества А и В были взяты в стехиометрическом соотношении?
1) x=t, y=CA
2) x=t, y=1/CA
3) x=t, y=lnCA
4) x=lnT, y=lnCA
5) x=t, y=1/C2A
71. Как связаны энергии активации прямой и обратной реакции (соответственно Е1 и Е2) с тепловым эффектом реакции?
1) ΔH=E1+E2
2) ΔH=E2-E1
3) ΔH=E1-E2
4) ΔH=E1/E2
5) ΔH=E1*E2
72. Укажите правильную форму записи уравнения Аррениуса?
1) 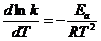
2) 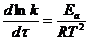
3) 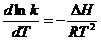
4) 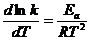
5) 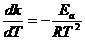
73. Реакция аА+bB→cC имеет первые порядки по А и В. В каком случае верна формула ![]() ?
?
1) никогда
2) если исходные вещества взяты в стехиометрическом соотношении
3) всегда
4) если вещество А взято в избытке
5) если вещество В взято в избытке
74. Укажите размерность скорости реакции, порядок которой равен n=1?
1) 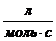 2)
2) ![]() 3)
3) 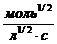 4)
4) ![]() 5)
5) ![]()
75. Порядок реакции равен …… частных порядков
1) разности
2) произведению
3) сумме
4) отношению
5) порядок реакции не зависит от частных порядков
76. При каких условиях кинетику химической реакции A+2B→C можно описать кинетическим уравнением типа ![]() ?
?
1) вдали от состояния равновесия
2) всегда
3) никогда
4) при высоких температурах
5) вблизи состояния равновесия
77. Укажите размерность константы скорости реакции, порядок которой равен n=2?
1) 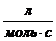 2)
2) ![]() 3)
3) 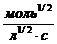 4)
4) ![]() 5)
5) ![]()
78. В каких координатах следует спрямлять зависимость СA=f(T), чтобы убедиться, что реакция аА+bB→cC имеет 2-й порядок, если исходные вещества А и В были взяты в стехиометрическом соотношении?
1) x=t, y=CA
2) x=t, y=1/CA
3) x=t, y=lnCA
4) x=lnT, y=lnCA
5) x=t, y=1/C2A
79. В каком случае порядок реакции по данному веществу совпадает со стехиометрическим коэффициентом, стоящим перед этим веществом в уравнении реакции?
1) Если система далека от состояния равновесия
2) Никогда
3) В случае обратимых реакций
4) Всегда
5) Если рассматриваемая реакция является элементарной
80. Константа скорости реакции не зависит от
1) температуры
2) природы реагирующих веществ
3) присутствия катализатора
4) природы растворителя, в котором ведется реакция
5) концентрации реагирующих веществ
Вопросы 6-го семестра:
1. Средняя ионная активность электролита ![]() – это … из активностей катиона и аниона.
– это … из активностей катиона и аниона.
1) среднее
2) среднее арифметическое
3) средневзвешенное
4) среднее геометрическое
5) среднее логарифмическое
2. Средний ионный коэффициент активности электролита ![]() - это … из коэффициентов активности катиона и аниона.
- это … из коэффициентов активности катиона и аниона.
1) среднее
2) среднее арифметическое
3) средневзвешенное
4) среднее геометрическое
5) среднее логарифмическое
3. Коэффициент активности иона в разбавленном растворе зависит от …
1) природы других ионов
2) температуры
3) ионной силы
4) концентрации электролита
5) плотности растворителя
4. Потенциал электрода, на котором протекает реакция ![]() , определяется по формуле:
, определяется по формуле:
1) 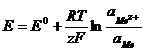
2) 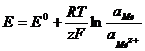
3) 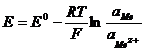
4) ![]()
5) ![]()
5. В гальваническом элементе ![]() протекает реакция:
протекает реакция:
1) ![]()
2) ![]()
3) ![]()
4) ![]()
5) ![]()
6. ЭДС гальванического элемента с электродами, потенциалы клторых равны Е+ = 0,2 В и Е– = –0,4 В равна…
1) 0,2 В
2) 0,3 В
3) 0,4 В
4) 0,6 В
5) 0,1 В
7. При работе в обратимых условиях в гальваническом элементе выделяется тепло. С увеличением температуры ЭДС …
1) возрастает
2) убывает
3) постоянная
4) однозначного ответа нет
5) не изменяется
8. Степень диссоциации электролита зависит от … электролита
1) вязкости
2) природы
3) плотности
4) диэлектрической проницаемости
5) температуры
9. Степень диссоциации слабого электролита в водном растворе с концентрацией 1 моль/дм 3 и Т = 25 ºС равна 0,1, а константа – …
1) 0,01
2) 0,1
3) 1
4) 0,02
5) 0,2
10. Фосфорная кислота диссоциирует по трем ступеням:
![]()
![]()
![]()
Константа диссоциации этого электролита равна
1) 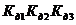
2) ![]()
3) ![]()
4) ![]()
5) Kд2
11. Электрическая проводимость растворов электролитов может быть:
1) расчетной
2) моляльной
3) абсолютной
4) удельной
5) средней
12. Удельная [См·м-1] и молярная [См·м2моль-1] электрические проводимости связаны соотношением:
1) ![]()
2) ![]()
3) ![]()
4) ![]()
5) ![]()
13. В гальваническом элементе на положительном электроде протекает реакция …
1) окисления
2) диспропорционирования
3) восстановления
4) перезарядки
5) ионного обмена

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |




