4)
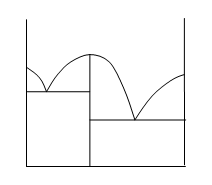

5)
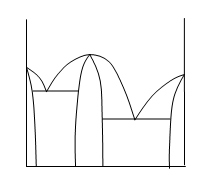

39. Что происходит на участке V кривой охлаждения для сплава 1 (Рис.)?
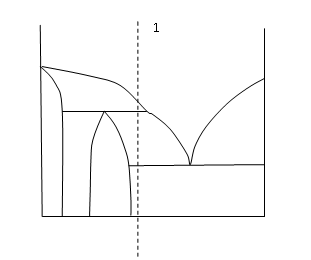



1) перитектическая реакция
2) из жидкости выделяются кристаллы твердого раствора
3) эвтектическая реакция
4) на этом участке не происходит фазовых превращений
5) полная кристаллизация жидкости
40. Сколько фаз находится в равновесии в указанной на диаграмме точке (Рис.)?


1) 0
2) 1
3) 2
4) 3
5) 4
41. Укажите правильную запись уравнения Клаузиуса-Клапейрона:
1) ![]()
2) ![]()
3) ![]()
4) ![]()
5) ![]()
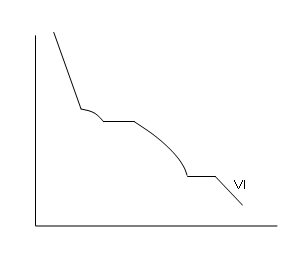
42. Что происходит на участке VI кривой охлаждения для сплава 1 (Рис.)?



1) эвтектическая реакция
2) перитектическая реакция
3) на этом участке не происходит фазовых превращений
4) из жидкости выделяются кристаллы твердого раствора
5) полная кристаллизация жидкости
43. Чему равно максимальное число фаз, которые могут одновременно находиться в равновесии в трехкомпонентной системе при фиксированной величине давления и температуры?
1) 1
2) 2
3) 3
4) 4
5) 5
44. Термодинамическая система, состоящая из различных по физическим или химическим свойствам частей, отделенных друг от друга поверхностями раздела – это…
1) открытая система
2) закрытая система
3) изолированная система
4) гетерогенная система
5) гомогенная система
45. Часть гетерогенной системы, ограниченная поверхностью раздела и характеризующаяся одинаковыми физическими, химическими и термодинамическими свойствами во всех точках – это…
1) фаза
2) компонент
3) система
4) тело
5) область
46. Повышение температуры кипения раствора по сравнению с температурой кипения чистого растворителя – это…
1) криоскопия
2) турбидиметрия
3) эбуллиоскопия
4) осмос
5) однозначного ответа нет
47. Понижение температуры замерзания раствора по сравнению с температурой замерзания чистого растворителя – это…
1) криоскопия
2) турбидиметрия
3) эбуллиоскопия
4) осмос
5) однозначного ответа нет
48. Коэффициент распределения (К) вещества в гетерогенной системе зависит от:
1) температуры и природы компонентов
2) давления
3) температуры
4) концентрации
5) природы компонентов
49. С увеличением числа кратности экстракции (n) степень извлечения вещества…
1) увеличится
2) уменьшится
3) не изменится
4) сначала увеличится, а затем уменьшится
5) сначала уменьшится, а затем увеличится
50. Условие термодинамического равновесия при p,Т= const для двухфазной однокомпонентной системы:
1) ![]()
2) ![]()
3) ![]()
4) ![]()
5) ![]()
51. Число молекул, одновременно сталкивающихся и реагирующих в элементарном акте химического превращения – это…
1) Порядок
2) Молекулярность
3) Молярность
4) Эквивалент
5) Затрудняюсь ответить
52. Показатель степени при концентрации реагирующего вещества в кинетическом уравнении реакции – это…
1) Полный порядок
2) Частный порядок
3) Молекулярность
4) Эквивалент
5) Молярность
53. Скорость последовательной реакции зависит от концентрации
1) промежуточных продуктов реакции
2) продуктов реакции
3) исходных веществ
4) исходных веществ и продуктов реакции
5) исходных веществ и промежуточных продуктов реакции
54. Численные значения молекулярности и порядка совпадают:
1) для одностадийных реакций
2) для сложных реакций
3) в элементарных актах химических превращений
4) для сопряженных реакций
5) для цепных реакций
55. Гетерогенная реакция – это реакция, протекающая…
1) на поверхности раздела фаз
2) при одинаковом агрегатном состоянии всех реагирующих веществ
3) в гзообразной среде
4) в пределах одной фазы
5) в жидкой среде
56. Константа скорости химической реакции характеризует
1) состояние химического равновесия
2) зависимость скорости реакции о температуры
3) скорость реакции при концентрации реагирующих веществ, равных 1
4) зависимость скорости реакции от концентрации реагирующих веществ
5) скорость реакции при постоянных концентрациях реагирующих веществ.
57. Величина константы скорости химической реакции зависит от
1) температуры
2) катализатора
3) природы реагирующих веществ
4) концентрации реагирующих веществ
5) механизма реакции
58. Константа скорости реакции не зависит от
1) природы реагирующих веществ
2) присутствия катализатора
3) природы растворителя, в котором ведется реакция
4) температуры
5) концентрации реагирующих веществ
59. 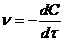 , если С – концентрация
, если С – концентрация
1) исходного вещества
2) продуктов реакции
3) любых веществ
4) равна 1
5) не изменяется
60. Гомогенная реакция – это реакция, протекающая
1) между твердым и газообразным веществом
2) в растворе
3) на поверхности раздела фаз
4) в пределах одной фазы
5) таких не бывает
61. Скорость и константа скорости реакции одновременно зависят от
1) времени
2) концентрации реагирующих веществ
3) объема реакционного сосуда
4) концентрации продуктов реакции
5) температуры
62. Процесс протекает в диффузионной области, если
1) лимитирующей стадией является диффузия веществ
2) лимитирующей стадией является химическая реакция на поверхности раздела фаз
3) диффузионная область в гетерогенном процессе отсутствует
4) коэффициент диффузии больше константы скорости реакции
5) никогда не протекает в диффузионной области
63. Увеличение скорости реакции при введении в систему положительного катализатора объясняется
1) повышением средней кинетической энергии молекул реагирующих веществ
2) уменьшением доли активных частиц
3) повышением энергии активации реакции
4) уменьшением энергии активации реакции
5) уменьшением константы скорости реакции
64. При введении катализатора в реакционную смесь не изменяется:
1) константа скорости реакции
2) энергия активации реакции
3) скорость реакции
4) доля активных частиц в реакционной смеси
5) константа химического равновесия обратимой реакции
65. В каких координатах следует спрямлять зависимость константы скорости от температуры, чтобы найти энергию активации?
1) х=Т, у=lnk
2) x=1/n, y=k
3) x=lnT, y=lnk
4) x=T, y=k
5) x=1/T, y=lnk
66. Укажите размерность константы скорости реакции, порядок которой равен n=-1?
1) 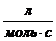 2)
2) ![]() 3)
3) 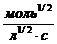 4)
4) ![]() 5)
5) ![]()
67. От чего зависит константа химической реакции?
1) от температуры и концентрации реагирующих веществ
2) только от природы реагирующих веществ
3) только от природы
4) от температуры и времени
5) от природы реагирующих веществ и температуры

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |




