Схема 5
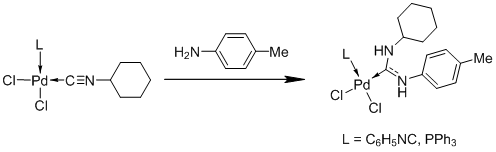
Этим методом можно синтезировать даже бис-(ациклические диаминокарбеновые) комплексы палладия с хиральными N-заместителями [26], что невозможно любым другим способом (Схема 6).
Схема 6
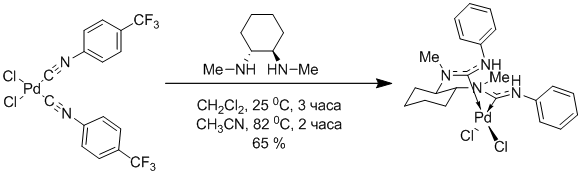
Простота и удобство данного метода позволяет синтезировать большой набор ациклических диамнокарбеновых комплексов палладия с хорошими выходами.
В качестве N-нуклеофилов могут выступать ароматические амины [25], алифатические амины [26], гидразины [27], гидразоны [28] и этот круг нуклеофилов будет расширяться.
2.3. Свойства ациклических диаминокарбенов, как вспомагательных лигандов
Ациклические диаминокарбены (ADCs), получили значительно меньшую распространенность в качестве вспомогательных лигандов, чем NHCs. Хотя ациклические диаминокарбены являются полными аналогами гетероциклических. Наличие двух атомов азота у карбенового атома углерода ADCs должно оказать электронную стабилизацию аналогичную доказанной для NHCs [29]. Некоторые работы посвященные ADCs [30-34] указывают на свойства ADCs лигандов, которые могут предоставить определенные преимущества по сравнению с NHCs.
Как говорилось выше, свободные ациклические карбены менее устойчивы, чем циклические аналоги. Устойчивых ADCs синтезировано значительно меньше, чем NHCs, в силу того, что стабильными являются только те ациклические диаминокарбены, которые при атомах азота имеют объемные заместители, и это является существенным недостатком как в получение свободных карбенов, так и в их координации к металлоцентру. Такие рекции протекают с очень низкими выходами. Бис-(диизопропиламино)карбен (11) (Рисунок 2), полученный депротонированием формамидиниевого иона с помощью LDA [11], был найден стабильным в растворе и мог сублимироваться без разложения, хотя проявлял более высокую чувствительность к воздуху и к влажности, чем свободные NHCs. В случае менее стерически насыщеных бис-(N-пиперидил)карбенов (12) [12] и бис-(диэтиламино)карбенов (13) [35], наблюдается процесс димеризации в тетраазаэтилены, а бис (диметиламино)карбены (14) [36] и вовсе распадается на неидентифицируемые продукты при 0 °С. К примеру, в отличие от ADCs, димеризация NHCs термодинамически запрещена даже без особой стерической насыщенности N-заместителей [37].
В силу своей малой стабильности ациклические диаминокарбены в большинстве случаев не могут существовать в виде индивидуальных соединений, и этим можно объяснить их низкую распространенность и применимость.
Рисунок 2
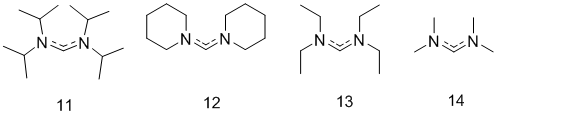
Однако, в координированной форме ациклические диаминокарбены устойчивы и проявляют стабильность аналогичную циклическим.
Кроме того, ADCs могут выступать в качестве более сильных σ-доноров, чем NHCs [30,38]. К тому же, из-за их большего N-C-N угла можно разместить более стерически объемные лиганды, что повлияет на конфигурационную гибкость коплекса и будет препятствовать вращению вокруг карбенового связей С-N [11,39], повышая при этом сопряжение p-орбиталей атомов азота с р-орбиталями карбенового атома углерода.
Их большая σ-донорная способность по сравнению с циклическими диаминокарбенами может быть доказана по смещению сигналов карбенового атома углерода в спетрах ЯМР 13С в ряду состоящем из циклического ненасыщенного, циклического насыщенного и ациклического диаминокарбеного комплекса родия (Рисунок 3), слева на право соответственно.
Рисунок 3
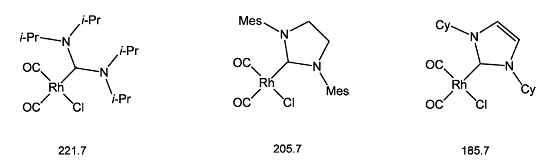
А по частотам колебания С=O связи (ν(CO)) соответствующих комплексов (Таблица 1) можно подтвердить предыдущее утверждение, так как при увеличение σ-донорных свойств лиганда соседа, то есть лиганда находящегося по соседству с карбонильным лигандом (С=O) в координационной сфере металла, происходит ослабление энергии C=O связи и соответственно уменьшение частоты ее колебания, что мы и наблюдаем [40].
Таблица 1
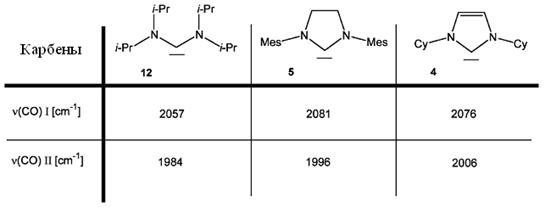
Работ по исследованию ADCs в качестве вспомогательных лигандов в катализе было очень мало [22,41-43], но они показали хорошие результаты. Каталитическая активность ациклических диаминокарбеновых комплексов была такой же или чуть лучше по сравнению с аналогичными NHC системами, но данные работы были описаны только для определенных типов Pd-катализируемых взаимодействий.
К настоящему времени в литературе отсутствуют работы по исследованию каталитической активности ADC в реакции Соногаширы.
2.4. Реакция Соногаширы
Несимметричные алкины могут быть получены в мягких условиях с помощью реакции терминальных алкинов с арилзамещенными йодидами или виниловыми бромидами в присутствии каталитического количества Pd(PPh3)2Cl2 и йодида меди (CuI), впервые это было обнаружено в 1975 Соногаширой [44] и его сотрудниками.
Одновременно две исследовательские группы Р. Хека и Л. Кассара независимо открыли подобные Pd-катализируемые процессы, но они не использовали медный cокатализатор, и условия реакции были жёстче.
Медно-палладий катализируемое сочетание терминальных алкинов с арил - и винилгалогенидами с образованием енинов известно как реакция кросс-сочетания Соногаширы и она может быть рассмотрена как каталитическая версия сочетания Кастро-Стивенса.
Общие особенности реакции:
1) Кросс-сочетание обычно проводиться при умеренных температурах, и это - главное преимущество реакции Соногаширы, перед жесткими условиями, требуемыми для альтернативы сочетания Кастро-Стивенса;
2) Побочных реакций с участием ацетиленидов меди избегают при помощи использования каталитического количества солей меди (I);
3) В качестве солей меди (I) чаще используются коммерчески доступные и стабильные CuI или CuBr и обычно применяются в 0.5-5 % мольных относительно галогенида или алкина;
4) Наибольшее распространение получили катализаторы палладия Pd(PPh3)2Cl2 или Pd(PPh3)4;
5) Растворители и реактивы не обязательно должны быть строго высушены. Однако, полное дегазирование очень важно, так как фосфиновые комплексы палладия проявляют низкую устойчивость к окислительному действию кислорода;
6) Реакция работает одинаково хорошо как для микро, так и для макро количеств;
7) Реакция - стереоспецифичная; стереохимия субстратов сохранена в продуктах;
8) Ряд активности для арил и винил галогенидов такой I ≈ OTf>Br>>Cl;
9) Различие между показателями активности йодидов и бромидов позволяют селективно проводить реакцию с йодидами в присутствии бромидов;
10) Реакция инертна ко многим функциональным группам которые входят в состав ароматическом или виниловых галогенида.
Часто, механизм [45] реакции Соногаширы в литературных данных представляют в виде двух каталитических циклов: цикл с участием Pd0(L)2 и Cu(I) (Рисунок 4).
Рисунок 4
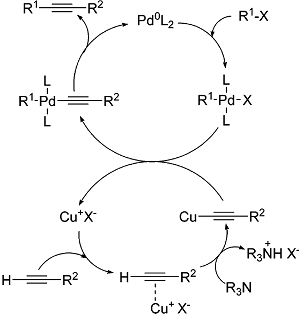
Каталитический цикл палладия:
1) Активной формой палладиевого катализатора является четырнадцати электронное состояние Pd0(L)2 , которое реагирует с арил - или винилгалогенидным субстратом по реакции окислительного присоединения и образуется четырехкоординированный комплекс Pd2+;
2) Этот комплекс вступает в реакцию переметаллирования с ацетилинидом меди, с отщеплением CuHal;
3) Затем, из запрещенной для восстановительного элиминирования транс-конфигурации, образуется разрешенная цис-конфигурация;
4) В заключительном этапе по реакции восстановительного элиминирования образуется целевой продукт кросс-сочетания с регенерацией Pd0(L)2.
Медный цикл:
1) Взаимодействие CuX c терминальными ацетиленами приводит к образованию ацетилинида меди, которое ускоряется за счет действия основания;
2) Далее, образовавшийся ацетиленид меди вступает в реакцию переметалирования с последующий регенерацией галогенида меди (I).
Побочная реакция - это реакция Глазера, которая идет с образованием интернальных диацетиленидов.
Существуют также и безмедные варианты реакции Соногаширы. Однако, существует мнение а том, что палладиевые катализаторы могут быть загрязнены солями меди [46] и поэтому говорить о безмедном варианте не корректно.
2.5. Палладиевые катализаторы для реакции Соногаширы
Реакция Соногаширы обычно катализируется фосфиновыми комплексами палладия в присутствии каталитического количества солей меди(I). Традиционно используются катализаторы с трифенилфосфиновыми лигандами, например, тетракис-(трифенилфосфин)палладия Pd(PPh3)4, но из-за своей большей стабильности и растворимости в катализ используется Pd(PPh3)2Cl2, как аналог предыдущего. В этом случае процесс требует достаточно высокой загрузки катализатора (обычно 5мол%) и большое количество соли меди(I), поэтому на данный момент является актуальной задачей поиск более активных катализаторов.
Кроме фосфиновых комплексов, в литературе известны реакции, где катализ осуществляется комплексами палладия с азотсодержащими лигандами. К примеру, пиридины и пиримидины образуют достаточно устойчивые комплексы с палладием, которые могут быть использованы в качестве катализаторов реакции Соногаширы. Таким образом, дипиридиновых палладиевый комплекс 15 (Рисунок 5), полученный смешиванием соответствующего дипиридина с H2[PdCl4],был успешно использован в безмедном варианте реакции Соногаширы на примере иод-, бром-и хлорбензола с фенилацетиленом и использованием три-н-бутиламинв качестве основания в тетрагидрофуране (ТГФ) при температуре 65 °C, реакции проходили с хорошими выходами [47].
Рисунок 5
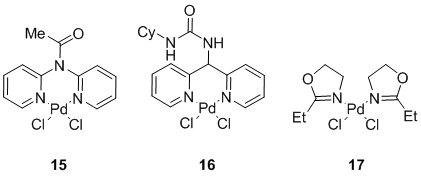
Комплекс 16 был использован в безмедной реакции Соногаширы арилиодидов и арилбромидов в N-метилпирролидоне (NMP) с использованием тетра-н-бутиламмония ацетата (TBAA) в качестве основания при 110°С [48]. Интересно отметить, что комплекс 16 катализировал реакцию даже на воздухе и в воде с использованием в качестве основания пирролидина [48] (Схема 7), хотя его эффективность была выше в случае использования NMP, как растворителя, и пирролидина с добавкой тетра-н-бутиламмония бромида (TBAB), в качестве основания.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



