4. Экспериментальная часть
Спекты ЯМР 1H (300,13 Мгц) сняты на приборе «Bruker» для растворов в CDCl3
Масс-спектры получали на масс-спектрометре Bruker micrOTOF.
Продажные реактивы
4-иоданизол, 98%; фирма Acros Organics; CAS: 696-62-8
2-метилбут-3-ин-2-ол, 99%; фирма Acros Organics; CAS: 115-19-5
Трет-бутилизоцианид, 99%; фирма Acros Organics; CAS: 7188-38-7
Подготовка растворителей
Этанол: продажный препарат кипятили в течение 6 часов над свежепрокаленнм CaO, затем выдерживали 5 часов над CaO и перегоняли без доступа влаги над натрием.
Хлороформ: продажный реактив очищали встряхиванием с концентрированной H2SO4 после чего промывали водой, сушили над CaCl2 и перегоняли над P2O5.
4.1. Синтетическая часть
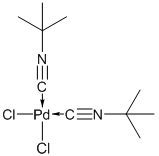
4.1.1. Синтез бис-(ацетонитрил)-палладия дихлорида
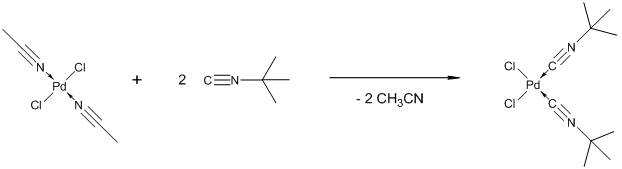
В колбу на 25 мл, снабженную магнитной мешалкой, поместили 0,78 г (3 ммоль) бис-(ацетонитрил)палладий дихлорида (Pd(NCCH3)2Cl2) и прилили 5 мл ацетнитрила. После того как весь осадок растворился, прилили 0,5 г (6 мммоль) третбутилизоцианида (CNC(CH3)3). Через 10 минут перемешивания при комнатной температуре выпал белый осадок. Образовавшийся осадок отфильтровали на фильтре Шотта и промыли сначала ацетонитрилом, потом диэтиловым эфиром. Осадок сушили под вакуумом. Было получено 0,91 г (88%) бис-(ацетонитрил)палладий дихлорида в виде белого порошка. Спектр ЯМР 1Н (300,13 МГц, CDCl3), d, м. д.: 1.55 с (транс - 18H, C(CH3)3), 1.92 с (цис - 18H, C(CH3)3),
4.1.2. Синтез Катализатора 3
В колбу на 10 мл, снабжённую магнитной мешалкой и обратным холодильником, поместили 0.034 г (0.1 мммоль) бис-(третбутилизонитрил)палладий дихлорида (Pd(CNBut)2Cl2, 0.022 г (0,11 ммоль) N-гидрокси-3,4-диметоксибензамидина (C6H3(OMe)2C(NH)NOH), добавили 2 мл хлороформа (CHCl3). Реакцию проводили при температуре 65 0C. После растворения всех компонентов реакционная масса стала приобретать желтую окраску. Через 4 часа хлороформ был удален в вакууме и получен остаток 0.049 г в виде мелкокристаллического порошка коричневого цвета.
4.1.3. Синтез 4-(4-метоксифенил)-2-метилбут-3-ин-2-ола
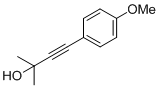 В колбу на 20 мл, снабжённую магнитной мешалкой и обратным холодильником, поместили 0.702 г (3 ммоль) 4-иоданизола, 0.278 г (3,3 мммоль) 2-метилбут-3-ин-2-ола, 10 мл ТГФ и 0.118 г (0.45 ммоль) трифенилфосфина (PPh3). Аргон продували через полученный раствор в течение 10 минут. После чего добавили в раствор 0.021 г (0.3 ммоль) бис-(трифенилфосфин)палладий дихлорида, продували аргон еще 5 минут и добавили 0.057 г (0,3 ммоль) иодида меди (CuI). После добавления CuI реакционную систему изолировали от атмосферы и включили нагрев. Реакции шла при температуре 60 0С и закончилась через 3 часа. Конец реакции был установлен методом ТСХ. Реакционная масса была отчищена методом жидкостный колоночной хромотографией. В качестве элюента была подобрана система этилацетат : гексан в соотношении 3:4 . Было получено 0.542 г (95%) 4-(4-метоксифенил)-2-метилбут-3-ин-2-ола в виде коричневых кристаллов т. пл. 50-51 ºС (лит. т. пл. 51-53 °C [60]). Спектр ЯМР 1Н (300,13 МГц, CDCl3), d, м. д.: 1.63 с (6H, C(CH3)2), 2.00 с (1H, OH), 3.83 с (3H, OCH3), 6.84 д (2Hаром, C6H4), 7.37 д (2Hаром, С6H4);
В колбу на 20 мл, снабжённую магнитной мешалкой и обратным холодильником, поместили 0.702 г (3 ммоль) 4-иоданизола, 0.278 г (3,3 мммоль) 2-метилбут-3-ин-2-ола, 10 мл ТГФ и 0.118 г (0.45 ммоль) трифенилфосфина (PPh3). Аргон продували через полученный раствор в течение 10 минут. После чего добавили в раствор 0.021 г (0.3 ммоль) бис-(трифенилфосфин)палладий дихлорида, продували аргон еще 5 минут и добавили 0.057 г (0,3 ммоль) иодида меди (CuI). После добавления CuI реакционную систему изолировали от атмосферы и включили нагрев. Реакции шла при температуре 60 0С и закончилась через 3 часа. Конец реакции был установлен методом ТСХ. Реакционная масса была отчищена методом жидкостный колоночной хромотографией. В качестве элюента была подобрана система этилацетат : гексан в соотношении 3:4 . Было получено 0.542 г (95%) 4-(4-метоксифенил)-2-метилбут-3-ин-2-ола в виде коричневых кристаллов т. пл. 50-51 ºС (лит. т. пл. 51-53 °C [60]). Спектр ЯМР 1Н (300,13 МГц, CDCl3), d, м. д.: 1.63 с (6H, C(CH3)2), 2.00 с (1H, OH), 3.83 с (3H, OCH3), 6.84 д (2Hаром, C6H4), 7.37 д (2Hаром, С6H4);
4.2. Исследования каталитической активности катализаторов 1 и 2
 | |||
 | |||
|
|
Модельная реакция
Во всех случаях в реакцию были взяты 1-иод-2-нитробензол (0.610 г, 2.45 ммоль) и окт-1-ин (0.550 г, 5.00 ммоль). Во всех случаях кроме 6 и 7, CuI (0.045г, 9.60 ммоль%) был добавлен как сокатализатор, и во всех случаях кроме 5, PPh3 (0.030 г, 4.60 ммоль%) был добавлен в реакционную смесь. Все опыты были проведены при температуре 60 ºC кроме 1 и 2 (проводились при 20 ºC) до исчезновения исходного иодида. Конверсия определялась на основе анализа спектров ЯМР (1H), по наиболее слабопольным сигналам протонов ароматического кольца находящихся рядом с нитрогруппой.
1-нитро-2-(окт-1-инил)бензол
Спектр ЯМР 1Н (300 МГц, CDCl3), , м. д.: 0.92 (3H, т, J=6 Гц, CH3); 1.25 – 1.40 (4H, м, (СН2)2); 1.41 – 1.58 (2H, м, (СН2));1.63 (2H, дт, J=7 Гц, ССН2СН2); 2.49 (2H, т, J=7 Гц, ССН2); 7.39 (1H, т, J=7 Гц, H-CAr), 7.49-7.65 (2H, м, H-CAr), 7.96 (1H, д, J=7 Гц, H-CAr).
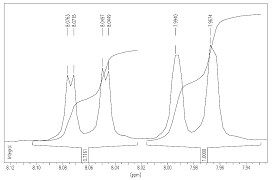
Таблица 1. Определение каталитической активности комплексов 1 и 2 в реакции Соногаширы.
№ опыта | Катализатор | Загрузка катализатора, моль% | Растворитель | Основание | Время, ч | Конверсия (выход), % | TON | TOF, ч–1 |
1 | 1 | 0.07 | THF | Et3N | 96 | 99 (94) | 1400 | 150 |
2 | 2 | 0.07 | THF | Et3N | 68 | 99 | 1400 | 150 |
3 | 1 | 0.07 | THF | Et3N | 24 | 99 | 1400 | 60 |
4 | 2 | 0.07 | THF | Et3N | 12 | 99 | 1400 | 1200 |
5 | 1 | 0.07 | THF | Et3N | 24 | 20 | 290 | 12 |
6 | 1 | 0.07 | EtOH | K2CO3 | 24 | – | – | – |
7 | 2 | 0.07 | EtOH | K2CO3 | 24 | 10 | 140 | 6 |
8 | 1 | 0.07 | EtOH | K2CO3 | 20 | 99 (96) | 1400 | 100 |
9 | 2 | 0.07 | EtOH | K2CO3 | 5 | 99 | 1400 | 280 |
10 | [PdCl2(PPh3)]2 | 0.1 | EtOH | K2CO3 | 18 | 40 | 400 | 22 |
11 | 1 | 0.1 | EtOH | K2CO3 | 18 | 99 | 990 | 55 |
12 | 2 | 0.1 | EtOH | K2CO3 | 4 | 99 | 990 | 250 |
13 | 2 | 0.05 | EtOH | K2CO3 | 18 | 99 | 2000 | 110 |
Синтез 1-(додека-1,3-диинил)-2-нитробензола
К суспензии K2CO3 в 12 мл EtOH добавили 2-иоднитробензол 494 мг (1.98 ммоль), додека-1,3-диин 500 мг (3.08 ммоль), «Катализатор 2» 1 мг (1.6х10-3 ммол), PPh3 50 мг (0.2 ммоль), последним вносили CuI 40 мг (0.2 ммоль). Далее реакционную смесь нагревали до температуры 450С и перемешивали в течение 6 часов. После исчезновения исходного иодида (контроль ТСХ) реакционную смесь выливали в воду, отделяли органический слой, водный экстрагировали CH2Cl2. Объединенные органические слои промыли водным раствором NH4Cl и сушили над CaCl2. После удаления растворителей продукты выделяли методом колоночной хроматографии (силикагель, EtOAc / петролей) получено 545 мг, выход продукта составил 97%.
Спектр ЯМР 1Н (300 МГц, CDCl3), , м. д.: 0.90 (3H, т, J=6 Гц, CH3); 1.18 – 1.47 (10H, м, (СН2)5); 1.62 (2H, дт, J=7 Гц, ССН2СН2); 2.40 (2H, т, J=7 Гц, ССН2); 7.48 (1H, т, J=7 Гц), 7.59 (1H, т, J=7 Гц), 7.67 (1H, д, J=7 Гц), 8.09 (1H, д, J=7 Гц, H-CAr). Спектр ЯМР 13C, (75 МГц, CDCl3), , м. д.: 14.54, 20.13, 23.14, 28.58, 29.33, 29.40, 29.54, 32.25, 65.48, 69.72, 82.79, 89.14, 118.48, 125.26, 129.44, 133.33, 136.38, 150.56.
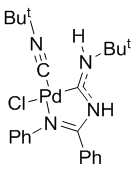
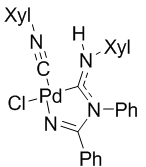
4.3. Исследования каталитической активности катализаторов 3 и 4
Структуры исследуемых катализаторов
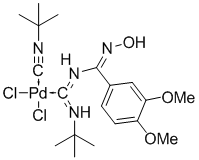
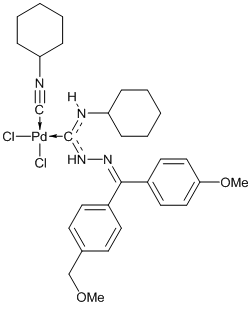
Катализатор 3* Катализатор 4
*Наиболее вероятная структура.
4.2.1 Общая методика проверки каталитической активности диаминокарбеновых комплексов палладия на реакции Pd/Cu катализируемого кросс-сочетания 4-йоданизола с 2-метилбут-3-ин-2-олом (реакция Соногаширы).
Процедура A
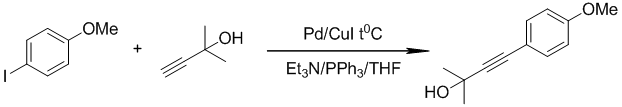

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



