Санкт-Петербургский Государственный Университет
Химический факультет
Кафедра органической химии
Дипломная работа
на тему
Исследование каталитической активности ациклических диаминокарбеновых комплексов палладия (II) в реакции Соногаширы
Студент IV курса:
Научный руководитель:
ст. преп, к. х.н.
Заведующий кафедрой
проф., д. х.н.
Санкт-Петербург
2011
Содержание
1. Введение 3
2. Литературный обзор 5
3. Обсуждение результатов 21
4. Экспериментальная часть 30
5. Выводы 39
6. Список используемой литературы 40
1. Введение.
Применение Pd-катализируемых реакций кросс-сочетания является на данный момент одним из наиболее эффективных методов создания новой углерод-углеродной связи. Несмотря на то, что в 2010 году Нобелевская премия по химии была присуждена трем ученым, внесшим наибольший вклад в развитие реакций кросс-сочетания, катализируемых комплексами переходных металлов, и, в частности, палладия, это направление продолжает бурно развиваться. Перспективными и актуальными остаются исследования, направленные как на открытие новых превращений, катализируемых комплексами переходных металлов, так и на совершенствование каталитических систем для уже известных химических превращений. Наиболее важными в этой области являются проблемы, связанные с необходимостью получения катализаторов с более высокой каталитической активностью и устойчивостью в условиях реакции, каталитических систем для осуществления стереоселективных синтезов. Кроме того, до сих пор остается не очевидной связь строения комплекса переходного металла с его каталитической активностью, поэтому исследования в этом направлении также являются актуальными.
В настоящее время в качестве гомогенных катализаторов в реакциях кросс-сочетания обычно используются палладиевые комплексы с фосфиновыми лигандами. Расширение круга возможных субстратов требует разработки более активных и стабильных каталитических систем. Сравнительно недавно появились сообщения об использовании в качестве альтернативы фосфиновым комплексам палладия комплексов, содержащих лиганды карбенового типа с циклическими (а) и ациклическими (б) диаминокарбенами [55,56] (Рисунок 1):
Рисунок 1
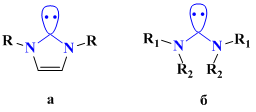
Аминокарбеновые комплексы показывают большую стабильность по сравнению с фосфиновыми по отношению к окислению, природе растворителя и основания. Кроме того, карбеновые комплексы палладия, благодаря донорным свойствам лиганда, чрезвычайно активны в реакциях окислительного присоединения арилгалогенидов. Вследствие этого подобные комплексы являются высокоэффективными катализаторами различных реакций образования связи углерод–углерод, использующих арилгалогениды в качестве субстратов: реакции Сузуки-Мияура, Хека, Соногаширы [57,58,59]. Однако, известные методы получения таких комплексов, основанные на предварительном синтезе карбенового лиганда с последующим введением его в координационную сферу металлокомплекса, являются многостадийными и трудоемкими, что ограничивает возможности варьирования структурных параметров комплексов.
В первые открытый Чугаевым Львом Александровичом [23], способ получения аминокарбеновых комплексов нового типа с использованием металлопромотируемых реакций нуклеофильного присоединения к координированным изонитрилам должен позволить позволит широко варьировать структуру образующегося комплекса и, как следствие, предоставит хорошую возможность изучения взаимосвязи между структурой комплекса и его каталитической активностью.
Цели и задачи квалификационной работы:
1. Провести исследования каталитической активности полученных ранее ациклических аминокарбеновых комплексов палладия в реакции Соногаширы.
2. Разработать методику получения каталитических системы на основе ациклических аминокарбеновых комплексов палладия для исследования каталитической активности.
2. Литературный обзор
2.1. Некоординированые диаминокарбены
Диаминокарбены – соединения, имеющие в своем составе двухвалентный атом углерода, находящийся в шестиэлектронном окружении, и связанный с двумя аминогруппами. Данный тип карбенов имеет угловое строение и является синглетным по природе.
Долгое время не удавалось синтезировать устойчивых карбенов, из-за их низкой стабильности. В начале 1960-х, Ванзлик предположил, что устойчивость карбенов может быть увеличена наличием амино-заместителей и пытался получить 1,3-дифенилимидазолидин-2-илиден (2) из 1, термическим удалением хлороформа (Схема 1) [1].
Схема 1
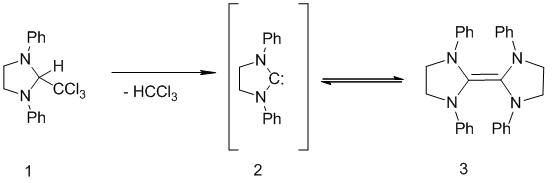
В то время, был получен только димерный тетраазоолефин (3), и равновесие между 3 и двумя единицами карбена оказалось сильно смещено в сторону димера [2-4]. Однако, только через 30 лет в работе Денка [5] было доказано существование этого равновесия.
В 1970 году Ванзлик с сотрудниками показали, что соли имидазолия (4a, b), могут быть депротонированны третбутоксидом калия с образованием соответствующих имидазол-2-илиденов (5a,b), которые были зафиксированы, но не выделены [6]. Следуя этому принципу, почти двумя десятилетиями позже Аргуенгом были получены стабильные кристаллические карбены [7]. Соединение 5c было получено с количественным выходом с помощью депротонирования 1,3-ди-1-адамантилимидазолил хлорида (4с) гидридом калия в присутствии каталитических количеств трет-бутилата калия (Схема 2).
Схема 2
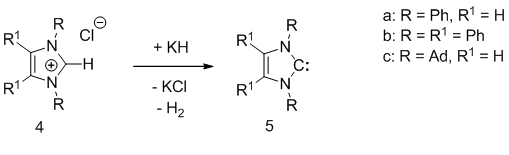
Бесцветные кристаллы 5с оказались термически стабильными и плавящимися при 240-241 0С без разложения.
За последние годы было синтезировано множество устойчивых аминокарбенов: имидазолидин-2-илидены (6) [8], тетрагидропиримид-2-илиден (7) [9], имидазол-2-илидены (8), 1,2,4-триазол-5-илидены (9) [10], и некоторое количество ациклических (10) [11,12](Рисунок 1).
Рисунок 1
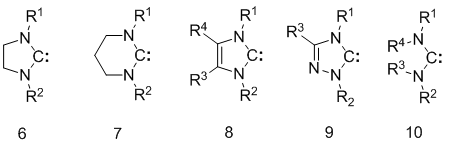
Стабильность синглетных карбенов 6-10 является результатом электронных эффектов (положительного мезомерного (+М), а также отрицательного индуктивного (-I)) [13]. Ароматический характер 6 π-электронов пятичленных карбеновых циклов 8, 9 в последнее время является плохо изученной областью [14,15]. Ранее, Диксон и Аргуенго [16] объяснил чрезвычайную устойчивость этих карбенов за счет индуктивного влияния соседних атомов азота. Считалось, что сопряжение неподеленных пар электронов от атомов азота и электронов двойной С=С связи должна обеспечить достаточную кинетическую стабильность карбена [17]. Однако, последующие исследования Циословского [18] показали, что π-донорная способность неподеленных пар азота играет только незначительную роль. К концу спор пришел только в 1996 году, когда Апелойг [19] и Френкин [20] независимо изучали ароматичность карбенов 8. По структурным, термодинамическим и магнитным критериям, а также с помощью измеренной π-заселености и потенциалов ионизации, был сделан вывод о том, что циклическая делокализация электронов действительно происходит в имидазол-2-илиденах, но характер ароматичности менее выражен, чем в их предшественниках, солях имидазолия 4. Таким образом, ароматичность не является основным стабилизирующим эффектом для карбенов 8. Более важным является взаимодействие карбенового центра с σ-π-донорными аминогруппами. Это объясняет то, что диаминокарбены типа 6, 7 тоже проявляют устойчивость и также могут быть выделены в виде свободных соединений [8,9].
За счет своих σ-донорных π-акцепторных свойств карбеновый атом углерода в диаминокарбеновом фрагменте может выступать в качестве комплексообразующего агента. За последние годы было синтезировано большое количество диаминокарбеновых комплексов переходных металлов. Многие из них являются интересными объектами для исследований и широко используются в современной химии в качестве катализаторов. Однако, наибольшее распространение в научно-исследовательском мире получили циклические варианты диаминокарбенов, их невероятная устойчивость в виде свободных кристаллических карбенов дает им преимущество перед ациклическими аналогами.
2.2.Синтез ациклических диаминокарбеновых комплексов палладия
Меньшая распространенность ациклических диаминокарбенов (ADCs) по сравнению с NHCs является результатом меньшей стабильности свободного карбена и соответственно более сложным способом генерации (Схема 3).
Схема 3
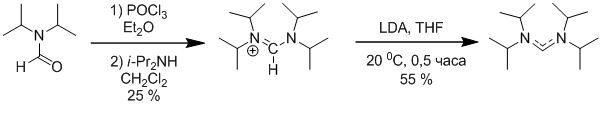
К тому же, реакция получения формамидиниевого иона проходит с низким выходом и дает побочные продукты [21], и в силу меньшей кислотности для депротонирования необходимо использование более сильного основания, такого как литийдиизопропиламин (LDA). Поэтому для получения ациклических карбеновых были разработаны другие методы.
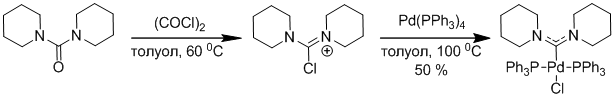
Один из способов получения ациклических диаминокарбеновых комплексов был продемонстрирован Фурстнером [22]. Метод получения заключается в окислительном присоединении тетракис-(трифинилфосфин)палладия Pd(Ph3P)4 по C-Cl связи хлороамидиниевых ионов (Схема 4). Однако, этот путь многостадиен и требует использования только фосфиновых комплексов палладия, что ограничивает его применимость.
Схема 4
Существует другой подход к синтезу ациклических диаминокарбеновых комплексов палладия, получивший наибольшую распространенность в силу своей простоты. Реакция заключается в нуклеофильном присоединения азотсодержащего нуклеофила (N-нуклеофила) по скоординированному изонитрилу. Первый ADC комплекс данным методом был синтезирован еще Чугаевым в 1915 году [23], но был не верно описан, как сложный комплексный димер, соединенный через гидразин. Истинная структура была определена позднее в работах Шоу.[24] Однако, первыми открывателями этого метода, применимого для получения соответствующих комплексов палладия, была группа Ричарда [25], которые в качестве N-нуклеофила использовали анилины (Схема 5).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



