На следующем этапе мы решили провести сравнительный эксперимент с широко используемым коммерчески доступным бис-(трифенилфосфин)палладий дихлоридом (Таблица 2, Опыты 10-12). Реакции проводились в среде этанола при использовании карбоната калия в качестве основания и добавок CuI и PPh3. Через 3 часа после начала реакции в случае использовании PdCl2(PPh3)2 конверсия по данным спектроскопии ЯМР 1H составила 35%, которая через 24 часа увеличилась до 40%. В тех же условиях каталитическая система на основе комплекса 1 позволила получить конверсию в 40% через три часа и 99% через 24 часа. Лучшие результаты показала каталитическая система на основе комплекса 2, так уже через 3 часа конверсия составила 99%.
С целью установления оптимального соотношения катализатор / арилйодид был проведен эксперимент с 0.05 мольными процентами катализатора 2, максимальное значение TON в 1980 (при конверсии в 99%) было достигнуто через 18 часов.
На следующем этапе работы мы решили применить показавшую себя лучше всего каталитическую систему на основе диаминокарбенового комплекса 2 к синтезу 1-(додека-1,3-диинил)-2-нитробензола.
Подобные соединения (ортодиинилзамещенные арены) представляют значительный интерес в тандемных циклизациях. Но, к сожалению, набор методов их синтеза серьезно ограничен, и очень часто именно реакция Соногаширы используется в качестве ключевой стадии. В связи с вышеизложенным, нам представляется довольно актуальным поиск каталитических систем для проведения реакции Соногаширы в ряду диацетиленов.
Схема 9
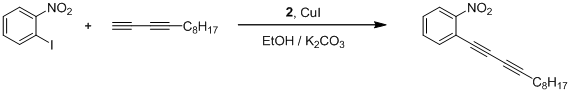
Реакцию (Схема 9) проводили в условиях опыта 9 (Таблица 2), но из-за низкой стабильности терминальных диацетиленов было решено понизить температуру до 500С. По данным ТСХ исходный арилйодид полностью прореагировал за 6 часов. Продукт реакции 1-(додека-1,3-диинил)-2-нитробезнол был выделен с помощью колоночной хроматографии, его выход составил 97%. Стоит отметить, что в предыдущих работах [63] данное соединение было получено с выходом 80% при использовании 10 мольных процентов Pd(OAc)2
3.1. Исследование каталитической активности ациклического аминокарбенового комплекса 3 и сравнение его с Pd(CNBut)2Cl2
Для дальнейших исследований было решено синтезировать новую каталитическую систему. Предварительно был синтезирован бис-(третбутилизонитрил)палладий дихлорид. Причем продукт получился в виде смеси состоящей из цис- и транс-изомеров в соотношении 2:1, что было подтверждено спектрами ЯМР 1H по двум соответствующим сигналам протонов третбутильной группы в цис- и транс-форме.
В дальнейшем нами было решено разработать методику исключающую выделение образующегося аминокарбенового комплекса с целью более эффективного исследования каталитической активности. Нами было отмечено, что при проведении реакции изонитрильного комплекса с нуклеофилами, довольно часто остается значительное количество непрореагировавшего исходного бис-(изонитрил)палладий дихлорида, этот факт возможно объясняется различной скоростью нуклеофильного присоединения по изонитрильной группе в цис- и транс-форме исходного изоцианидного комплекса. Поскольку сам бис-(изонитрил)палладий дихлорид может выступать в роли катализатора в реакции Соногаширы было решено подобрать такую модельную реакцию, в которой он не проявлял бы заметной каталитической активности.
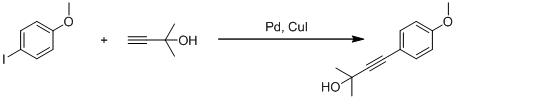
Был проведен холостой опыт, показавший, что реакция 1-йод-2-нитробензола с окт-1-ином может быть катализирована исходным изонитрильным комплексом палладия. С целью устранения данного влияния была предложена, в качестве модельной реакция 4-иоданизола с карбинолом Фаворского (Схема 10). При проведении холостого опыта образование продуктов сочетания при катализе бис-(изонитрил)палладий дихлоридом, при температуре 65 0С не было зафиксировано даже через 20 часов. В дальнейшем эксперименты по исследованию каталитической активности проводили с использованием данной модельной реакции. Кроме того различия в параметрах удерживания при проведение хроматографического разделения между исходным веществом и продуктом реакции позволили упростить процесс выделения.
В качестве нуклеофильной частицы нами был выбран амидоксим. После двухчасового кипячения смеси бис-(изонитрил)палладий дихлорида с амидоксимом в хлороформе растворитель был удален, точное количество полученного осадка растворяли в определенном объеме хлороформа, и далее использовали этот раствор в виде каталитических аликвот для проведения экспериментов по исследованию каталитической активности.
Схема 10
 |  |
|
Таблица 3
№ опыта | Катализатор 0.5 моль% | CuI % | PPh3 % | T0C | Раство-ритель | Основание | Время, ч | Конверсия (выход), % | TON | TOF, ч–1 |
1 | 3 | 10 | 1,5 | 55 | THF | Et3N | 24 | 75 | 150 | 6 |
Pd(CNBut)2Cl2 | 10 | 1,5 | 55 | THF | Et3N | 24 | 0 | 0 | 0 | |
2 | 3 | - | 1,5 | 65 | THF | Et3N | 24 | 62 | 124 | 5 |
Pd(CNBut)2Cl2 | - | 1,5 | 65 | THF | Et3N | 24 | 0 | 0 | 0 | |
3 | 3 | - | - | 65 | THF | Et3N | 24 | 13 | 26 | 1 |
Pd(CNBut)2Cl2 | - | - | 65 | THF | Et3N | 24 | 0 | 0 | 0 | |
4 | 3 | - | 2 | 50 | EtOH | K2CO3 | 4 | 20 | - | |
Pd(CNBut)2Cl2 | - | 2 | 50 | EtOH | K2CO3 | 4 | 20 | - | ||
5 | 3 | 10 | 3 | 55 | THF | Et3N | 24 | 74 | 150 | 6 |
6 | 3 | 10 | 1,5 | 65 | THF | Cs2CO3 | 24 | 73 | 150 | 6 |
|
На первом этапе тестов каталитической активности был проведен опыт в классических условиях, в среде тетрагидрофурана и поташа, как основания с добавкой CuI и PPh3, который показал умеренную каталитическую активность катализатора 3 даже в случае использования менее активного иодида. Для определения влияния присутствия CuI на конверсию арилиодида в следующих экспериментах была предпринята попытка провести реакцию Соногаширы в безмедных условиях реакции Хека. В этом случае наблюдалось существенное снижение каталитической активности, как и в экспериментах с катализаторами 1 и 2, что говорит о важности использования CuI как сокатализатора. Следующий опыт был проведен без добавок PPh3 и CuI, который показал существенное влияние PPh3 как возможного стабилизирующего или активирующего агента в реакции. Конверсия исходного арилиодида снизилась до минимальных значений. Механизм и природа PPh3-воздействия пока не изучена, и еще является предметом обсуждения. Данный факт стабилизирующей активности трифенилфосфина для ациклических диаминокарбеновых комплексов был открыт совсем недавно в нашей лаборатории, и работ, объясняющих природу стабилизации, пока не существует.
Опыт 4 (Таблица 3) показал, что оптимальным соотношением PPh3:[Pd] является 3:1 и дальнейшее увеличение концентрации PPh3 не приводит к увеличению конверсии продукта, а соответственно и к дополнительной стабилизации катализатора.
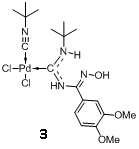
Получив хорошие результаты каталитической активности катализатора 3, нами было решено проанализировать соединение и установить его структуру. Комплексом физико-химических методов анализа был проанализирован остаток, получающийся по средством реакции нуклеофильного присоединение N-гидрокси-3,4-диметоксибензамидина к изонитрильной связи бис-(третбутилизонитрил)палладия дихлорида. Полученные результаты могут свидетельствовать в пользу предположительной структуры (Рисунок 8). Так в масс-спектре мы наблюдали массу соответствующего аминокарбеного комплекса минус Cl-, такая фрагментация характерна для подобных структур. В спектрах ЯМР 1H были найдены сигналы третбутильных протонов, которые не соответствуют таким же сигналам в исходном изонитрильном комплексе палладия, они лежат в более слабопольной области, к сожалению, из-за наличия нескольких нуклеофильных центров в молекуле, однозначно сделать заключение о структуре комплекса не представляется возможным без данных рентгеноструктурного анализа. Работы в этом направлении будут продолжены.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



