К 2 мл «раствора 1» последовательно добавляли 1 мл Et3N, 0,001 ммоль палладиевого катализатора и самым последним добавляли 0.004 г (0,02 ммоль) CuI. Далее реакционную смесь оставляли при постоянном перемешивании и нагревании на 24 часа. После завершения времени реакции отбирали 1 мл реакционной смеси и удаляли легкокипящие компоненты. Остаток растворяли в CDCl3 и снимали спектр ЯМР 1H, по которому определяли конверсию.
4.2.2. Приготовление реакционного «раствора 1»
В 15 мл тетрагидрофурана (ТГФ) растворили 0.351 г (1,50ммоль) 4-иоданизола, 0.129 г (1.53 мммоль) 2-метилбут-3-ин-2-ола, 6 мг трифенилфосфина (PPh3). Тщательно перемешали, добившись полного растворения компонентов раствора.
4.2.3. Опыт №1
Проводили три параллельные реакции. В три колбы (колбы пронумерованы №1, №2 и №3) на 10 мл оснащённые обратным холодильником и перемешиванием поместили по 2 мл раствора A и по стандартной схеме в соответствие с Процедурой А готовили реакционную смесь. В качестве палладиевых катализаторов в колбу №1 был добавлен 0,3 мг (1*10-3ммоль) бис-(третбутилизонитрил) палладия дихлорид (Pd(CNBut)2Cl2), в колбу №2 0,5 мг (1*10-3ммоль) Катализатор_3 и в колбу №3 0,7 мг (1*10-3ммоль) Катализатор_4. Температура масляной бани была 55 0С. Конверсия составила 0%, 75% и 8% соответственно.
4.2.4. Опыт №2
Проводили три параллельные реакции. В три колбы (колбы пронумерованы №1, №2 и №3) на 10 мл оснащённые обратным холодильником и перемешиванием поместили по 2 мл раствора A и по стандартной схеме в соответствие с Процедурой А готовили реакционную смесь, за исключением одного момента - реакция проводилась без добавления CuI. Добавление катализаторов осуществлялось в том же порядки, как и в предыдущим опыте. Температура масляной бани была 65 0С. Конверсия составила 0%, 62% и 4% соответственно.
4.2.5. Опыт №3
Проводили три параллельные реакции. В три колбы (колбы пронумерованы №1, №2 и №3) на 10 мл, оснащённые обратным холодильником и перемешиванием поместили по 2 мл раствора A и по стандартной схеме в соответствие с Процедурой А готовили реакционную смесь, только «раствор 1» был приготовлен без PPh3 и также как в Опыте №2 добавление CuI не осуществлялось. Добавление катализаторов осуществлялось в том же порядки, как и в предыдущих опытах. Температура масляной бани была 65 0С. Конверсия составила 0%, 13% и 0% соответственно.
4.2.6. Опыт № 4
Провели повторение Опыта №1. Только увеличили содержание PPh3 в 2 раза. Температура масленой бани также была 55 0С. При этом конверсия составила 0%, 74% и 9% соответственно.
4.2.7. Опыт №5
Провели повторение Опыта №1. Только вместо тетрагидрофурана было взято эквивалентное количество этанола, а вместо 1 мл Et3N 1 г K2CO3.
После 4 часов конверсия была определена качественно по данным ТСХ, и она составила приближённо 20%, 30% и 20% соответственно (оценка грубая).
5. Выводы
1. Ациклическими диаминокарбеновые комплексы палладия способны катализировать реакцию Соногаширы, как в присутствии, так и, в отсутствии CuI в качестве сокатализатора, в зависимости от условий реакции.
2. Добавка трифенилфосфина существенно повышает устойчивость каталитической системы.
3. Необходимо значительно меньшее количество катализатора (до 0,05%) по сравнению с широко используемыми фосфиновыми комплексами, реакции проходят при небольшом нагревании (20-65ОС) как в классических условиях (THF, Et3N), так и в среде этанола при использовании в качестве основания K2CO3.
4. Предложенные каталитические системы оказались не чувствительны к присутствию кислорода воздуха, что привело к упрощению процедуры подготовки растворителей и освободило от необходимости проведения реакции в инертной атмосфере.
6. Список используемой литературы
[1] Wanzlick, H. W.; Kleiner, H. J. Angew. Chem. 1961, 73, 493.
[2] Lemal, D. M.; Lovald, R. A.; Kawano, K. I. J. Am. Chem. Soc. 1964, 86, 2518.
[3] Winberg, H. E.; Carnahan, J. E.; Coffman, D. D.; Brown, M. J. Am. Chem. Soc. 1965, 87, 2055.
[4] Wiberg, N. Angew. Chem., Int. Ed. Engl. 1968, 7, 766.
[5] Denk, M. K.; Hatano, K.; Ma, M. Tetrahedron Lett. 1999, 40, 2057-2060.
[6] Wanzlick, H. W.; Scho. nherr, H. J. Liebigs Ann. Chem. 1970. 731, 176.
[7] Arduengo, A. J., III; Harlow, R. L.; Kline, M. J. Am. Chem. Soc. 1991, 113, 361.
[8] Arduengo, A. J., III; Goerlich, J.; Marshall, W. J. Am. Chem. Soc. 1995, 117, 11027.
[9] Alder, R. W.; Blake, M. E.; Bortolotti, C.; Bufali, S.; Butts, C. P.; Linehan, E.; Oliva, J. M.; Orpen, A. G.; Quayle, M. J. J. Chem. Soc., mun. 1999, 241.
[10] Enders, D.; Breuer, K.; Raabe, G.; Runsink, J.; Teles, J. H.; Melder, J. P.; Ebel, K.; Brode, S. Angew. Chem., Int. Ed. Engl. 1995, 34, 1021.
[11] Alder, R. W.; Allen, P. R.; Murray, M.; Orpen, G. Angew. Chem., Int. Ed. Engl. 1996, 35, 1121.
[12] Alder, R. W.; Blake, M. E. J. Chem. Soc., mun. 1997, 1513.
[13] Denk, M. K.; Thadani, A.; Hatano, K.; Lough, A. J. Angew. Chem., Int. Ed. Engl. 1997, 36, 2607.
[14] Heinemann, C.; Mu. ller, T.; Apeloig, Y.; Schwarz, H. J. Am. Chem. Soc. 1996, 118, 2023.
[15] Lehmann, J. F.; Urquhart, S. G.; Ennis, L. E.; Hitchcock, A. P.; Hatano, K.; Gupta, S.; Denk, M. K. Organometallics 1999, 18, 1862.
[16] Dixon, D. A.; Arduengo, A. J., III J. Phys. Chem. 1991, 95, 4180.
[17] Arduengo, A. J., III; Dias, H. V. R.; Dixon, D. A.; Harlow, R. L.; Klooster, W. T.; Koetzle, T. F. J. Am. Chem. Soc. 1994, 116, 6812.
[18] Cioslowski, J. Int. J. Quantum Chem., Quantum Chem. Symp. 1993, 27, 309.
[19] Heinemann, C.; Mu. ller, T.; Apeloig, Y.; Schwarz, H. J. Am. Chem. Soc. 1996, 118, 2023.
[20] Boehme, C.; Frenking, G. J. Am. Chem. Soc. 1996, 118, 2039.
[21] Alder, R. W.; Blake, M. E.; Bufali, S.; Butts, C. P.; Orpen, A. G.; Schu. tz, J.; Williams, S. J. J. Chem. Soc., Perkin Trans. 1 2001, 1586–1593.
[22] Kremzow, D.; Seidel, G.; Lehmann, C. W.; Furstner, A. Chem. Eur. J. 2005, 11, 1833–1853.
[23] Chugaev, L.; Skanavy-Grigorizeva, M. J. Russ. Chem. Soc. 1915, 47, 776.
[24] Rouschias, G.; Shaw, B. L. J. Chem. Soc. m. 1970, 183–183.
[25] Crociani, B.; Boschi, T.; Belluco, U. Inorg. Chem. 1970, 9, 2021–2025.
[26] Wanniarachchi, Y. A. and L. M. Slaughter, mun. 2007., 3294–3296.
[27] Burke, A., A. L. Balch, and J. H. Enemark, J. Am. Chem. Soc. 1970., 92, 2555–2557.
[28] Luzyanin, K. V.; Tskhovrebov, A. G.; Carias, M. C.; Guedes da Silva, M. F. C.; Pombeiro, A. J. L.; Kukushkin, V. Y. Organometallics 2009, 28, 6559–6566.
[29] D. Bourissou, O. Guerret, F. Gabbai, G. Bertrand, Chem. Rev. 100 (2000) 39–91.
[30] K. Denk, P. Sirsch, W. A. Herrmann, J. Organomet. Chem. 2002, 649, 219–224.
[31] W. A. Herrmann, K. Ofele, D. von Preysing, E. Herdtweck, J. Organomet. Chem. 2003, 684, 235–248;
[32] G. D. Frey, W. A. Herrmann, J. Organomet. Chem. 2005, 690, 5876–5880.
[33] D. Kremzow, G. Seidel, C. W. Lehmann, A. Furstner, Chem. Eur. J. 2005, 11, 1833–1853.
[34] E. L. Rosen, M. D. Sanderson, S. Saravanakumar, C. W. Bielawski, Organometallics 2007, 26, 5774–5777.
[35]. Alder, R. W., L. Chaker, and F. P. V. Paolini, mun. 2004, 2172–2173.
[36]. Otto, M., S. Coejero, Y. Canac, V. D. Romanenko, V. Rudzevitch, and
G. Bertrand, J. Am. Chem. Soc. 2004, 126, 1016–1017.
[37]. Arduengo, A. J., III, H. V. R. Dias, R. L. Harlow, and M. Kline, J. Am. Chem. Soc. 1992, 114, 5530–5534.
[38] M.-T. Lee, C.-H. Hu, Organometallics 2004, 23, 976–983.
[39] A. L. Steinmetz, B. V. Johnson, Organometallics 1983, 2, 705–709.
[40] K. Denk, P. Sirsch, W. A. Herrmann, J. Organomet. Chem. 2002, 649, 219.
[41] A. I. Moncada, M. A. Khan, L. M. Slaughter, Tetrahedron Lett. 2005, 46,1399–1403.
[42] Moncada, S. Manne, J. M. Tanski, L. M. Slaughter, Organometallics 2006, 25, 491–505.
[43] B. Dhudshia, A. N. Thadani, mun. 2006, 668–670.
[44] Sonogashira, K., Tohda, Y., Hagihara, N. Tetrahedron Lett. 1975, 4467-4470
[45] Bohm, V. P. W., Herrmann, W. A. Eur. J. Org. Chem.2000, 3679-3681.
[46] Gil-Molto, Juan; Najera, Carmen Advanced Synthesis and Catalysis 2006, 348, 1874–1882
[47] Buchmeiser, M. R.; Schareina, T.; Kempe, R.; Wurst, K. J. Organomet. Chem. 2001, 634, 39.
[48] Gil-Molto., J.; Na. jera, C. Eur. J. Org. Chem. 2005, 4073.
[49] Eisnor, C. R.; Gossage, R. A.; Yadav, P. N. Tetrahedron 2006, 62, 3395.
[50] Arques, A.; Aun˜o. n, D.; Molina, P. Tetrahedron Lett. 2004, 45, 4337.
[51] Nishide, K.; Liang, H.; Ito, S.; Yoshifuji, M. J. Organomet. Chem. 2005, 690, 4809.
[52] Batey, R. A.; Shen, M.; Lough, A. J. Org. Lett. 2002, 4, 1411.
[53] Mas-Marza., E.; Segarra, A. M.; Claver, C.; Peris, E.; Ferna. ndez, E. Tetrahedron Lett. 2003, 44, 6595.
[54] Ma, Y.; Song, C.; Jiang, W.; Wu, Q.; Wang, Y.; Liu, X.; Andrus, M. B. Org. Lett. 2003, 5, 3317.
[55] L. Jafarpour, S. P. Nolan, Adv. Organomet. Chem. 2000, 181.
[56] E. Peris, R. H. Crabtree, Coord. Chem. Rev. 2004, 248, 2239
[57] F. Glorius, Top.Organomet. Chem., Vol. 21, (Vol. Ed. F. Glorius), Springer-Verlag, Berlin Heidelberg, 2007, pp. 1–20.
[58] P. Frémont, N. Marion, S. P. Nolan, Coord. Chem. Rev. 2009, 253, pp. 862–892.
[59] S. P. Nolan, O. Navarro, Comprehensive Organometallic Chemistry III, 1st ed.; Vol. 11, Ch. 11.01, (Ed. A. Canty), Elsevier, Oxford, 2007, pp. 1–38
[60] Dulog, Lothar; Koerner, Bernd; Heinze, Juergen; Yang, Jianjun, Liebigs Annalen, 1995,9 ,1663 – 1672.
[61] Dhudshia, B.; Thadani, A. N. mun 2006, 668–670.
[62] Kirsch, G.; Hesse, S.; Comel, A. Curr. Org. Synth. 2004, 1, 47–63.
[63] Balova, I. A.;Morozkina, S. N.; Sorokoumov, V.N.;Vinogradova, O. V.; Knight, D. W.; Vasilevsky, S. F. Eur. J. Org. Chem. 2005, 882–888.
7. Приложение
1-нитро-2-(окт-1-инил)бензол
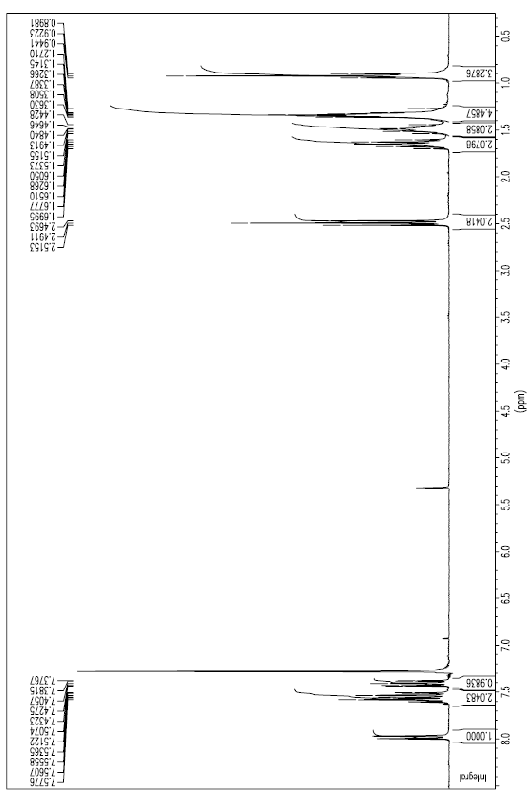

1-(додека-1,3-диинил)-2-нитробензол
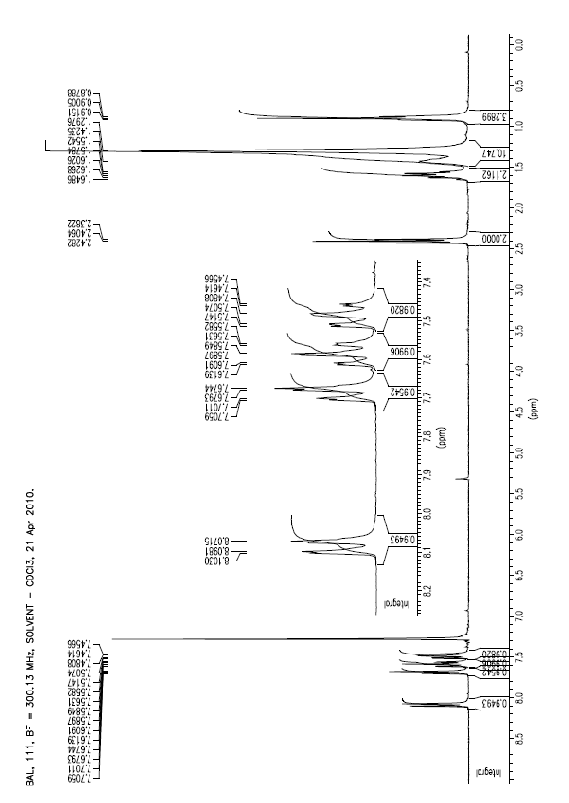


|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



