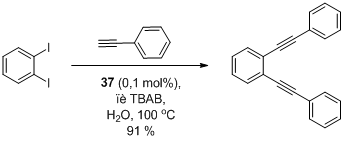
Схема 7
Существуют примеры, где в качестве катализатора используют бис-оксозалиновые комплексы палладия. Таким образом, комплекс 17 в количестве 0,055 моль% катализировал реакцию кросс-сочетания йодбензола с фенилацетиленом на воздухе в пирролидине при 90 °С с большим количеством йодида меди (50 моль%) за 3 часа, выход составил 32 % [49].
Рисунок 6
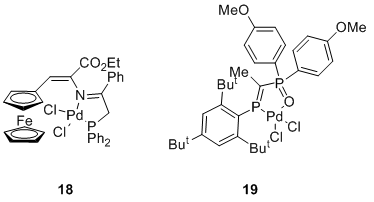
Есть примеры P, N - и P, O-бидентантных комплексных палладиевых катализаторов. К этой категории принадлежит комплекс 18 (Рисунок 6), содержащий ферроценовую основу с фосфиниминовым лигандом, который проявляет достаточно высокую каталитическую активность [50]. Комплекс 19, содержащий Р, О-бидентантный 3-оксо-1,3-дифосфопропеновый лиганд, катализировал реакцию йодбензола с фенилацетиленом при использовании триэтиламина в качестве основания и растворителя, при комнатной температуре, с выходом до 68% [51].
Бесспорно, в современной химии самой распространённой группой палладиевых катализаторов, которые уже являются эффективной заменой классическим фосфиновым, являются NHCs комплексы палладия. К примеру, комплекс 20 (1 моль%) (Рисунок 7) показал хорошую каталитическую активность в реакциях кросс-сочетания дезактивированных арилбромидов с алкинами при 80 °C в DMF с триэтиламином как основанием [52]. Интересным является факт катализа тридентантным комплексом 21, который тестировался на примере реакции иодбензола с фенилацетиленом при кипечении в пирролидине, который показал высокую каталитическую активность [53]. Причем отмечалось, что если не было избытка основания, то выпадала палладиевая чернь.
Рисунок 7
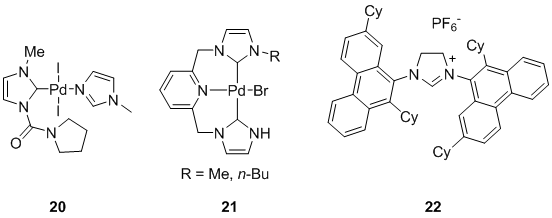
Существует также множество примеров, где катализирование происходит in situ образованными N-гетероциклическими комплексами палладия посредством добавления свободных карбенов. Таким образом, стерически насыщенная фенантраценилимидазоливая соль, такая как 22, была исследована в качестве лигандной добавки (3 моль%) к Pd(PPh3)2Cl2 (3 моль%) в безмедном кросс-сочетании в ТГФ при температуре 65 0С при использовании требутоксида калия и этот подход оказался очень эффективным [54].
Для NHCs комплексов палладия существует огромное количество примеров их каталитической активности в реакции Соногаширы. Однако для их ациклических аналогов (ADCs) примеров катализа этой реакции на данный момент не существует.
3. Обсуждение результатов
3.1. Исследование каталитической активности ациклических аминокарбеновых комплексов 1 и 2
В нашем распоряжении оказались два аминокарбеновых комплекса палладия (1), (2) (Рисунок 8) синтезированных в научной группе профессора По реакции замещеного амидина с изонитрильными комплексами палладия.
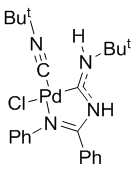
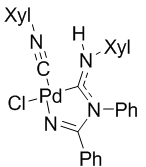 Рисунок 8
Рисунок 8
|
|
Подобные комплексы проявили высокую каталитическую активность в реакции Сузуки [28]. Это дало нам основание полагать, что данный тип катализаторов окажется эффективным и в других реакциях кросс-сочетания. Принимая во внимание богатый синтетический опыт в проведении реакции Соногаширы, имеющийся в нашей научной группе как для моно-, так и для диацетиленов, не удивительно, что именно эта реакция была выбрана для исследования. Несмотря на то, что большое количество палладиевых катализаторов имеющих как фосфорные, так и азотистые лиганды были всесторонне исследованы в реакции Соногаширы, в литературе был найден лишь единственный пример исследования каталитической активности ациклического аминокарбенового комплекса палладия (II) [61].
В качестве модельной была выбрана реакция 1-йод-2-нитробензола с окт-1-ином (Схема 8), это было связано большим интересом к ортозамещенным арилацетиленам. Последние широко применяются в синтезе фармакологически важных замещенных гетероциклов таких как индолы, хинолины, изохинолины, индоло[1,2-с]хинолины, фуропиридины и пиразолины [62].
Схема 8
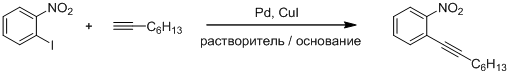
На первом этапе было решено провести реакцию в классических условиях в среде тетрагидрофурана с использование триэтиламина в качестве основания и CuI как сокатализатора, PPh3 был добавлен для увеличения устойчивости палладиевого комплекса в условиях реакции (Таблица 2, опыты 1-5).
Таблица 2. Определение каталитической активности комплексов 1 и 2 в реакции Соногаширы.
№ опыта | Катализатор | Загрузка катализатора, моль% | Растворитель | Основание | Время, ч | Конверсия (выход), % | TON | TOF, ч–1 |
1 | 1 | 0.07 | THF | Et3N | 96 | 99 (94) | 1400 | 150 |
2 | 2 | 0.07 | THF | Et3N | 68 | 99 | 1400 | 150 |
3 | 1 | 0.07 | THF | Et3N | 24 | 99 | 1400 | 60 |
4 | 2 | 0.07 | THF | Et3N | 12 | 99 | 1400 | 1200 |
5 | 1 | 0.07 | THF | Et3N | 24 | 20 | 290 | 12 |
6 | 1 | 0.07 | EtOH | K2CO3 | 24 | – | – | – |
7 | 2 | 0.07 | EtOH | K2CO3 | 24 | 10 | 140 | 6 |
8 | 1 | 0.07 | EtOH | K2CO3 | 20 | 99 (96) | 1400 | 100 |
9 | 2 | 0.07 | EtOH | K2CO3 | 5 | 99 | 1400 | 280 |
10 | [PdCl2(PPh3)]2 | 0.1 | EtOH | K2CO3 | 18 | 40 | 400 | 22 |
11 | 1 | 0.1 | EtOH | K2CO3 | 18 | 99 | 990 | 55 |
12 | 2 | 0.1 | EtOH | K2CO3 | 4 | 99 | 990 | 250 |
13 | 2 | 0.05 | EtOH | K2CO3 | 18 | 99 | 2000 | 110 |
Во всех случаях в реакцию были взяты 1-иод-2-нитробензол (0.610 г, 2.45 ммоль) и окт-1-ин (0.550 г, 5.00 ммоль). Во всех случаях кроме 6 и 7, CuI (0.045г, 9.60 ммоль%) был добавлен как сокатализатор, и во всех случаях кроме 5, PPh3 (0.030 г, 4.60 ммоль%) был добавлен в реакционную смесь. Все опыты были проведены при температуре 60 ºC кроме 1 и 2 (проводились при 20 ºC). Конверсия определялась на основе анализа спектров ЯМР (1H).
При комнатной температуре полная конверсия исходного арилйодида была достигнута через 96 часов (для катализатора 1) и через 68 часов (для катализатора 2) (Таблица 2, Опыты 1,2). Препаративный выход в реакции после хроматографического разделения составил 94%. Увеличение температуры до 600С реакции позволило сократить время полной конверсии до 24 и 12 часов соответственно (Таблица 2, Опыты 3,4). Кроме того, нами было обнаружено, что добавление PPh3, довольно существенно влияет на скорость реакции и конверсию в реакции, в условиях опыта 5 через 24 часа конверсия составила лишь только 20%.
Ранее было показано, что ациклические диаминокарбеновые комплексы палладия являются устойчивыми и в протонных растворителях (EtOH) в присутствии оснований (K2CO3, Cs2CO3). В подобных условиях они проявляют существенную каталитическую активность в реакции Сузуки. Мы решили протестировать данные условия в приложении к реакции Соногаширы. В среде этанола при использовании поташа, как основания, целевой 1-нитро-2-(окт-1-инил)бензол был получен с количественным выходом (Таблица 2, Опыты 8,9). Как и в предыдущих экспериментах, палладиевый комплекс 2 проявил несколько большую каталитическую активность – 99% конверсия была достигнута через 20 и 5 часов соответственно.
В литературе имеются примеры проведения реакции Соногаширы без использования Cu+ в качестве сокатализатора, иногда такие условия оказываются предпочтительными, т. к. соли одновалентной меди способны катализировать реакции циклизации ортозамещенных арилацетиленов. Мы решили исследовать влияние добавки CuI на ход реакции при использовании аминокарбеновых комплексов 1 и 2 (Таблица 2, Опыты 6, 7) Было отмечено существенное снижении скорости реакции кроссочетания в случае использования каталитической системы на основе комплекса 2 в отсутствие меди. Так через 24 часа наблюдалась лишь 10% конверсия исходного арилйодида. Образование продуктов реакции зафиксировано не было при использовании катализатора 1, в отсутствии меди. В дальнейшем был проведен ряд опытов показавший, что оптимальным является использование CuI в количестве 5-10% мольных процентов. Полученные данные, позволяют сделать вывод о значительном влиянии одновалентной меди на каталитический цикл в случае ациклических диаминокарбеновых комплексов палладия.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



