Значение титрования без липазы (время реакции “0”) вычитают из величины последующих титрований. В этом случае полученные графики пройдут через начало координат, поскольку так учитывается наличие органических и желчных кислот в молоке (исходная кислотность молока) до начала действия липазы.
Пример графика зависимости содержания свободных ВЖК от времени инкубации:
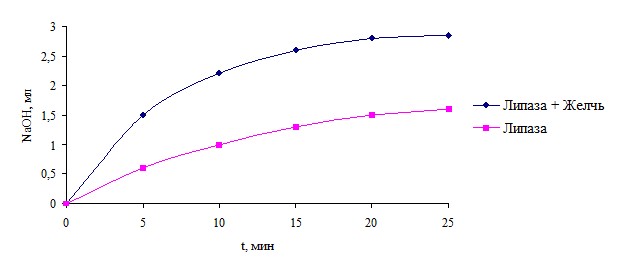
Схема определения
I. Приготовление исходной смеси (в стаканчиках) | ||
Реактивы и этапы | Стаканчик 1 | Стаканчик 2 |
1. Разбавленное (1:1) молоко 2. Вода 3. Желчь | 10 мл- 1 мл | 10 мл 1 мл - |
II. Определение исходной кислотности молока | ||
Колба для титрования 1 | Колба для титрования 2 | |
1. Исходная смесь (отбирают аликвоту из стаканчика в колбочку для титрования) 2. Фенолфталеин (добавляют в каждую колбочку) Титруют пробы раствором NaOH (до розового цвета). Значения записывают в таблицу результатов (V0 и V0 ’). | 2 мл 1-2 кап | 2 мл 1-2 кап |
III. Отбор смеси и титрование в присутствии липазы | ||
К оставшейся исходной смеси в оба стаканчика быстро добавляют по 1мл липазы и отмечают время. Через 5 мин отбирают аликвоты в колбы для титрования | ||
Колба для титрования 1 | Колба для титрования 2 | |
1. Аликвота 2. Фенолфталеин Быстро титруют раствором NaOH (до розового цвета). Значения записывают в таблицу результатов (V и V ’) Повторные титрования проводят через каждые 5 мин и результаты заносят в следующую таблицу. | 2 мл 1-2 кап | 2 мл 1-2 кап |
Оформление результатов
V(NaOH), мл t, мин | проба № 1 (с желчью) | проба № 2 (без желчи) | ||
V | V-V0 | V’ | V’-V0 ’ | |
0 (определение исходной кислотности молока) | V0 = | 0 | V0 ’= | 0 |
5 | V = | V’= | ||
10 | ||||
15 | ||||
20 | ||||
по получен-ным данным строят кинетическую кривую № 1 | по получен-ным данным строят кинетическую кривую № 2 |
Выводы
Занятие 14.
14.1. Семинар: «Расчёт энергетического эффекта распада высших жирных кислот и глицерина».
Используя пример расчёта баланса энергии в учебнике (, , издание третье, с 376 -377) проведите расчёт количества АТФ, образующегося при окислении молекул:
А) стеариновой кислоты
Б) олеиновой кислоты
Г) пальмитиновой кислоты
14.2. Лабораторная работа: «Определение ацетоновых тел в моче».
К ацетоновым телам относятся ацетон, в-гидроксимасляная кислота и ацетоуксусная кислота.
В норме моча млекопитающих животных и человека содержит незначительные количества ацетоновых тел, которые не выявляются обычными химическими реакциями. Повышенное выделение ацетоновых тел с мочой наблюдается при нарушении жирового или углеводного обмена, при голодании и неправильном режиме питания.
Для обнаружения веществ, которые в моче здорового человека и животных не встречаются в аналитически определяемых количествах (белки, глюкоза, кетоновые тела, билирубин и гемоглобин) можно использовать экспресс-методы полуколичественного анализа (так называемые, тест-полоски).
Цель работы
Провести экспресс-тесты с 5 образцами мочи. Определить рН каждого из образцов, а также содержание белка, кетоновых тел, глюкозы. Проанализировать полученные результаты.
Принцип метода
О концентрации того или иного реагента можно судить по изменению окраски сенсорной зоны, сопоставив полученный результат с соответствующей цветной шкалой на упаковке.
Сенсорная или реакционная зона любой тест-полоски (для определения глюкозы, кетонов, белка, нитритов, билирубина, уробилиногена и т. д.) представляет собой некую матрицу, в которой находится много различных сбалансированных химических компонентов. Наряду с химическими компонентами в некоторые сенсорные зоны тест-полосок вводят ферменты, специфически взаимодействующие с определяемым веществом в пробе. Тест-полоски с наличием ферментов в сенсорной зоне называют ферментативными.
Чтобы результаты определения были корректными, определение необходимо проводить в строгом соответствии с прилагаемой инструкцией по применению.
Реагенты, используемые в сенсорной зоне
№ п/п | Анализируемое соединение | Рабочий реагент |
1 | белок | Эфир тетрабромфенолфталеина, тетрабромфеноловый синий |
2 | глюкоза | Глюкозооксидаза, пероксидаза, тетраметилбензидин |
3 | кетоновые (ацетоновые) тела | Натрия нитропруссид |
4 | рН | Метиловый красный, бромтимоловый синий |
Примечание:
Проба, анализируемая на наличие белка, наиболее чувствительна к альбумину, значительно менее чувствительна к глобулинам, мукопротеинам, гемоглобину. На определение белка не влияет величина рН мочи, но в сильно щелочной моче (рН выше 8) или в моче с высокой буферной емкостью тест может дать ложноположительные результаты. Не обращайте внимания на окраску сухой зоны.
Определение глюкозы основано на ферментативной (глюкозоксидаза/пероксидаза) реакции, тест специфичен для глюкозы, другие сахара не взаимодействуют. Реакция не зависит от рН и присутствия кетоновых тел.
Кетоны - проба значительно чувствительнее к ацетоуксусной кислоте, чем к ацетону. С бета-гидроксимасляной кислотой проба не реагирует. Лекарственные и диагностические препараты на основе фенолфталеина, присутствующие в моче, могут в щелочной среде зоны окрашиваться в красный и даже пурпурный цвет. Цветная шкала сравнения на этикетке отражает концентрацию ацетоуксусной кислоты в моче.
Выполнение работы
Тест-полоску опускают на 1-2 с. в исследуемый образец так, чтобы сенсорные зоны были смочены. Капли мочи с полоски удаляют, проведя полоской по краю сосуда с мочой. Полоску оставляют в горизонтальном положении. Приблизительно через 60 с. сопоставляют окраску зон индикации с соответствующей цветной шкалой.
Оформление работы
I обра-зец | II обра-зец | III обра- зец | IV обра- зец | V обра- зец |
рН | ||||
Белок | ||||
Глюкоза | ||||
Кетоновые тела |
Выводы
fРаздел 8e
Обмен простых и сложных белков.
Белковому обмену принадлежит особое место среди других видов обмена веществ. Это объясняется выполнением белками специфических функций, которые не могут заменить ни углеводы, ни липиды: пластической, каталитической, иммунной.
Белки направляют и регулируют обмен веществ, создавая оптимальные условия для их собственного воспроизводства в живых системах. Исключение белка из клрма животных не столько сказывается на уменьшении массы органов и ткани, сколько в снижении активности ферментов, замедлении биосинтеза белка.
Поскольку белки всех организмов отличаются строгой видовой и тканевой специфичностью, организм человека и моногастричных животных использует белки пищи только после их полного гидролиза до АМК в желудочно-кишечном тракте под действием ряда протеолитических ферментов – петидаз. Все пептиды в зависимости от места расположения гидролизуемой пептидной связи делятся на:
1) эндопептидазы, гидролизующие пептидные связи, удалённые от концов пептидной цепи: пепсин, трипсин, химотрипсин, эластаза.
2) экзопептидазы, гидролизующие пептидые связи, образованные N - и C-концевыми аминокислотами: аминопептидаза, карбоксипептидаза, дипептидаза.
Желудочные и панкреатические пептидазы вырабатываются в неактивной форме, секретируются в месте действия, где активируются путём частичного протеолиза. Такой механизм образования активных ферментов необходим для защиты секреторных клеток желудка и поджелудочной железы от самопереваривания.
Переваривание белков в желудке происходит под действием пепсина. Профермент пепсиноген вырабатывается главными клетками слизистой желудка и при поступлении пищи секретируется в полость желудка. Пепсиноген активируется двумя способами:
1) соляной кислотой (медленно);
2) аутокаталитически (быстро) уже имеющимся пепсином
Желудочный сок содержит соляную кислоту, которая вырабатывается обкладочными клетками желудка и выполняет следующие функции:
1) оказывает бактерицидное действие;
2) вызывает частичную денатурацию белков пищи;
3) создаёт оптимум рН для пепсина;
4) активирует пепсиноген путём частичного протеолиза
Переваривание белков в кишечнике моногастричных животных происходит под действием:
1) ферментов поджелудочной железы: трипсина, химотрипсина, эластазы, карбоксипептидаз;
2) ферментов тонкой кишки: аминопептидаз, дипептидаз, трипептидаз.
Активная форма трипсина образуется в кишечнике при участии энтеропептидазы, которая отщепляет от N-конца трипсиногена гексапептид, что приводит к изменению конформации молекулы и формированию активного центра трипсина.
Остальные протеазы панкреатического сока: химотрипсиноген, прокарбоксипептидаза, проэластаза – активируются трипсином.
Активация панкреатических пептидаз происходит по каскадному механизму. Кишечные пептидазы синтезируются в энтероцитах сразу в активной форме.
Конечным результатом переваривания белков является образование свободных АМК, поступающих в клетки слизистой оболочки кишечника путём активного транспорта.
Переваривание белков жвачных животных происходит в основном в рубце, где осуществляется распад практически всех белков под действием ферментов бактерий (в основном, стрептококков) и простейших (инфузорий).
Большая часть свободных АМК, образующихся в результате переваривания белков, используется для синтеза собственных белков организма, часть на синтез биологически активных молекул: гормонов, биогенных аминов, а также нуклеотидов, гемма, креатинфосфата и многих других соединений, в том числе глюкозы в процессе глюконеогенеза.
Важнейший путь превращения АМК в организме – это реакции трансаминирования с б-кетокислотами с образованием новых (заменимых) АМК.
Ещё один путь метаболизма – декарбоксилирование АМК с образованием биологически активных молекул – биогенных аминов. Основным коферментом обмена АМК является пиридоксальфосфат (ПФ).
Деградация АМК происходит путём их дезаминирования: безазотистые остатки могут использоваться для синтеза глюкозы (глюконеогенез) или, превращаясь в ацетил-КоА, окисляться до углекислого газа и воды с образованием энергии (различаю гликогенные и кетогенные АМК).
В организме человека и животных ежесуточно распадается до аминокислот (АМК) около 400 г белков и столько же синтезируется. Основным источником АМК для человека являются пищевые белки. Суточная норма потребления белков для человека составляет около 100 г. Все 20 АМК, которые входят в состав белков организма, можно разделить на заменимые (синтезируемые самим организмом) и незаменимые (не синтезируются и должны поступать с пищей). Присутствие в пищевых белках всех незаменимых АМК определяет полноценность белкового питания человека и животных.
При недостаточном содержании бека в корме животного, неполноценном по аминокислотному составу, а также при заболеваниях желудочно-кишечного тракта происходит снижение его роста, замедление развития, нарушение репродуктивных функций, снижается сопротивляемость к инфекциям, а у сельскохозяйственных животных наблюдается снижение молочной и мясной продуктивности.
Вопросы для внеаудиторной теоретической работы по разделу:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |



