Таблица 2.1
Значения константы скорости реакции окисления FeS водяным паром (расход пара 1 л/мин)
Объем H2O в дутьё, % | t, єC | -lgK |
10 | 1150 1250 1350 | 1,221 1,045 0,833 |
35 | 1150 1250 1350 | 0,986 0,581 0,658 |
50 | 1150 1200 1250 1350 | 0,670 0,574 0,444 0,134 |
Скорость реакции растет с температурой. Например (рис. 2.1, а, б), за две минуты с начала эксперимента степень десульфуризации FeS увеличилась с 29 (при 1150 єС) до 75% (при 1250 єС).
Скорость окисления может быть выражена уравнением
V = 0,244 + 0,00362 (t - 1150), (2.4)
где V – скорость окисления, мг/с; t - температура, єС.
На скорость окисления влияет содержание водяного пара в дутье (см. рис. 2.1, а). Так, при увлажнении с 10 до 50% при 1250 єС соответствующая зависимость описывается формулой
V = 0,206 + 0,0131 (![]()
![]() - 10), (2.5)
- 10), (2.5)
где ![]()
![]() - содержание водяного пара в дутье, %.
- содержание водяного пара в дутье, %.
Минералогическим анализом продуктов взаимодействия подтверждено, что реакция описывается преимущественно стехиометрическим уравнением (2.1), т. е. окисление протекает до закиси железа. При избытке водяного пара и незначительной концентрации сернистого железа вюстит в отсутствии кремнезема окисляется до магнетита.
Результаты по окислению сульфида меди Cu2S водяным паром приведены на рис. 2.1, в, г.
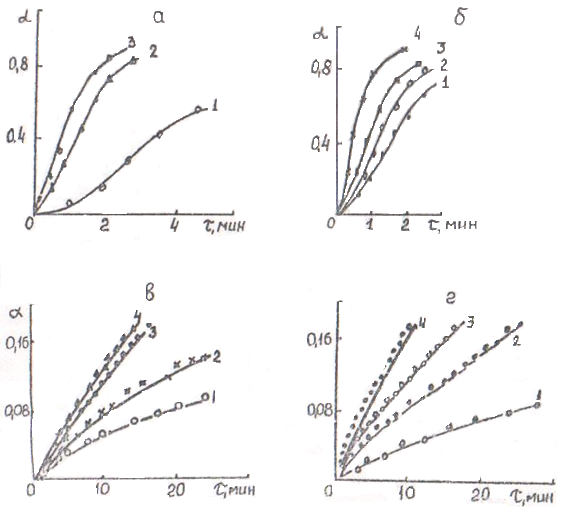
Рис. 2.1. Изменение степени десульфуризации FeS (а, б) и Cu2S (в, г) в зависимости от продолжительности опыта;
а, в: 1-10, 2-35, 3-50, 4-70% H2O (t = 1250 єC)
б, г: 1-1150, 2-1200, 3-1250, 4-1300 єС (![]()
![]() = 50%)
= 50%)
Как в случае FeS, так и Cu2S скорость десульфуризации практически не зависит от изменения концентрации серы в расплаве (таблю 2.2, 2.3). значение энергии активации составило 120-136 кДж/г-моль FeS и 180-200 кДж/г-моль Cu2S.
Зависимость энергии активации от природы сульфида можно объяснить либо существованием активационных затруднений в сульфидной фазе – затрудненным разрывом связей атомов металла с серой, либо неодинаковой адсорбируемостью молекул воды на разных сульфидах и в связи с этим различными энергетическими затруднениями в процессе отрыва атома кислорода от молекул водорода.
| t, єC | Степень десульфуризации, % | V · 106, г-атом/(см2·с) | ||
Опыт 1 | Опыт 2 | Опыт 1 | Опыт 2 | ||
10 | 1150 1250 1300 | 33,62 33,12 32,71 | 27,10 26,21 25,48 | 0,70 1,00 1,72 | 0,95 1,46 2,15 |
35 | 1150 1200 1250 | 33,62 33,30 33,12 | 23,11 22,12 22,61 | 1,09 2,02 2,84 | 1,85 2,51 4,74 |
50 | 1150 1200 1250 1300 | 32,94 33,39 33,67 34.21 | 23,11 23,78 23,49 23,84 | 2,25 2,75 3,55 7,56 | 3,60 4,57 6,46 12,20 |
Следует отметить, что большие значения скоростей десульфуризации в случае расплава FeS, по сравнению с Cu2S, находятся в соответствии с представлениями о большей энергии связи между атомами меди и серы.
Высказано предположение о том, что наиболее вероятной лимитирующей стадией окисления сульфида железа при продувке парогазовой смесью является массоперенос в расплаве, т. е. в целом окисление FeS протекает в диффузионном режиме на границе раздела фаз. В начальный момент процесса, по мнению авторов, протекают реакции
FeS + 3H2O = FeO + SO2 + 3H2, (2.6)
FeS + 3Fe3O4 = 10FeO + SO2, (2.7)
3FeO + H2O = Fe3O4 + H2, (2.8)
а по мере падения концентрации FeS становятся вероятными реакции (2.8) и (2.1).
Взаимодействие сульфидов металлов с водяным паром при низких температурах исследовано в 20-х гг. Томпсоном и Тиллингом, Они изучили десульфуризацию серного колчедана в атмосфере воздуха; воздуха, насыщенного паром, и пара. Показано, что при обработке водяным паром с повышением температуры до 430 °С в огарке увеличивается содержание растворимой серы, по мнению авторов, сульфатной. При температуре выше 680°С сульфаты железа разлагаются. Эти данные, несомненно, нуждается в серьезном экспериментальном подтверждении.
Большое внимание уделяется переработке халькопиритных руд и халькопирита. Главная цель изучения взаимодействия халькопирита с водяным паром - последующее селективное разделение сульфидов меди и железа. Исследования проводили при температурах выше 400 °С. При этом халькопирит превращается в магнетит Fe3O4, борнит Cu5FeS4 и следы Cu4,96S.
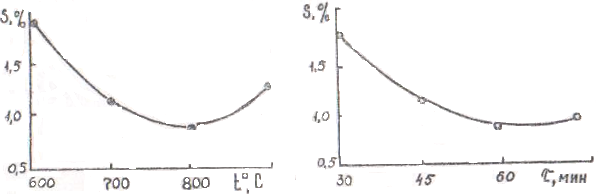
Рис.2.4. Зависимость содержания Рис.2.5. Зависимость содержания
остаточной серы от температуры. остаточной серы от продолжитель -
ности процесса.
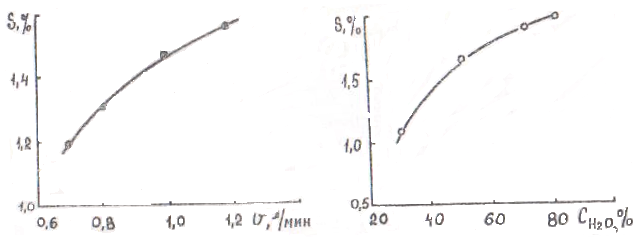
Рио.2.6. Зависимость содержания Рис.2.7. Зависимость содержания остаточной серы от скорости остаточной серы от количества подачи воздуха водяных паров в парогазовой смеси
Реакция пара о большинством сульфидов металлов имеет очень маленький коэффициент равновесия. В связи с этим для поглощения отходящих газов использована известь ( табл. 2.8 ).
Для исследования реакций взаимодействия сульфидов металлов о водяным паром в присутствии СаО брали таблетку сульфида металла, причем большое влияние на степень превращения оказывает пористость образца (рис.2.8). Процесс взаимодействия
Таблица 2.8.
Энергия Гиббса реакций взаимодействия сульфидов
металлов с водяным паром.
Реакция | МеxS | Энергия Гиббса, ДGє, кДж/моль | ||
900К | 1000К | 1100К | ||
CaO + H2S(r) = CaS + H2O(r) | - | -75,1 | -70,4 | -66,4 |
MexS + H2O = MexO + H2S | MoS2 ZnS NiS Cu2S FeS PbS | 56,2 65,0 75,6 150,4 50,2 107,2 | 55,1 64,8 77,6 155,2 51,0 108,0 | 54,1 64,2 79,5 159,1 51,6 109,0 |
MeS + CaO = MexO + CaS | MoS2 ZnS NiS Cu2S FeS PbS | -19,2 -10,4 -0,2 -75,0 -25,2 -31,8 | -15,3 -5,6 7,2 84,8 -19,4 37,6 | -12,3 -2,2 13,1 92,7 -14,8 42,6 |
Реакция с сульфидом цинка протешет по следующей схеме:
ZnS + H2O = ZnO + H2S, (2.40)
H2S + CaO = CaS + H2O (2.41)
ZnS + CaO = ZnO + CaS (2.42)
Избыток СаО оказывает благоприятные последствия на весь
ход реакций (рис.2.10).
Кинетическое уравнение, выведенное на основе этой реакции,
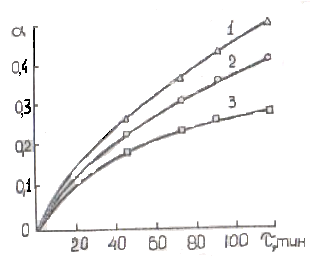
Рис.2.10.Зависимость степени превращения сульфида цинка от времени при отношении в смеси СaO: ZnS 1-4,0; 2-3,0; 3-2,0
На основании рассмотренных примеров можно сделать вывод, что возможно оксидировать сульфиды цветных металлов и без расплавления, применяя в качестве окислителя водяной пар. Имеются реальные пути исключения из технологических процессов вредных серосодержащих газов путем получения товарного сульфида кальция.
Окисление сульфидов свинца и цинка
Свинец встречается в природе в виде ряда сульфидных минералов, наиболее важных из которых – галенти (свинцовый блеск) PbS. Он присутствует во всех сульфидных рудах гидротермального происхождения. Залежам свинцового блеска обычно сопутствуют месторождения англезита PbSO4. В СНГ свинец получают почти исключительно из сульфидных руд, которых содержится сульфид цинка ZnS.
В представлены первые сведения о поведении сульфидов цинка и свинца при нагревании в атмосфере водяного пара. Однако прежде чем излагать эти результаты, рассмотрим кратко основные свойства PbS, ZnS и продуктов их окисления.
Сульфид свинца - черно-серые кристаллы с металлическим блеском кубической структуры (б = 0,59362 нм), температура плавления 1114 °С. При нагревании на воздухе до 400-500 °С окисляется с образованием сульфата, основных сульфатов и оксида свинца:
2PbS + 3O2 = 2PbO + 2SO2 (основная реакция),
РbS + 2O2 = PbSO4 (побочная).
Водородом PbS восстанавливаются до металлического свинца при температуре около 600 °С:
PbS + H2 = Pb + H2S
Металлический свинец взаимодействует с кислородом, серой
и сериястым газом по реакциям:
3Pb + 2O2 = Pb3O4 + 175,6 ккал, (2.103)
Pb + ![]()
![]() O2 = PbO + 51,96 ккал, (2,104)
O2 = PbO + 51,96 ккал, (2,104)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |




